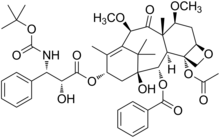
Кабазитаксел
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Джевтана |
| Другие имена | XRP-6258 |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а611009 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | внутривенный |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| КЭБ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.205.741 |
| Химические и физические данные | |
| Формула | С 45 Н 57 Н О 14 |
| Молярная масса | 835.944 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Кабазитаксел , продаваемый под торговой маркой Джевтана , представляет собой полусинтетическое производное природного таксоида . [ 3 ] Это ингибитор микротрубочек , [ 2 ] и четвертый таксан, который будет одобрен в качестве средства для лечения рака . [ нужна ссылка ]
Кабазитаксел был разработан компанией Санофи-Авентис и одобрен Управлением по контролю за продуктами и лекарствами США (FDA) для лечения гормонорезистентного рака простаты в июне 2010 года. [ 4 ] [ 5 ] [ 6 ] Он доступен в виде непатентованного лекарства . [ 7 ] [ 8 ]
Медицинское использование
[ редактировать ]Кабазитаксел показан в сочетании с преднизолоном для лечения метастатического кастрационно-резистентного рака простаты после лечения на основе доцетаксела . [ 2 ]
Механизм действия
[ редактировать ]Таксаны усиливают стабилизацию микротрубочек и ингибируют митоз и деление клеток. [ 9 ] Более того, таксаны предотвращают передачу сигналов андрогенного рецептора (AR) путем связывания клеточных микротрубочек и связанного с микротрубочками моторного белка динеина, тем самым предотвращая ядерную транслокацию AR. [ 10 ]
Клинические испытания
[ редактировать ]У людей с метастатическим кастрационно-резистентным раком предстательной железы (мКРРПЖ) общая выживаемость (ОВ) заметно увеличивается при применении кабазитаксела по сравнению с митоксантроном после предварительного лечения доцетакселом. FIRSTANA (идентификатор ClinicalTrials.gov: NCT01308567) оценила, действует ли кабазитаксел в дозе 20 мг/м2. 2 (C20) или 25 мг/м 2 (C25) превосходит доцетаксел 75 мг/м 2 (D75) с точки зрения общей выживаемости у пациентов с мКРРПЖ, ранее не проходивших химиотерапию. Однако C20 и C25 не продемонстрировали превосходства по ОВ по сравнению с D75 у людей с мКРРПЖ, ранее не проходивших химиотерапию. Кабазитаксел и доцетаксел продемонстрировали разные профили токсичности, а C20 продемонстрировал в целом самую низкую токсичность. [ 11 ] В исследовании фазы III с участием 755 мужчин по лечению резистентного к кастрации рака простаты медиана выживаемости составила 15,1 месяца для участников, получавших кабазитаксел, по сравнению с 12,7 месяца для участников, получавших митоксантрон . Кабазитаксел ассоциировался с большей нейтропенией 3–4 степени (81,7%), чем митоксантрон (58%). [ 12 ] К частым побочным эффектам кабазитаксела относятся нейтропения (в том числе фебрильная нейтропения), а побочные эффекты со стороны ЖКТ проявлялись главным образом в виде диареи, тогда как нейропатия выявлялась редко. [ 13 ]
Фармакокинетика
[ редактировать ]Введение кабазитаксела вызывает снижение концентрации в плазме, демонстрируя трехфазную кинетику: средний период полувыведения (t 1/2 ) составляет 2,6 мин в первой фазе, средний период t 1/2 составляет 1,3 часа во второй фазе и средний t 1/. 2 из 77,3 ч в третьей фазе. [ 14 ]
Метаболизм
[ редактировать ]Кабазитаксел метаболизируется в печени посредством [цитохрома P 450 (CYP)3A4/5 > CYP2C8], в результате чего образуется семь метаболитов плазмы и выводится 20 метаболитов. В течение 14 дней после приема 80% кабазитаксела выводится из организма: 76% с калом и 3,7% - с почками. [ 15 ]
Ссылки
[ редактировать ]- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»).» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ^ Jump up to: а б с «Комплект «Джевтана-кабазитаксел»» . ДейлиМед . Проверено 30 декабря 2021 г.
- ^ «Кабазитаксел» . Словарь лекарств NCI . Министерство здравоохранения и социальных служб США, Национальные институты здравоохранения, Национальный институт рака. 2 февраля 2011 г.
- ^ «Пакет одобрения лекарственного средства: Джевтана (Кабазитаксел) NDA № 201023» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 8 июля 2013 года . Проверено 30 декабря 2021 г.
- ^ «Джевтана (кабазитаксел) для инъекций одобрена FDA США после приоритетной проверки» (пресс-релиз). Санофи Авентис. 17 июня 2010 года . Получено 30 декабря 2021 г. - через PR Newswire.
- ^ «Джевтана (кабазитаксел) для инъекций одобрена FDA США после приоритетного рассмотрения – 17 июня 2010 г.» (пресс-релиз). Санофи. 17 июня 2010 года . Проверено 30 декабря 2021 г.
- ^ «Кабазитаксел: препараты, одобренные FDA» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . Проверено 30 декабря 2021 г.
- ^ «Первое одобрение непатентованного лекарственного средства» . Управление по контролю за продуктами и лекарствами США . 17 октября 2022 г. . Проверено 28 ноября 2022 г.
- ^ Джордан, Массачусетс, Уилсон Л. (апрель 2004 г.). «Микротрубочки как мишень для противораковых препаратов». Обзоры природы. Рак . 4 (4): 253–65. дои : 10.1038/nrc1317 . ПМИД 15057285 . S2CID 10228718 .
- ^ Даршан М.С., Лофтус М.С., Тадани-Мулеро М., Леви Б.П., Эскуин Д., Чжоу К.К. и др. (сентябрь 2011 г.). «Вызванная таксаном блокада ядерного накопления андрогенных рецепторов предсказывает клинические реакции при метастатическом раке простаты» . Исследования рака . 71 (18): 6019–29. дои : 10.1158/0008-5472.CAN-11-1417 . ПМЦ 3354631 . ПМИД 21799031 .
- ^ Удар С., Физази К., Сенгелёв Л., Даугард Г., Саад Ф., Хансен С. и др. (октябрь 2017 г.). «Кабазитаксел по сравнению с доцетакселом в качестве терапии первой линии для пациентов с метастатическим кастрационно-резистентным раком простаты: рандомизированное исследование III фазы-FIRSTANA». Журнал клинической онкологии . 35 (28): 3189–3197. дои : 10.1200/JCO.2016.72.1068 . ПМИД 28753384 .
- ^ «Кабазитаксел эффективен при гормонорефрактерном раке простаты после неэффективности таксотера» . [ постоянная мертвая ссылка ]
- ^ Паллер К.Дж., Антонаракис Э.С. (март 2011 г.). «Кабазитаксел: новый метод лечения второй линии метастатического рака простаты, резистентного к кастрации» . Дизайн, разработка и терапия лекарств . 5 : 117–24. дои : 10.2147/DDDT.S13029 . ПМК 3063116 . ПМИД 21448449 .
- ^ Мита А.С., Денис Л.Дж., Ровински Е.К., Дебоно Дж.С., Гетц А.Д., Очоа Л. и др. (январь 2009 г.). «Фаза I и фармакокинетическое исследование XRP6258 (RPR 116258A), нового таксана, вводимого в виде 1-часовой инфузии каждые 3 недели пациентам с распространенными солидными опухолями» . Клинические исследования рака . 15 (2): 723–30. дои : 10.1158/1078-0432.CCR-08-0596 . ПМИД 19147780 .
- ^ Цао К.К., Каттинг Э., Мартин Дж., О В.К. (июнь 2014 г.). «Роль кабазитаксела в лечении метастатического рака простаты, резистентного к кастрации» . Терапевтические достижения в урологии . 6 (3): 97–104. дои : 10.1177/1756287214528557 . ПМК 4003844 . ПМИД 24883107 .
Внешние ссылки
[ редактировать ]- «Кабазитаксел Аккорд 20 мг/мл, концентрат для инфузий раствора: риск ошибок при назначении препарата и путаницы с растворителем Джевтана (60 мг/1,5 мл) для инфузий» . Европейское агентство лекарственных средств (EMA) . 28 октября 2020 г.
- Номер клинического исследования NCT00417079 для «XRP6258 плюс преднизолон по сравнению с митоксантроном плюс преднизон при гормонорефрактерном метастатическом раке простаты (ТРОПИК)» на сайте ClinicalTrials.gov
- Номер клинического исследования NCT01308580 «Кабазитаксел в дозе 20 мг/м² по сравнению с дозой 25 мг/м² с преднизолоном для лечения метастатического рака простаты, резистентного к кастрации (PROSELICA)» на сайте ClinicalTrials.gov
- Номер клинического исследования NCT02485691 «Кабазитаксел в сравнении с переходом на альтернативный АР-таргетный агент (энзалутамид или абиратерон) у пациентов с метастатическим кастрационно-резистентным раком предстательной железы (мКРРПЖ), ранее получавших доцетаксел, и у которых предыдущий препарат, нацеленный на АР (CARD), быстро оказался неэффективным» на сайте ClinicalTrials.gov