Карбоплатин
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | / ˈ k ɑː r boʊ ˌ p l æ t n ə / |
| Торговые названия | Параплатин, другие |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а695017 |
| Маршруты администрация | внутривенный |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Биодоступность | полный |
| Связывание с белками | Очень низкий |
| Период полувыведения | 1,1-2 часа |
| Экскреция | Почка |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.050.388 |
| Химические и физические данные | |
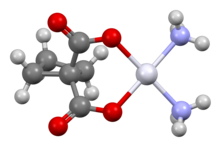
| Формула | С 6 Н 12 Н 2 О 4 Пт |
| Молярная масса | 371.256 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Карбоплатин под торговой маркой Параплатин , продаваемый , среди прочего, , представляет собой химиотерапевтический препарат, используемый для лечения ряда форм рака . [3] Сюда входят рак яичников , рак легких , рак головы и шеи , рак головного мозга и нейробластома . [3] Его применяют путем инъекции в вену . [3]
Обычно возникают побочные эффекты. [3] Общие побочные эффекты включают низкий уровень клеток крови , тошноту и проблемы с электролитами . [4] [3] Другие серьезные побочные эффекты включают аллергические реакции и мутагенез . Он может быть канцерогенным , но для подтверждения этого необходимы дальнейшие исследования. [3] Использование во время беременности может нанести вред ребенку. [3] Карбоплатин относится к на основе платины семейству противоопухолевых препаратов и действует путем вмешательства в дупликацию ДНК . [3] [5]
Карбоплатин был разработан как менее токсичный аналог цисплатина . [6] Он был запатентован в 1972 году и одобрен для медицинского использования в 1989 году. [7] Он включен в Список основных лекарственных средств Всемирной организации здравоохранения 2023 года . [8]
Медицинское использование
[ редактировать ]Карбоплатин используется для лечения ряда форм рака . Сюда входят рак яичников , рак легких , рак головы и шеи , рак головного мозга и нейробластома . Его можно использовать при некоторых типах рака яичек , но цисплатин , как правило, более эффективен. [3] Его также использовали для лечения тройного негативного рака молочной железы .
Побочные эффекты
[ редактировать ]По сравнению с цисплатином наибольшим преимуществом карбоплатина является уменьшение побочных эффектов, особенно устранение нефротоксических эффектов. Тошнота и рвота менее выражены и их легче контролировать. [9]
Основным недостатком карбоплатина является его миелосупрессивный эффект. Это приводит к тому, что выработка клеток крови и тромбоцитов костного мозга в организме резко снижается, иногда до 10% от обычного уровня производства. Надир этой миелосупрессии обычно наступает через 21–28 дней после первого лечения, после чего уровни клеток крови и тромбоцитов в крови начинают стабилизироваться, часто приближаясь к уровням прекарбоплатина. Это снижение количества лейкоцитов ( нейтропения ) может вызвать осложнения и иногда лечится такими препаратами, как филграстим . Наиболее заметным осложнением нейтропении является повышенная вероятность заражения условно-патогенными организмами, что требует повторной госпитализации и лечения антибиотиками .
Механизм действия
[ редактировать ]Карбоплатин отличается от цисплатина тем, что он содержит бидентатный вместо двух хлоридных лигандов дикарбоксилат (лиганд — циклобутандикарбоксилат, CBDCA) . Оба препарата являются алкилирующими агентами . CBDCA и хлорид являются уходящими группами в этих соответствующих препаратах. Карбоплатин демонстрирует более медленную аквавацию (замену CBDCA водой) и, следовательно, более медленную кинетику связывания ДНК, хотя он образует те же продукты реакции in vitro в эквивалентных дозах с цисплатином. В отличие от цисплатина, карбоплатин может быть восприимчив к альтернативным механизмам. Некоторые результаты показывают, что цисплатин и карбоплатин вызывают различные морфологические изменения в MCF-7, проявляя при этом свое цитотоксическое поведение. клеточных линиях [10] Сниженная реактивность ограничивает выведение белково-карбоплатиновых комплексов. Более низкая скорость выведения карбоплатина означает, что его большее количество удерживается в организме и, следовательно, его эффекты более продолжительны (период полувыведения карбоплатина составляет 30 часов по сравнению с 1,5-3,6 часами в случае цисплатина).
Как и цисплатин, карбоплатин связывается с ДНК и сшивает ее, препятствуя репликации и подавляя рост раковых клеток. [11] [12]
Доза
[ редактировать ]Для расчета дозы карбоплатина используется формула Калверта. Он учитывает клиренс креатинина и желаемую площадь под кривой . [13] Через 24 часа около 70% карбоплатина выводится с мочой в неизмененном виде. Это означает, что дозу карбоплатина необходимо корректировать в зависимости от любого нарушения функции почек . [14]
Формула Калверта:
Типичная площадь под кривой (AUC) для карбоплатина колеблется в пределах 3-7 (мг/мл)*мин. [14]
Синтез
[ редактировать ]Цисплатин реагирует с нитратом серебра , а затем с циклобутан-1,1-дикарбоновой кислотой с образованием карбоплатина. [15]

История
[ редактировать ]Карбоплатин, аналог цисплатина, был разработан компанией Bristol Myers Squibb и Институтом исследований рака с целью снижения токсичности цисплатина. [6] [16] США В марте 1989 года он получил одобрение Управления по контролю за продуктами и лекарствами (FDA) на карбоплатин под торговой маркой Параплатин. Начиная с октября 2004 года стали доступны генерические версии препарата.
Исследовать
[ редактировать ]Карбоплатин также использовался для адъювантной терапии 1 стадии семиноматозного рака яичка . Исследования показали, что для этого лечения оно не менее эффективно, чем адъювантная лучевая терапия , но имеет меньше побочных эффектов. [17] Это привело к тому, что в клинической практике адъювантная терапия на основе карбоплатина обычно предпочтительнее адъювантной лучевой терапии. [18]
Карбоплатин в сочетании с гексадецильной цепью и полиэтиленгликолем, по-видимому, обладает повышенной липорастворимостью и ПЭГилированием . Это полезно при химиотерапии , особенно при немелкоклеточном раке легких . [19]
Ссылки
[ редактировать ]- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»).» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ^ «Обновления о безопасности бренда в монографии о продукции» . Здоровье Канады . 7 июля 2016 года . Проверено 3 апреля 2024 г.
- ^ Перейти обратно: а б с д и ж г час я «Карбоплатин» . Американское общество фармацевтов системы здравоохранения. Архивировано из оригинала 21 декабря 2016 года . Проверено 8 декабря 2016 г.
- ^ Оун Р., Мусса Й.Е., Уит, штат Нью-Джерси (май 2018 г.). «Побочные эффекты химиотерапевтических препаратов на основе платины: обзор для химиков». Транзакции Далтона . 47 (19): 6645–6653. дои : 10.1039/c8dt00838h . ПМИД 29632935 .
- ^ Apps MG, Choi EH, Wheate NJ (август 2015 г.). «Состояние дел и будущее платиновых препаратов» . Эндокринный рак . 22 (4): Р219–Р233. дои : 10.1530/ERC-15-0237 . hdl : 2123/24426 . ПМИД 26113607 .
- ^ Перейти обратно: а б Лебволь Д., Канетта Р. (1998). «Клиническое развитие комплексов платины в терапии рака: историческая перспектива и обновленная информация» . Eur J Рак . 34 (10): 1522–34. дои : 10.1016/s0959-8049(98)00224-x . ПМИД 9893623 .
- ^ Фишер Дж., Ганеллин С.Р. (2006). Открытие аналоговых лекарств . Джон Уайли и сыновья. п. 513. ИСБН 9783527607495 . Архивировано из оригинала 20 декабря 2016 г.
- ^ Всемирная организация здравоохранения (2023 г.). Выбор и использование основных лекарств до 2023 г.: веб-приложение A: Типовой список основных лекарств Всемирной организации здравоохранения: 23-й список (2023 г.) . Женева: Всемирная организация здравоохранения. hdl : 10665/371090 . ВОЗ/MHP/HPS/EML/2023.02.
- ^ Гулбис А.М., Уоллис В.Д. (2023). «10 - Препаративные схемы, используемые при трансплантации гемопоэтических клеток и терапии Т-клетками с использованием химерных антигенных рецепторов». Руководство по трансплантации гемопоэтических клеток и клеточной терапии . Эльзевир. стр. 125–143. дои : 10.1016/B978-0-323-79833-4.00010-3 . ISBN 9780323798334 .
- ^ Натараджан Г., Малати Р., Холлер Э. (ноябрь 1999 г.). «Повышенная ДНК-связывающая активность цис-1,1-циклобутандикарбоксилатодиамминплатины (II) (карбоплатина) в присутствии нуклеофилов и цитоплазматических экстрактов клеток MCF-7 рака молочной железы человека: новый взгляд на теорию активации». Биохимическая фармакология . 58 (10): 1625–1629. дои : 10.1016/S0006-2952(99)00250-6 . ПМИД 10535754 .
- ^ Нолл Д.М., Мейсон Т.М., Миллер П.С. (февраль 2006 г.). «Образование и восстановление межнитевых связей в ДНК» . Химические обзоры . 106 (2): 277–301. дои : 10.1021/cr040478b . ПМК 2505341 . ПМИД 16464006 .
- ^ Эдельман М.Дж., Рупард Э.Дж. (2006). «ОПУХОЛИ ЗЛОКАЧЕСТВЕННЫЕ / Химиотерапевтические средства». Энциклопедия респираторной медицины . Академическая пресса. стр. 332–338. дои : 10.1016/B0-12-370879-6/00409-9 . ISBN 9780123708793 .
- ^ О'Сирбхейл Р., Саббатини П.С. (1 сентября 2012 г.). «Новые рекомендации по дозированию карбоплатина» . Мемориальный онкологический центр Слоана-Кеттеринга. Архивировано из оригинала 31 октября 2014 г. Проверено 27 марта 2014 г.
- ^ Перейти обратно: а б Калверт А.Х., Ньюэлл Д.Р., Гамбрелл Л.А., О'Рейли С., Бернелл М., Боксалл Ф.Е. и др. (ноябрь 1989 г.). «Дозировка карбоплатина: проспективная оценка простой формулы, основанной на функции почек». Журнал клинической онкологии . 7 (11): 1748–1756. дои : 10.1200/JCO.1989.7.11.1748 . ПМИД 2681557 .
- ^ Варданян Р.С., Грубий В.Ю. (2006). «30 – Противоопухолевые средства». Синтез основных лекарственных средств . Эльзевир. стр. 389–418. дои : 10.1016/B978-044452166-8/50030-3 . ISBN 9780444521668 .
- ^ «Открытие ранних химиотерапевтических препаратов» . Институт исследования рака . Проверено 6 октября 2023 г.
- ^ Оливер Р.Т., Мейсон М.Д., Мид Г.М., фон дер Маасе Х., Растин Г.Дж., Джоффе Дж.К. и др. (2005). «Лучевая терапия по сравнению с однократным приемом карбоплатина в адъювантном лечении семиномы I стадии: рандомизированное исследование» . Ланцет . 366 (9482): 293–300. дои : 10.1016/S0140-6736(05)66984-X . ПМИД 16039331 . S2CID 6001898 .
- ^ Тонер GC (май 2015 г.). «Рак яичка: оптимальное лечение семиномы I стадии в 2015 году». Обзоры природы. Урология . 12 (5): 249–251. дои : 10.1038/nrurol.2015.85 . ПМИД 25896179 . S2CID 8072355 .
- ^ Ланг Т, Ли Н, Чжан Дж, Ли Ю, Ронг Р, Фу Ю (декабрь 2021 г.). «Стратегия нанодоставки на основе пролекарств для улучшения противоопухолевой способности карбоплатина in vivo и in vitro » . Доставка лекарств . 28 (1): 1272–1280. дои : 10.1080/10717544.2021.1938754 . ПМК 8238065 . ПМИД 34176381 .
Дальнейшее чтение
[ редактировать ]- Канетта Р., Розенцвейг М., Картер С.К. (сентябрь 1985 г.). «Карбоплатин: клинический спектр на сегодняшний день». Обзоры лечения рака . 12 Приложение А (Приложение А): 125–136. дои : 10.1016/0305-7372(85)90027-1 . ПМИД 3002623 .
- Ян XL, Ван А.Х. (сентябрь 1999 г.). «Структурные исследования атомоспецифических противораковых препаратов, действующих на ДНК». Фармакология и терапия . 83 (3): 181–215. дои : 10.1016/S0163-7258(99)00020-0 . ПМИД 10576292 .
