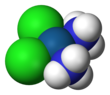
Цисплатин
 | |||
| |||
| Клинические данные | |||
|---|---|---|---|
| Торговые названия | Платинол, другие | ||
| Другие имена | Цисплатин, платамин, неоплатин, цисмаплат, цис -диамминдихлорплатина(II) (CDDP) | ||
| AHFS / Drugs.com | Монография | ||
| Медлайн Плюс | а684036 | ||
| Данные лицензии | |||
| Беременность категория | |||
| Маршруты администрация | внутривенный | ||
| код АТС | |||
| Юридический статус | |||
| Юридический статус |
| ||
| Фармакокинетические данные | |||
| Биодоступность | 100% (IV) | ||
| Связывание с белками | > 95% | ||
| Период полувыведения | 30–100 часов | ||
| Экскреция | Реналь | ||
| Идентификаторы | |||
| Номер CAS | |||
| ПабХим CID | |||
| Лекарственный Банк | |||
| ХимическийПаук | |||
| НЕКОТОРЫЙ | |||
| КЕГГ | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| PDB-лиганд | |||
| Панель управления CompTox ( EPA ) | |||
| Информационная карта ECHA | 100.036.106 | ||
| Химические и физические данные | |||
| Формула | [Pt(NH 3 ) 2 Cl 2 ] | ||
| Молярная масса | 300.05 g·mol −1 | ||
| 3D model ( JSmol ) | |||
| | |||
Цисплатин представляет собой химическое соединение формулой цис- с [Pt(NH 3 ) 2 Cl 2 ] . Это координационный комплекс платины , который используется в качестве химиотерапевтического препарата для лечения ряда видов рака . [3] К ним относятся рак яичек , рак яичников , рак шейки матки , рак мочевого пузыря , рак головы и шеи , рак пищевода , рак легких , мезотелиома , опухоли головного мозга и нейробластома . [3] Его вводят путем инъекции в вену . [3]
Общие побочные эффекты включают подавление функции костного мозга , проблемы со слухом, включая тяжелую потерю слуха, повреждение почек и рвоту . [3] [4] [5] Другие серьезные побочные эффекты включают онемение, проблемы с ходьбой, аллергические реакции , проблемы с электролитом и болезни сердца . [3] Использование во время беременности может нанести вред развивающемуся плоду. [1] [3] Цисплатин относится к на основе платины . семейству противоопухолевых препаратов [3] Частично он действует путем связывания с ДНК и ингибирования ее репликации . [3]
Цисплатин был открыт в 1845 году и лицензирован для медицинского применения в 1978 и 1979 годах. [6] [3] Он входит в Список основных лекарственных средств Всемирной организации здравоохранения . [7] [8]
Медицинское использование
Цисплатин вводят внутривенно в виде кратковременной инфузии в физиологическом растворе для лечения солидных и гематологических злокачественных опухолей. Он используется для лечения различных типов рака, включая саркомы , некоторые карциномы (например, мелкоклеточный рак легкого , плоскоклеточный рак головы и шеи и рак яичников ), лимфомы , рак мочевого пузыря , рак шейки матки , [9] и герминогенные опухоли .
Внедрение цисплатина в качестве стандартного лечения рака яичка улучшило показатели ремиссии с 5-10% до 1974 года до 75-85% к 1984 году. [10]
Побочные эффекты [ править ]
Цисплатин имеет ряд побочных эффектов, которые могут ограничивать его применение:
- Нефротоксичность (поражение почек) является основным побочным эффектом, ограничивающим дозу, и представляет собой серьезную клиническую проблему. Цисплатин избирательно накапливается в проксимальных канальцах посредством базолатерального транспорта к апикальному, где он нарушает энергетику митохондрий и эндоплазматический ретикулум . 2+ гомеостаза и стимулирует активные формы кислорода и провоспалительные цитокины . [11] Клинически и доклинически изучаются многочисленные стратегии смягчения последствий, включая режимы гидратации, амифостин , ингибиторы транспортеров, антиоксиданты, противовоспалительные средства, а также эпоксиэйкозатриеновые кислоты и их аналоги. [11] [12]
- Нейротоксичность (повреждение нервов) можно предвидеть, проводя исследования нервной проводимости до и после лечения. Общие неврологические побочные эффекты цисплатина включают нарушения зрительного восприятия и слуха, которые могут возникнуть вскоре после начала лечения. [13] Хотя запуск апоптоза посредством вмешательства в репликацию ДНК остается основным механизмом действия цисплатина, не было обнаружено, что он способствует неврологическим побочным эффектам. Недавние исследования показали, что цисплатин неконкурентно ингибирует архетипический мембраносвязанный механочувствительный переносчик ионов натрия и водорода, известный как NHE-1 . [13] В первую очередь он обнаруживается в клетках периферической нервной системы, которые в больших количествах агрегируются вблизи глазных и слуховых центров восприятия стимулов. Это неконкурентное взаимодействие связано с гидроэлектролитическим дисбалансом и изменениями цитоскелета, оба из которых были подтверждены in vitro и in vivo. Однако было обнаружено, что ингибирование NHE-1 является как дозозависимым (половинное ингибирование = 30 мкг/мл), так и обратимым. [13] Цисплатин может повышать уровень сфингозин-1-фосфата в центральной нервной системе , способствуя развитию когнитивных нарушений после химиотерапии . [14] [15]
- Тошнота и рвота : цисплатин является одним из наиболее рвотных химиопрепаратов, но этот симптом купируется профилактическими противорвотными средствами ( ондансетрон , гранисетрон и др.) в сочетании с кортикостероидами . Было показано, что апрепитант в сочетании с ондансетроном и дексаметазоном лучше подходит для высокоэметогенной химиотерапии, чем просто ондансетрон и дексаметазон .
- Ототоксичность и потеря слуха, связанные с применением цисплатина, могут быть серьезными и считаются побочным эффектом, ограничивающим дозу. [5] Для оценки тяжести ототоксичности может потребоваться аудиометрический анализ. Другие препараты (например, антибиотики класса аминогликозидов ) также могут вызывать ототоксичность, поэтому назначения антибиотиков этого класса пациентам, получающим цисплатин, обычно избегают. Ототоксичность как аминогликозидов, так и цисплатина может быть связана с их способностью связываться с меланином в сосудистой полоске внутреннего уха или с генерацией активных форм кислорода . США В сентябре 2022 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило тиосульфат натрия под торговой маркой Pedmark для снижения риска ототоксичности и потери слуха у людей, получающих цисплатин. [16] [17] [18] Продолжается исследование использования инъекций ацетилцистеина в качестве профилактической меры. [5] [19]
- Электролитные нарушения : Цисплатин может вызвать гипомагниемию, гипокалиемию и гипокальциемию. Гипокальциемия, по-видимому, возникает у пациентов с низким уровнем магния в сыворотке крови, вторичным по отношению к цисплатину, поэтому она не связана в первую очередь с цисплатином.
- Гемолитическая анемия может развиться после нескольких курсов приема цисплатина. ответственны антитела, реагирующие с мембраной цисплатин-эритроцитов Предполагается, что за гемолиз . [20]
Фармакология [ править ]
Цисплатин препятствует репликации ДНК, что убивает самые быстропролиферирующие клетки, которые теоретически являются раковыми. После введения один ион хлорида медленно вытесняется водой с образованием аквакомплекса цис- [PtCl(NH 3 ) 2 (H 2 O)] + , в процессе, называемом аквацией . Диссоциация хлорида внутри клетки благоприятствует, поскольку внутриклеточная концентрация хлорида составляет всего 3–20% от концентрации хлорида примерно 100 мМ во внеклеточной жидкости. [21] [22]
Молекула воды в цис- [PtCl(NH 3 ) 2 (H 2 O)] + сам по себе легко замещается N - гетероциклическими ДНК основаниями . Гуанин преимущественно связывается. Получено модельное соединение и исследованы кристаллы методом рентгеновской кристаллографии. [23]
После образования [PtCl(гуанин-ДНК)(NH 3 ) 2 ] + сшивание может происходить за счет замещения другого хлорида, обычно другим гуанином. [24] Цисплатин сшивает ДНК несколькими различными способами, препятствуя делению клеток путем митоза . Поврежденная ДНК запускает механизмы репарации ДНК , которые, в свою очередь, активируют апоптоз , когда восстановление оказывается невозможным. В 2008 году исследователям удалось показать, что апоптоз, индуцированный цисплатином в клетках рака толстой кишки человека, зависит от митохондриальной сериновой протеазы Omi/Htra2 . [25] Поскольку это было продемонстрировано только для клеток карциномы толстой кишки, остается открытым вопрос, участвует ли белок Omi/Htra2 в индуцированном цисплатином апоптозе в карциномах из других тканей. [25]
Наиболее заметными среди изменений в ДНК являются 1,2-внутрицепочечные поперечные связи с пуриновыми основаниями. К ним относятся 1,2-внутрицепочечные аддукты d( Gp G), которые образуют почти 90% аддуктов, и менее распространенные 1,2-внутрицепочечные аддукты d( Ap G). Химики-координаторы получили кристаллы продуктов реакции цисплена с небольшими моделями ДНК. Вот график POVray связывания платины с небольшой моделью ДНК. [26]

Встречаются 1,3-внутрицепочечные аддукты d(GpXpG), но они легко удаляются путем нуклеотидов эксцизионной репарации ( NER ). Другие аддукты включают межцепочечные поперечные связи и нефункциональные аддукты, которые, как предполагается, способствуют активности цисплатина. Взаимодействие с клеточными белками, особенно с белками домена HMG , также рассматривается как механизм вмешательства в митоз, хотя, вероятно, это не основной метод его действия. [27]
Резистентность цисплатину к
Комбинированная химиотерапия цисплатином является краеугольным камнем лечения многих видов рака. Начальная чувствительность к платине высока, но у большинства онкологических больных в конечном итоге возникает рецидив с развитием цисплатин-резистентного заболевания. Было предложено множество механизмов резистентности к цисплатину, включая изменения клеточного поглощения и оттока препарата, усиление детоксикации препарата, ингибирование апоптоза , усиление репарации ДНК или изменения метаболизма. [28] [29] В лабораторных условиях оксалиплатин активен в отношении раковых клеток с высокой резистентностью к цисплатину; однако имеется мало доказательств его активности при клиническом лечении пациентов с цисплатин-резистентным раком. [29] Препарат паклитаксел может быть полезен при лечении рака, устойчивого к цисплатину; механизм этой активности пока неизвестен. [30]
Трансплатин [ править ]
Трансплатин , транс -стереоизомер цисплатина, имеет формулу транс- [PtCl 2 (NH 3 ) 2 ] и не проявляет сравнительно полезного фармакологического эффекта. Было предложено два механизма, объясняющих снижение противоракового эффекта трансплатина. Во-первых, считается, что транс- расположение хлор-лигандов придает трансплатину большую химическую реакционную способность, вызывая дезактивацию трансплатина до того, как он достигнет ДНК, где цисплатин проявляет свое фармакологическое действие. Во-вторых, стереоконформация трансплатина такова, что он не способен образовывать характерные 1,2-внутрицепочечные аддукты d(GpG), образуемые в большом количестве цисплатином. [31]
Молекулярная структура [ править ]
Цисплатин представляет собой плоский координационный комплекс цис-[Pt(NH 3 ) 2 Cl 2 ]. [32] : 286–8 [33] : 689 Приставка цис указывает на цис- изомер , в котором два одинаковых лиганда находятся в соседних положениях. [32] [33] : 550 Систематическое химическое название этой молекулы — цис -диамминдихлорплатина, [32] : 286 где аммин с двумя m указывает на аммиачный (NH 3 ) лиганд , в отличие от органического амина с одним m. [32] : 284
История [ править ]
Соединение цис- [Pt(NH 3 ) 2 Cl 2 ] было впервые описано итальянским химиком Мишелем Пейроном в 1845 году и долгое время было известно как соль Пейрона. [34] [35] Структура была выведена Альфредом Вернером в 1893 году. [24] В 1965 году Барнетт Розенберг , Ван Кэмп и др. из Мичиганского государственного университета обнаружили, что электролиз платиновых электродов генерирует растворимый комплекс платины, который ингибирует бинарное деление в бактериях Escherichia coli ( E. coli ). Хотя рост бактериальных клеток продолжался, деление клеток было остановлено, бактерии разрастались в виде нитей, длина которых в 300 раз превышала их нормальную длину. [36] Было обнаружено, что октаэдрический комплекс Pt(IV) цис- [PtCl 4 (NH 3 ) 2 ], но не транс -изомер, эффективен в стимулировании нитевидного роста клеток E. coli . Плоский квадратный комплекс Pt(II) цис- [PtCl 2 (NH 3 ) 2 ] оказался еще более эффективным в стимулировании нитевидного роста. [37] [38] Это открытие привело к наблюдению, что цис- [PtCl 2 (NH 3 ) 2 ] действительно очень эффективен в снижении массы сарком у крыс . [39] Подтверждение этого открытия и распространение испытаний на другие линии опухолевых клеток положили начало медицинскому применению цисплатина. Цисплатин был одобрен Управлением по контролю за продуктами и лекарствами США для применения при раке яичек и яичников 19 декабря 1978 года. [24] [40] [41] и в Великобритании (и в ряде других европейских стран) в 1979 году. [42] Цисплатин был разработан первым. [43] В 1983 году детский онколог Роджер Пакер начал включать цисплатин в адъювантную химиотерапию для лечения детской медуллобластомы . [44] Новый протокол, который он разработал, привел к заметному увеличению безрецидивной выживаемости пациентов с медуллобластомой примерно до 85%. [45] Протокол Пакера с тех пор стал стандартным методом лечения медуллобластомы. Аналогичным образом, было обнаружено, что цисплатин особенно эффективен против рака яичек , где его использование улучшило уровень излечения с 10% до 85%. [10]
Недавно некоторые исследователи исследовали на доклиническом уровне новые формы пролекарств цисплатина в сочетании с наноматериалами с целью локализации высвобождения препарата в мишени. [46] [47]
Синтез [ править ]
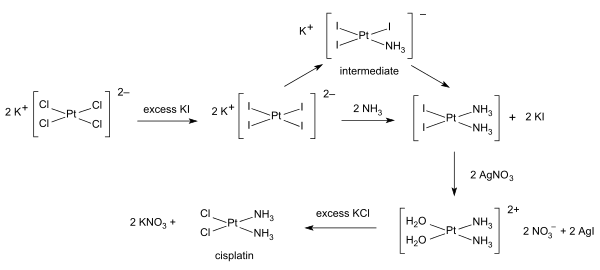
Синтез цисплатина начинается с тетрахлорплатината калия . Доступно несколько процедур. Одним из препятствий является легкое образование зеленой соли Магнуса (MGS), которая имеет ту же эмпирическую формулу, что и цисплатин. Традиционный способ избежать MGS включает преобразование K 2 PtCl 4 в K 2 PtI 4 , как первоначально описано Дхарой. [48] [49] Реакция с аммиаком приводит к образованию PtI 2 (NH 3 ) 2 , который выделяют в виде соединения желтого цвета. При нитрата серебра добавлении в воду нерастворимый йодид серебра выпадает в осадок, а [Pt(OH 2 ) 2 (NH 3 ) 2 ](NO 3 ) 2 остается в растворе. При добавлении хлорида калия образуется конечный продукт, который выпадает в осадок. [49] В трииодном промежуточном соединении присоединение второго аммиачного лиганда определяется транс-эффектом . [49]
однореакторный синтез цисплатина из K 2 PtCl 4 Разработан . Он основан на медленном высвобождении аммиака из ацетата аммония. [50]
Исследования [ править ]
Цисплатин изучался вместе с Оже-терапией с целью усиления терапевтического эффекта цисплатина без увеличения токсичности для нормальных тканей. [51] Однако из-за значительных побочных эффектов поиск структурно новых соединений Pt(II) и Pd(II), проявляющих противоопухолевую активность, чрезвычайно важен и направлен на разработку более эффективных и менее токсичных препаратов. [52] Металлокомплексы, содержащие цисплатиноподобные молекулы ([PtCl(NH 3 ) 2 ] или [Pt(NH 3 )Cl 2 ]), связанные алкандиаминовыми цепями переменной длины, в последние несколько лет вызвали большой интерес в качестве альтернативных лекарств нового поколения для лечения рака. химиотерапия. [53] [54] [55]
Ссылки [ править ]
- ↑ Перейти обратно: Перейти обратно: а б с д «Использование цисплатина во время беременности» . Наркотики.com . 12 сентября 2019 года . Проверено 25 февраля 2020 г.
- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»).» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ↑ Перейти обратно: Перейти обратно: а б с д и ж г час я «Цисплатин» . Американское общество фармацевтов системы здравоохранения. Архивировано из оригинала 21 декабря 2016 года . Проверено 8 декабря 2016 г.
- ^ Оун Р., Мусса Й.Е., Уит, штат Нью-Джерси (май 2018 г.). «Побочные эффекты химиотерапевтических препаратов на основе платины: обзор для химиков». Транзакции Далтона . 47 (19): 6645–6653. дои : 10.1039/c8dt00838h . ПМИД 29632935 .
- ↑ Перейти обратно: Перейти обратно: а б с Кальехо А., Седо-Кабесон Л., Хуан И.Д., Льоренс Х. (июль 2015 г.). «Ототоксичность, вызванная цисплатином: эффекты, механизмы и стратегии защиты» . Токсики . 3 (3): 268–293. дои : 10.3390/токсики3030268 . ПМК 5606684 . ПМИД 29051464 .
- ^ Фишер Дж., Ганеллин С.Р. (2006). Открытие аналоговых лекарств . Джон Уайли и сыновья. п. 513. ИСБН 9783527607495 . Архивировано из оригинала 20 декабря 2016 года.
- ^ Всемирная организация здравоохранения (2019). Модельный список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г. Женева: Всемирная организация здравоохранения. hdl : 10665/325771 . ВОЗ/MVP/EMP/IAU/2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ Всемирная организация здравоохранения (2021 г.). Примерный список основных лекарственных средств Всемирной организации здравоохранения: 22-й список (2021 г.) . Женева: Всемирная организация здравоохранения. hdl : 10665/345533 . ВОЗ/MHP/HPS/EML/2021.02.
- ^ «Цисплатин» . Национальный институт рака . 2 марта 2007 г. Архивировано из оригинала 8 октября 2014 г. . Проверено 13 ноября 2014 г.
- ↑ Перейти обратно: Перейти обратно: а б Эйнхорн Л.Х. (ноябрь 1990 г.). «Лечение рака яичек: новая и улучшенная модель». Журнал клинической онкологии . 8 (11): 1777–81. дои : 10.1200/JCO.1990.8.11.1777 . ПМИД 1700077 .
- ↑ Перейти обратно: Перейти обратно: а б Миллер Р.П., Тадагавади Р.К., Рамеш Г., Ривз В.Б. (октябрь 2010 г.). «Механизмы нефротоксичности цисплатина» . Токсины . 2 (11): 2490–2518. дои : 10.3390/toxins2112490 . ПМЦ 3153174 . ПМИД 22069563 .
- ^ Сингх Н., Вик А., Либранд Д.Б., Мориссо С., Гамак Б.Д. (ноябрь 2021 г.). «Новые алкокси-аналоги эпоксиэйкозатриеновых кислот ослабляют нефротоксичность цисплатина in vitro посредством уменьшения митохондриальной дисфункции, окислительного стресса, митоген-активируемой передачи сигналов протеинкиназы и активации каспаз» . Химические исследования в токсикологии . 34 (12): 2579–2591. doi : 10.1021/acs.chemrestox.1c00347 . ПМЦ 8853703 . ПМИД 34817988 .
- ↑ Перейти обратно: Перейти обратно: а б с Милосавлевич Н., Дюрантон С., Джерби Н., Пуэх П.Х., Гунон П., Лагадич-Госсманн Д. и др. (октябрь 2010 г.). «Негеномные эффекты цисплатина: острое ингибирование механочувствительных транспортеров и каналов без ремоделирования актина» . Исследования рака . 70 (19): 7514–22. дои : 10.1158/0008-5472.CAN-10-1253 . ПМИД 20841472 .
- ^ Сквиллаче С., Нихофф М.Л., Дойл Т.М., Грин М., Эспозито Е., Кузокреа С., Арнатт С.К., Шпигель С., Фарр С.А., Сальвемини Д. (сентябрь 2022 г.). «Активация рецептора сфингозин-1-фосфата 1 в центральной нервной системе приводит к когнитивным нарушениям, вызванным цисплатином» . Журнал клинических исследований . 132 (17). дои : 10.1172/JCI157738 . ПМЦ 9433103 . ПМИД 36047496 .
- ^ «Разгадка тайны «химического мозга» » . Новости неврологии . 2 сентября 2022 г.
- ^ Оргель Э., Вильялуна Д., Крайло М.Д., Эсбеншаде А., Сунг Л., Фрейер Д.Р. (май 2022 г.). «Тиосульфат натрия для предотвращения потери слуха, вызванной цисплатином: обновленная информация о выживаемости по данным ACCL0431» . «Ланцет». Онкология . 23 (5): 570–572. дои : 10.1016/S1470-2045(22)00155-3 . ПМЦ 9635495 . ПМИД 35489339 .
- ^ Уинстед Э. (6 октября 2022 г.). «Тиосульфат натрия снижает потерю слуха у детей, больных раком» . Национальный институт рака . Проверено 9 марта 2023 г.
- ^ «FDA одобрило тиосульфат натрия для снижения риска ототоксичности, связанной с цисплатином, у педиатрических пациентов с локализованными неметастатическими солидными опухолями» . Управление по контролю за продуктами и лекарствами. 20 сентября 2022 г. Проверено 9 марта 2023 г.
- ^ Сарафраз З., Ахмади А., Данеши А. (июнь 2018 г.). «Транстимпанические инъекции N-ацетилцистеина и дексаметазона для профилактики ототоксичности, вызванной цисплатином: двойное слепое рандомизированное клиническое исследование». Международный журнал по тиннитусу . 22 (1): 40–45. дои : 10.5935/0946-5448.20180007 . ПМИД 29993216 .
- ^ Леви Дж. А., Арони Р. С., Дэлли Д. Н. (июнь 1981 г.). «Гемолитическая анемия после лечения цисплатином» . Британский медицинский журнал . 282 (6281): 2003–4. дои : 10.1136/bmj.282.6281.2003 . ПМК 1505958 . ПМИД 6788166 .
- ^ Ван Д., Липпард С.Дж. (апрель 2005 г.). «Клеточная переработка платиновых противораковых препаратов». Обзоры природы. Открытие наркотиков . 4 (4): 307–320. дои : 10.1038/nrd1691 . ПМИД 15789122 . S2CID 31357727 .
- ^ Джонстон Т.К., Сунтаралингам К., Липпард С.Дж. (март 2016 г.). «Следующее поколение платиновых препаратов: таргетные агенты Pt(II), доставка наночастиц и пролекарства Pt(IV)» . Химические обзоры . 116 (5): 3436–3486. doi : 10.1021/acs.chemrev.5b00597 . ПМЦ 4792284 . ПМИД 26865551 .
- ^ Орбелл Дж.Д., Солорцано С., Марзилли Л.Г., Кистенмахер Т.Дж. (октябрь 1982 г.). «Получение и структура цис-хлордиаммин (N2, N2-диметил-9-метилгуанин) гексафторфосфата платины (II). Модель промежуточного соединения в предлагаемом сшивающем механизме действия противоопухолевых средств платины (II)». Неорганическая химия . 21 (10): 3806–3810. дои : 10.1021/ic00140a041 .
- ↑ Перейти обратно: Перейти обратно: а б с Тшаска С (20 июня 2005 г.). «Цисплатин» . Новости химии и техники . 83 (25): 52. doi : 10.1021/cen-v083n025.p052 .
- ↑ Перейти обратно: Перейти обратно: а б Прюфер Ф.Г., Лизаррага Ф., Мальдонадо В., Мелендес-Зайгла Дж. (июнь 2008 г.). «Участие активности сериновой протеазы Omi Htra2 в апоптозе, индуцированном цисплатином на клетках рака толстой кишки SW480». Журнал химиотерапии . 20 (3): 348–354. дои : 10.1179/joc.2008.20.3.348 . ПМИД 18606591 . S2CID 11052459 .
- ^ Шерман С.Е., Гибсон Д., Ван А.Х., Липпард С.Дж. (октябрь 1985 г.). «Рентгеновская структура основного аддукта противоракового препарата цисплатина с ДНК: цис-[Pt(NH3)2(d(pGpG))]». Наука . 230 (4724): 412–7. Бибкод : 1985Sci...230..412S . дои : 10.1126/science.4048939 . ПМИД 4048939 .
- ^ Ху Дж., Либ Дж.Д., Санкар А., Адар С. (октябрь 2016 г.). «Карты повреждения и восстановления ДНК цисплатина генома человека с разрешением в один нуклеотид» . ПНАС . 113 (41): 11507–11512. Бибкод : 2016PNAS..11311507H . дои : 10.1073/pnas.1614430113 . ПМК 5068337 . ПМИД 27688757 . S2CID 11052459 .
- ^ Крус-Бермудес А., Ласа-Бривьеска Р., Висенте-Бланко Р.Х., Гарсиа-Гранде А., Коронадо М.Дж., Лайне-Менендес С. и др. (май 2019 г.). «Устойчивость к цисплатину включает метаболическое перепрограммирование посредством АФК и PGC-1α при НМРЛ, которое можно преодолеть путем ингибирования OXPHOS». Свободно-радикальная биология и медицина . 135 : 167–181. doi : 10.1016/j.freeradbiomed.2019.03.009 . hdl : 10486/688357 . ПМИД 30880247 .
- ↑ Перейти обратно: Перейти обратно: а б Стордал Б., Дэйви М. (ноябрь 2007 г.). «Понимание устойчивости к цисплатину с использованием клеточных моделей» (PDF) . ИУБМБ Жизнь . 59 (11): 696–699. дои : 10.1080/15216540701636287 . ПМИД 17885832 . S2CID 30879019 .
- ^ Стордал Б., Павлакис Н., Дэйви Р. (декабрь 2007 г.). «Систематический обзор устойчивости к платине и таксанам от лабораторного исследования до клиники: обратная зависимость» (PDF) . Обзоры лечения рака . 33 (8): 688–703. дои : 10.1016/j.ctrv.2007.07.013 . hdl : 2123/4068 . ПМИД 17881133 .
- ^ Колучча М., Натиле Дж. (январь 2007 г.). «Трансплатиновые комплексы в терапии рака». Противораковые агенты в медицинской химии . 7 (1): 111–123. дои : 10.2174/187152007779314080 . ПМИД 17266508 .
- ↑ Перейти обратно: Перейти обратно: а б с д Мисслер Г.Л., Тарр Д.А. (1999). Неорганическая химия (2-е изд.). Прентис Холл. ISBN 978-0-13-841891-5 .
- ↑ Перейти обратно: Перейти обратно: а б Housecroft CE, Sharpe AG (2005). Неорганическая химия (2-е изд.). Пирсон Прентис Холл. ISBN 978-0-130-39913-7 .
- ^ Кауфман ГБ, Пентималли Р., Холл, доктор медицины (2010). «Мишель Пейрон (1813–1883), первооткрыватель цисплатина» . Обзор платиновых металлов . 54 (4): 250–256. дои : 10.1595/147106710X534326 . Проверено 3 октября 2022 г.
Цель этой биографической статьи — впервые на английском языке представить краткий обзор его жизни и достижений, которых он добился за свою научную карьеру.
- ^ Пейрон М (1844 г.). «О действии аммиака на хлорид платины» . Энн. Хим . 51 (1): 1–29. дои : 10.1002/jlac.18440510102 .
- ^ Розенберг Б., Ванкамп Л., Кригас Т. (февраль 1965 г.). «Ингибирование деления клеток Escherichia coli продуктами электролиза платинового электрода». Природа . 205 (4972): 698–9. Бибкод : 1965Natur.205..698R . дои : 10.1038/205698a0 . ПМИД 14287410 . S2CID 9543916 .
- ^ Розенберг Б., Ван Кэмп Л., Гримли Э.Б., Томсон А.Дж. (март 1967 г.). «Ингибирование роста или деления клеток Escherichia coli различными ионными видами комплексов платины (IV)» . Журнал биологической химии . 242 (6): 1347–52. дои : 10.1016/S0021-9258(18)96186-7 . ПМИД 5337590 .
- ^ Кристи Д.А., Тэнси Э.М. (2007). Кристи Д.А., Тэнси Э.М., Томсон А.Дж. (ред.). Открытие, использование и влияние солей платины в качестве химиотерапевтического средства при раке . Добро пожаловать, свидетели медицины двадцатого века. Том. 30. стр. 6–15. ISBN 978-0-85484-112-7 .
- ^ Розенберг Б., ВанКэмп Л., Троско Дж.Э., Мансур В.Х. (апрель 1969 г.). «Соединения платины: новый класс мощных противоопухолевых средств». Природа . 222 (5191): 385–6. Бибкод : 1969Natur.222..385R . дои : 10.1038/222385a0 . ПМИД 5782119 . S2CID 32398470 .
- ^ Карпентер Д.П. (2010). Репутация и власть: организационный имидж и фармацевтическое регулирование в FDA . Принстон, Нью-Джерси: Издательство Принстонского университета. ISBN 978-0-691-14180-0 .
- ^ «Краткая информация об одобрении цисплатина при метастатических опухолях яичников» . Инструменты FDA для онкологии . Управление по контролю за продуктами и лекарствами , Центр оценки и исследования лекарств. 19 декабря 1978 года. Архивировано из оригинала 8 февраля 2008 года . Проверено 15 июля 2009 г.
- ^ Уилтшоу Э (1979). «Цисплатин в лечении рака». Обзор платиновых металлов . 23 (3): 90–8. дои : 10.1595/003214079X2339098 . S2CID 267470502 .
- ^ Келланд Л. (2007). «Возрождение химиотерапии рака на основе платины». Обзоры природы Рак . 7 (8): 573–584. дои : 10.1038/nrc2167 . ПМИД 17625587 . S2CID 205468214 .
- ^ Пакер Р.Дж., Саттон Л.Н., Элтерман Р., Ланге Б., Голдвейн Дж., Николсон Х.С. и др. (ноябрь 1994 г.). «Результат лечения детей с медуллобластомой с помощью лучевой терапии, цисплатина, CCNU и химиотерапии винкристином». Журнал нейрохирургии . 81 (5): 690–8. дои : 10.3171/jns.1994.81.5.0690 . ПМИД 7931615 .
- ^ Пакер Р.Дж., Саттон Л.Н., Голдвейн Дж.В., Перилонго Г., Бунин Г., Райан Дж. и др. (март 1991 г.). «Улучшение выживаемости при использовании адъювантной химиотерапии при лечении медуллобластомы». Журнал нейрохирургии . 74 (3): 433–40. дои : 10.3171/jns.1991.74.3.0433 . ПМИД 1847194 .
- ^ Дхар С., Дэниел В.Л., Гильоханн Д.А., Миркин К.А., Липпард С.Дж. (октябрь 2009 г.). «Конъюгаты поливалентных олигонуклеотидов с наночастицами золота как средства доставки боеголовок из платины (IV)» . Журнал Американского химического общества . 131 (41): 14652–3. дои : 10.1021/ja9071282 . ПМК 2761975 . ПМИД 19778015 .
- ^ Санти М., Мапанао А.К., Кассано Д., Вламидис Ю., Каппелло В., Волиани В. (апрель 2020 г.). «Эндогенно-активированная ультрамалая нанотерапия: оценка трехмерного плоскоклеточного рака головы и шеи» . Раки . 12 (5): 1063. doi : 10.3390/cancers12051063 . ПМЦ 7281743 . ПМИД 32344838 .
- ^ Дхара СК (1970). «Цисплатин». Индиан Дж. Хим . 8 : 123–134.
- ↑ Перейти обратно: Перейти обратно: а б с Олдерден Р.А., Холл, доктор медицинских наук, Хэмбли Т.В. (2006). «Открытие и разработка цисплатина». Дж. Хим. Образование. 83 (5): 728. Бибкод : 2006ЖЧЭд..83..728А . дои : 10.1021/ed083p728 . S2CID 29546931 .
- ^ Кукушикин В.Ю., Оскарссон О., Элдинг Л.И., Фаррелл Н. (2007). «Легкий синтез изомерно чистого цис -дихлордиамминплатины (II), цисплатина ». Простой синтез изомерно чистого цис-дихлордиамминплатины(II), цисплатина . Неорганические синтезы. Том. 32. С. 141–144. дои : 10.1002/9780470132630.ch23 . ISBN 9780470132630 .
- ^ Ку А, Факка В.Дж., Кай З., Рейли Р.М. (октябрь 2019 г.). «Оже-электроны для терапии рака – обзор» . EJNMMI Радиофармация и химия . 4 (1): 27. дои : 10.1186/s41181-019-0075-2 . ПМК 6800417 . ПМИД 31659527 .
- ^ Фиуза С.М., Амадо А.М., Оливейра П.Дж., Сардан В.А., Де Карвалью Л.Б., Маркес М.П. (2006). «Полиаминные комплексы Pt (II) и Pd (II) как новые противораковые препараты: исследование структуры и активности» . Письма о дизайне и открытии лекарств . 3 (3): 149–151. дои : 10.2174/157018006776286989 . hdl : 10316/45139 .
- ^ Тейшейра Л.Дж., Сибра М., Рейс Э., да Круз М.Т., де Лима М.К., Перейра Э. и др. (май 2004 г.). «Цитотоксическая активность металлокомплексов биогенных полиаминов: полиядерные хелаты платины(II)». Журнал медицинской химии . 47 (11): 2917–2925. дои : 10.1021/jm0311238 . hdl : 10316/10605 . ПМИД 15139770 .
- ^ Винчи Д., Шатейнер Д. (1 декабря 2022 г.). «Синтез и структурная характеристика нового биядерного комплекса платины (III) [Pt 2 Cl 4 (NH 3 ) 2 {μ-HN=C(O)Bu t } 2 ]» . Acta Crystallographica Раздел B Структурные науки, кристаллотехника и материалы . 78 (6): 835–841. дои : 10.1107/S2052520622009660 . ISSN 2052-5206 . ПМЦ 9728019 .
- ^ Омонди Р.О., Ойвач С.О., Джагани Д. (ноябрь 2020 г.). «Обзор сравнительных исследований цитотоксической активности комплексов Pt(II), Pd(II), Ru(II)/(III) и Au(III), их кинетики реакций замещения лигандов и взаимодействий ДНК/БСА». Неорганика Химика Акта . 512 : 119883. doi : 10.1016/j.ica.2020.119883 . S2CID 225575546 .
Дальнейшее чтение [ править ]
- Ридделл И.А., Липпард С.Дж. (2018). «Цисплатин и оксалиплатин: наше нынешнее понимание их действия». В Sigel A, Sigel H, Freisinger E, Sigel RK (ред.). Металло-лекарства: разработка и действие противораковых средств . Ионы металлов в науках о жизни. Том. 18. Берлин: де Грюйтер ГмбХ. стр. 1–42. дои : 10.1515/9783110470734-007 . ISBN 978-3-11-046984-4 . ПМИД 29394020 .
Внешние ссылки [ править ]
- «Цисплатин» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- Монография МАИР: «Цисплатин»
- Аминные комплексы
- Бионеорганическая химия
- Лечение рака
- Химиотерапия
- Хлорные комплексы
- Координационные комплексы
- Канцерогены группы МАИР 2А
- Медицинская неорганическая химия
- Металлосодержащие препараты
- Нефротоксины
- Платиновые комплексы
- Противоопухолевые средства на основе платины
- Соединения платины(II)
- Основные лекарства Всемирной организации здравоохранения