Ромовый соус
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Истодах |
| Другие имена | ФК228; ФР901228; Истодакс |
| Медлайн Плюс | а610005 |
| Данные лицензии |
|
| Маршруты администрация | Внутривенная инфузия |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | Не применимо (только IV) |
| Связывание с белками | 92–94% |
| Метаболизм | Печень (в основном CYP3A4 -опосредованная) |
| Период полувыведения | 3 часа |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЭБ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.211.884 |
| Химические и физические данные | |
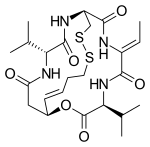
| Формула | С 24 Ч 36 Н 4 О 6 С 2 |
| Молярная масса | 540.69 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Ромидепсин , продаваемый под торговой маркой Istodax , представляет собой противораковый агент , используемый при кожной Т-клеточной лимфоме (CTCL) и других периферических Т-клеточных лимфомах (PTCL). Ромидепсин является натуральным продуктом, полученным из бактерии Chromobacterium violaceum , и действует путем блокирования ферментов, известных как деацетилазы гистонов , тем самым вызывая апоптоз . [ 2 ] Его иногда называют депсипептидом , по классу молекул, к которому он принадлежит. Ромидепсин выпускается под торговой маркой Gloucester Pharmaceuticals, входящей в состав Celgene , и принадлежит ей . [ 3 ]
История
[ редактировать ]Ромидепсин впервые был описан в научной литературе в 1994 году группой исследователей из фармацевтической компании Fujisawa (ныне Astellas Pharma ) в Цукубе , Япония, которые выделили его в культуре Chromobacterium violaceum из образца почвы, полученного в префектуре Ямагата . [ 4 ] Было обнаружено, что он практически не обладает антибактериальной активностью, но обладает высокой цитотоксичностью в отношении нескольких линий раковых клеток человека , не влияя на нормальные клетки; исследования на мышах позже показали, что он обладает противоопухолевой активностью in vivo . и [ 4 ]
Первый полный синтез ромидепсина был осуществлен исследователями из Гарварда и опубликован в 1996 году. [ 5 ] Механизм его действия был выяснен в 1998 году, когда исследователи из Фудзисавы и Токийского университета обнаружили, что он является ингибитором гистондеацетилазы с эффектами, аналогичными эффектам А. трихостатина [ 6 ]
Клинические испытания
[ редактировать ]I фаза исследований ромидепсина, первоначально получившего кодовые названия FK228 и FR901228, началась в 1997 году. [ 7 ] Испытания фазы II и фазы III проводились по различным показаниям. Наиболее значимые результаты были получены при лечении кожной Т-клеточной лимфомы (КТКЛ) и других периферических Т-клеточных лимфом (ПТКЛ). [ 7 ]
В 2004 году ромидепсин получил от FDA статус ускоренного режима для лечения кожной Т-клеточной лимфомы и статус орфанного препарата от FDA и Европейского агентства по лекарственным средствам по тому же показанию. [ 7 ]
FDA одобрило ромидепсин для лечения CTCL в ноябре 2009 г. [ 8 ] и одобрили ромидепсин для лечения других периферических Т-клеточных лимфом (PTCL) в июне 2011 года. [ 9 ]
Рандомизированное исследование III фазы ромидепсин + химиотерапия CHOP по сравнению с химиотерапией CHOP у пациентов с периферической Т-клеточной лимфомой дало отрицательные результаты, не оказав существенного влияния на выживаемость без прогрессирования или общую выживаемость. [ 10 ]
Доклиническое исследование ВИЧ
[ редактировать ]В 2014 году компания PLOS Pathogens опубликовала исследование с участием ромидепсина в исследовании, направленном на реактивацию латентного вируса ВИЧ с целью истощения резервуара ВИЧ. Латентно инфицированные Т-клетки подвергались воздействию ромидепсина in vitro и ex vivo , что приводило к увеличению обнаруживаемых уровней РНК ВИЧ, ассоциированной с клетками. В исследовании также сравнивали эффект ромидепсина с другим ингибитором гистондеацетилазы, вориностатом. [ 11 ]
Исследование аутизма на животных моделях
[ редактировать ]Исследование с использованием ромидепсина на животных показало, что кратковременное лечение небольшими количествами ромидепсина может обратить вспять социальные дефициты в модели аутизма на мышах. [ 12 ]
Фармакодинамика
[ редактировать ]В исследовании фазы II ромидепсина с участием пациентов с CTCL или PTCL были доказательства повышенного ацетилирования гистонов в мононуклеарных клетках периферической крови (PBMC) в течение 4–48 часов. Экспрессия гена ABCB1, маркера экспрессии генов, индуцированной ромидепсином, также была увеличена как в РВМС, так и в образцах биопсии опухоли. Увеличение экспрессии генов после увеличения ацетилирования гистонов является ожидаемым эффектом ингибитора HDAC. Повышенный уровень гемоглобина F (еще один суррогатный маркер изменений экспрессии генов, возникающих в результате ингибирования HDAC) также был обнаружен в крови после введения ромидепсина, а стойкое ацетилирование гистонов было обратно связано с клиренсом препарата и напрямую связано с реакцией пациента на терапию. [ 13 ]
Дозировка и способ применения
[ редактировать ]Утвержденная доза ромидепсина как при CTCL, так и при PTCL составляет четырехчасовое внутривенное введение 14 мг/м2 в 1, 8 и 15 дни 28-дневного цикла лечения. [ 6 ] Этот цикл следует повторять до тех пор, пока пациент продолжает получать пользу и переносить терапию. У некоторых пациентов с выраженной токсичностью возможно снижение дозы до 10 мг/м2.
Фармакокинетика
[ редактировать ]В исследованиях с участием пациентов с распространенным раком ромидепсин продемонстрировал линейную фармакокинетику в диапазоне доз от 1,0 до 24,9 мг/м2 при внутривенном введении в течение четырех часов. [ 14 ] Возраст, раса, пол, нарушение функции почек легкой и тяжелой степени и нарушение функции печени легкой и средней степени не влияли на фармакокинетику ромидепсина. После повторного приема не наблюдалось накопления концентрации в плазме. [ 6 ]
Механизм действия
[ редактировать ]Ромидепсин действует как пролекарство в котором дисульфидная связь восстанавливается , внутри клетки с высвобождением цинксвязывающего тиола . [ 4 ] [ 15 ] [ 16 ] Тиол связывается с атомом цинка в связывающем кармане Zn-зависимой гистондеацетилазы, блокируя ее активность. Таким образом, это ингибитор HDAC . Многие ингибиторы HDAC являются потенциальными средствами лечения рака благодаря способности эпигенетически восстанавливать нормальную экспрессию генов-супрессоров опухолей, что может приводить к остановке клеточного цикла, дифференцировке и апоптозу . [ 17 ]
Побочные эффекты
[ редактировать ]Использование ромидепсина всегда связано с побочными эффектами . [ 18 ] В клинических исследованиях наиболее распространенными были тошнота и рвота , усталость , инфекция , потеря аппетита и нарушения со стороны крови (включая анемию , тромбоцитопению и лейкопению ). Это также связано с инфекциями и метаболическими нарушениями (такими как аномальный уровень электролитов ), кожными реакциями, изменением вкусового восприятия и изменениями сердечной электропроводности . [ 18 ]
Ссылки
[ редактировать ]- ^ «Ромидепсин-МСН, Ромидепсин-Рич (Reach Pharmaceuticals Pty Ltd)» . Управление терапевтических товаров (TGA) . 13 января 2023 года. Архивировано из оригинала 18 марта 2023 года . Проверено 29 апреля 2023 г.
- ^ «Ромидепсин» . Национальный институт рака. Архивировано из оригинала 9 мая 2009 г. Проверено 11 сентября 2009 г.
- ^ «Ромидепсин» . Глостер Фармасьютикалс . Проверено 11 сентября 2009 г. [ постоянная мертвая ссылка ]
- ^ Jump up to: а б с Уэда Х., Накадзима Х., Хори Ю., Фудзита Т., Нисимура М., Гото Т., Окухара М. (март 1994 г.). «FR901228, новый противоопухолевый бициклический депсипептид, продуцируемый Chromobacterium violaceum № 968. I. Таксономия, ферментация, выделение, физико-химические и биологические свойства и противоопухолевая активность» . Журнал антибиотиков . 47 (3): 301–310. дои : 10.7164/антибиотики.47.301 . ПМИД 7513682 .
- ^ Ли К.В., Ву Дж., Син В., Саймон Дж.А. (июль 1996 г.). «Тотальный синтез противоопухолевого депсипептида FR-901,228». Журнал Американского химического общества . 118 (30): 7237–8. дои : 10.1021/ja9613724 .
- ^ Jump up to: а б с Накадзима Х., Ким Ю.Б., Терано Х., Ёсида М., Хориноути С. (май 1998 г.). «FR901228, мощный противоопухолевый антибиотик, представляет собой новый ингибитор гистондеацетилазы». Экспериментальные исследования клеток . 241 (1): 126–133. дои : 10.1006/excr.1998.4027 . ПМИД 9633520 .
- ^ Jump up to: а б с Масуока Ю., Шиндо Н., Инамура Н. (2008). «Ингибиторы гистондеацетилазы микроорганизмов: опыт Astellas». В Петерсене Ф., Амштуце Р. (ред.). Природные соединения как лекарства . Том. 2. Базель: Биркхойзер. стр. 335–59. ISBN 978-3-7643-8594-1 . Получено 8 ноября 2009 г. с помощью Поиска книг Google .
- ^ «Новые разрешения на лекарства - Часть XXII - Ромидепсин (Истодакс)» . Архивировано из оригинала 3 марта 2016 г. Проверено 3 декабря 2009 г.
- ^ «Drugs@FDA: препараты, одобренные FDA» . Архивировано из оригинала 24 июля 2013 г. Проверено 31 августа 2015 г.
- ^ «Окончательный анализ исследования фазы III Ro-CHOP (проведенного LYSA): ромидепсин плюс CHOP у пациентов с периферической Т-клеточной лимфомой» . 5 декабря 2020 года. Архивировано из оригинала 21 мая 2021 года . Проверено 21 мая 2021 г.
- ^ Вэй Д.Г., Чан В., Файн Э., Балакришнан М., Барнс Т., Граупе М. и др. (апрель 2014 г.). «Ингибитор гистондеацетилазы ромидепсин индуцирует экспрессию ВИЧ в Т-клетках CD4 у пациентов, получающих супрессивную антиретровирусную терапию, в концентрациях, достигаемых путем клинического дозирования» . ПЛОС Патогены . 10 (4): e1004071. дои : 10.1371/journal.ppat.1004071 . ПМК 3983056 . ПМИД 24722454 .
- ^ Цинь Л., Ма К., Ван З.Дж., Ху З., Мэйтас Е., Вэй Дж., Ян З. (апрель 2018 г.). «Социальные дефициты в моделях аутизма на мышах с дефицитом Shank3 устраняются за счет ингибирования деацетилазы гистонов (HDAC)» . Природная неврология . 21 (4): 564–575. дои : 10.1038/s41593-018-0110-8 . ПМК 5876144 . ПМИД 29531362 .
- ^ Бейтс С.Е., Жан З., Стедман К., Обрзут Т., Лученко В., Фрай Р. и др. (январь 2010 г.). «Лабораторные корреляты исследования фазы II ромидепсина при кожной и периферической Т-клеточной лимфоме» . Британский журнал гематологии . 148 (2): 256–267. дои : 10.1111/j.1365-2141.2009.07954.x . ПМЦ 2838427 . ПМИД 19874311 .
- ^ Брэднер Дж.Э., Уэст Н., Грачан М.Л., Гринберг Э.Ф., Хаггарти С.Дж., Варнов Т., Мазичек Р. (март 2010 г.). «Химическая филогенетика деацетилаз гистонов» . Химическая биология природы . 6 (3): 238–243. дои : 10.1038/nchembio.313 . ПМК 2822059 . ПМИД 20139990 .
- ^ Сигемацу Н., Уэда Х., Такасе С., Танака Х., Ямамото К., Тада Т. (март 1994 г.). «FR901228, новый противоопухолевый бициклический депсипептид, продуцируемый Chromobacterium violaceum № 968. II. Определение структуры» . Журнал антибиотиков . 47 (3): 311–314. дои : 10.7164/антибиотики.47.311 . ПМИД 8175483 .
- ^ Уэда Х., Манда Т., Мацумото С., Мукумото С., Нисигаки Ф., Кавамура И., Симомура К. (март 1994 г.). «FR901228, новый противоопухолевый бициклический депсипептид, продуцируемый Chromobacterium violaceum № 968. III. Противоопухолевое действие на экспериментальные опухоли у мышей» . Журнал антибиотиков . 47 (3): 315–323. дои : 10.7164/антибиотики.47.315 . ПМИД 8175484 .
- ^ Грешок Т.Дж., Джонс Д.М., Ногучи Ю., Уильямс Р.М. (февраль 2008 г.). «Улучшение общего синтеза мощного ингибитора HDAC FK228 (FR-901228)» . Органические письма . 10 (4): 613–616. дои : 10.1021/ol702957z . ПМК 3097137 . ПМИД 18205373 .
- ^ Jump up to: а б «Набор Истодакс-ромидепсин» . ДейлиМед . Национальная медицинская библиотека США. 30 июля 2021 года. Архивировано из оригинала 26 ноября 2022 года . Проверено 29 апреля 2023 г.