Андрогенная депривационная терапия
| Андрогенная депривационная терапия | |
|---|---|
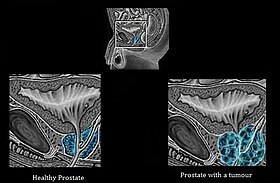 Отличия здоровой простаты от простаты с опухолью | |
| Другие имена | Андрогенная супрессивная терапия |
| Специальность | онкология |
Андрогендепривационная терапия ( АДТ ), также называемая терапией андрогенной абляции или андрогенсупрессивной терапией , представляет собой антигормональную терапию , основное применение которой заключается в лечении рака простаты . Для роста раковых клеток простаты обычно требуются андрогенные гормоны , такие как тестостерон . ADT снижает уровень андрогенных гормонов с помощью лекарств или хирургического вмешательства , чтобы предотвратить рост клеток рака простаты. [1] Фармацевтические подходы включают антиандрогены и химическую кастрацию .
Несколько исследований пришли к выводу, что АДТ продемонстрировала пользу у пациентов с метастатическим заболеванием и в качестве дополнения к лучевой терапии у пациентов с местно-распространенным заболеванием, а также у пациентов с неблагоприятным локализованным заболеванием среднего или высокого риска. Однако у пациентов с раком простаты низкого риска АДТ не продемонстрировало преимущества в выживаемости, но принесло значительный вред, такой как импотенция, диабет и потеря костной массы. [2] [3] [4] [5] [6]
Терапия также может уничтожить раковые клетки, индуцируя старение, вызванное лишением андрогенов . [7] Снижение уровня андрогенов или прекращение их проникновения в клетки рака простаты часто приводит к тому, что рак простаты на какое-то время уменьшается или замедляется. Однако это лечение необходимо сочетать с лучевой терапией (ЛТ). [8] потому что АДТ сама по себе не искореняет рак ; это просто снижает его агрессивность. [9]
Типы
[ редактировать ]Метод, основанный на хирургическом вмешательстве
[ редактировать ]- Орхиэктомия (хирургическая кастрация)
- Он заключается в удалении яичек , органа, в котором андрогены синтезируются , у больного раком. Это наиболее радикальный метод прекращения выработки андрогенов. Более того, это самый простой и дешевый вариант. Основным недостатком является то, что хирургическая кастрация является постоянным методом.
Методы на основе препаратов
[ редактировать ]
- Синтез тестостерона опосредован цепочкой процессов, которые начинаются в мозге. Когда организм обнаруживает низкий уровень тестостерона, гипоталамус начинает вырабатывать ЛГРГ . ЛГРГ активирует синтез ЛГ (лютеинизирующего гормона) в гипофизе. ЛГ индуцирует синтез тестостерона в яичках. [10] Существует два разных лекарства: ЛГРГ агонисты и антагонисты , которые снижают количество тестостерона, вырабатываемого яичками. Они действуют путем ингибирования образования ЛГ в гипофизе. Агонисты ЛГРГ вызывают внезапное повышение уровня тестостерона, за которым следует резкое падение, процесс, называемый обострением , тогда как антагонисты ЛГРГ непосредственно снижают количество тестостерона. Агонисты и антагонисты ЛГРГ, используемые в андрогенной депривационной терапии, включают лейпрорелин (лейпролид) , гозерелин , трипторелин , гистрелин , бусерелин и дегареликс .
- Эти препараты вводятся под кожу, достигая того же результата, что и хирургическая кастрация . Химическая кастрация может быть предпочтительнее хирургической кастрации. [ нужна ссылка ] поскольку он сохраняет яички неповрежденными.
- Антиандрогенная терапия
- Надпочечники были обнаружены как еще один центр производства андрогенов даже после процесса кастрации. Поэтому было разработано дополнительное лечение, в котором используются антиандрогены, чтобы блокировать способность организма использовать любые андрогены. Клетки простаты содержат андрогеновый рецептор (AR), который при стимуляции андрогенами, такими как тестостерон, способствует росту и поддерживает дифференцировку простаты. Однако эти сигналы, способствующие росту, могут быть проблематичными, когда они возникают в раковой клетке. Антиандрогены могут проникать в клетки и предотвращать связывание тестостерона с белками-рецепторами из-за их более высокого сродства к андрогеновым рецепторам.
- Основными антиандрогенами являются ципротерона ацетат , флутамид , нилутамид , бикалутамид и энзалутамид , которые назначаются в форме пероральных таблеток.
- новые антиандрогены, воздействующие на синтез тестостерона ( абиратерона ацетат и севитеронел ) или ядерную транслокацию АР ( энзалутамид , апалутамид и даролутамид ), а также комбинированные методы лечения ( галетерон Недавно были разработаны ), которые могут лучше воздействовать на андроген-чувствительные клетки в сочетании с АДТ. [11] Но они также могут иметь негативную отрицательную роль в развитии CRPC .
Влияние на мужскую сексуальность
[ редактировать ]Нормальная мужская сексуальность, похоже, зависит от очень специфических и сложных гормональных закономерностей, которые до конца не изучены. [12] Одно исследование предполагает, что АДТ может изменить гормональный баланс, необходимый для мужской сексуальной активности. С возрастом уровень тестостерона у мужчин снижается примерно на 1% в год после 30 лет; однако важно определить, вызван ли низкий уровень тестостерона нормальным старением или заболеванием, таким как гипогонадизм. [13] Тестостерон играет важную роль в сексуальном функционировании; следовательно, естественное снижение уровня тестостерона может привести к снижению нормального сексуального функционирования. Дальнейшее снижение уровня тестостерона в сыворотке может оказать негативное влияние на нормальную сексуальную функцию, что приведет к снижению качества жизни. [14]
Эректильная дисфункция не является редкостью после радикальной простатэктомии, и у мужчин, перенесших АДТ в дополнение к этому, вероятно, будет наблюдаться дальнейшее снижение их способности вступать в проникающий половой акт, а также их желания это делать. [13] Исследование, изучающее различия в использовании GnRH-A (и супрессантов андрогенов) или орхиэктомии, сообщает о различиях в сексуальном интересе, опыте эрекции и распространенности участия в сексуальной активности. Число мужчин, сообщивших об отсутствии сексуального интереса, увеличилось с 27,6% до 63,6% после орхиэктомии и с 31,7% до 58,0% после GnRH-A; у мужчин, у которых не было эрекции, этот показатель увеличился с 35,0% до 78,6%; а число мужчин, не сообщавших о сексуальной активности, увеличилось с 47,9% до 82,8% после орхиэктомии и с 45,0% до 80,2%. [14] Это исследование предполагает, что GnRH-A и орхиэктомия оказали одинаковое влияние на сексуальное функционирование. Это порочный круг, в котором снижение уровня тестостерона приводит к снижению сексуальной активности, что, в свою очередь, приводит к еще большему снижению уровней свободного и общего тестостерона. [12] Это демонстрирует важность андрогенов для поддержания сексуальных структур и функций. [12] [15]
Побочные эффекты
[ редактировать ]Хотя воздействие на андрогенную ось имеет явную терапевтическую пользу, его эффективность носит временный характер, поскольку опухолевые клетки простаты адаптируются, чтобы выжить и расти. Было показано, что удаление андрогенов активирует эпителиально-мезенхимальный переход (ЕМТ), нейроэндокринную трансдифференцировку (NEtD) и генные программы, подобные раковым стволовым клеткам . [16]
- ЕМТ установила свою роль в продвижении биологических фенотипов, связанных с прогрессированием опухоли (миграция/инвазия, выживание опухолевых клеток, свойства, подобные раковым стволовым клеткам, устойчивость к радиации и химиотерапии) при многих типах рака человека.
- НЭТД при раке предстательной железы связан с резистентностью к терапии, висцеральными метастазами и агрессивностью заболевания.
- Фенотипы раковых стволовых клеток связаны с рецидивом заболевания, метастазированием и выживанием клеток в кровообращении в виде циркулирующих опухолевых клеток .
Таким образом, активация этих программ посредством ингибирования андрогенной оси обеспечивает механизм, с помощью которого опухолевые клетки могут адаптироваться, способствуя рецидиву и прогрессированию заболевания. [11]
Орхиэктомия, аналоги ЛГРГ и антагонисты ЛГРГ могут вызывать схожие побочные эффекты из-за изменений уровня половых гормонов (тестостерона). [17]
Для пациентов и их партнеров была разработана программа, позволяющая распознавать и справляться с наиболее тяжелыми побочными эффектами андрогенной депривационной терапии. Одна программа построена на основе книги 2014 года «Андрогендепривационная терапия: основное руководство для пациентов с раком простаты и их близких», одобренной Канадской урологической ассоциацией. [18]
Недавние исследования показали, что АДТ может увеличить риск болезни Альцгеймера или деменции. [19] Увеличение риска может быть связано с продолжительностью АДТ. [20] Хотя некоторые исследования сообщают о снижении определенных областей когнитивных функций, таких как пространственные способности , внимание и вербальная память, связанных с АДТ, данные в целом остаются противоречивыми. [21] [22] [23] Полезные профилактические меры могут включать , среди прочего, социальное взаимодействие , физические упражнения и « средиземноморскую диету ». [21] Существует дополнительный небольшой риск сердечной аритмии.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перлмуттер и Лепор (2007). «Андрогендепривационная терапия в лечении распространенного рака простаты» . Преподобный Урол . 9 (Приложение 1): С3–8. ПМЦ 1831539 . ПМИД 17387371 .
- ^ «Рак простаты – в центре внимания двух исследований, комментарий» . JAMA Внутренняя медицина, Пресс-релизы . 14 июля 2014 г.
- ^ Грейс Л. Лу-Яо; Питер К. Альбертсен; Дирк Ф. Мур; и др. (сентябрь 2014 г.). «Результаты пятнадцатилетней выживаемости после первичной андрогенной депривационной терапии локализованного рака простаты» . Стажер ЖАМА. Мед . 174 (9): 1460–1467. doi : 10.1001/jamainternmed.2014.3028 . ПМЦ 5499229 . ПМИД 25023796 .
- ^ Куок-Дьен Трин; Дебора Шраг (сентябрь 2014 г.). «Измерение эффективности андрогенной депривационной терапии рака простаты среди населения Medicare. Адекватные данные не являются ни тем же самым, ни врагом идеальных данных». Стажер ЖАМА. Мед . 174 (9): 1468–9. doi : 10.1001/jamainternmed.2014.1107 . ПМИД 25023522 .
- ^ Карен Э. Хоффман; Цзянгун Ню; Ю Шен; и др. (сентябрь 2014 г.). «Вариации врачебного лечения рака простаты низкого риска: популяционное когортное исследование» . Стажер ЖАМА. Мед . 174 (9): 1450–9. doi : 10.1001/jamainternmed.2014.3021 . ПМЦ 4372187 . ПМИД 25023650 .
- ^ АНАХАД О'КОННОР (14 июля 2014 г.). «Скидки на исследование тестостероновой терапии при раннем раке простаты» . Нью-Йорк Таймс .
Существует так много побочных эффектов, связанных с этой терапией, и очень мало доказательств в поддержку ее использования», — сказала доктор Грейс Л. Лу-Яо, исследователь из Института рака Рутгерса в Нью-Джерси и ведущий автор опубликованного отчета. в понедельник в JAMA Internal Medicine «Я бы сказал, что для большинства пациентов с локализованным раком простаты это не лучший вариант.
- ^ Бертон, Доминик Джорджия; Гирибальди, Мария Г.; Муньос, Анислейдис; Халворсен, Кэтрин; Патель, Асмита; Хорда, Мерс; Перес-Стабль, Карлос; Рай, Приямвада; Агульник, Ирина Ю. (27 июня 2013 г.). Агульник, Ирина Ю. (ред.). «Старение, вызванное андрогенной депривацией, способствует росту резистентных к андрогенам клеток рака простаты» . ПЛОС ОДИН . 8 (6): e68003. Бибкод : 2013PLoSO...868003B . дои : 10.1371/journal.pone.0068003 . ПМЦ 3695935 . ПМИД 23840802 .
- ^ Вард, Падрейг; Мейсон, Малькольм; Дин, Кейю; Киркбрайд, Питер; Брандейдж, Майкл; Коуэн, Ричард; Господирович, Мария; Сандерс, Карен; Косташук, Эдмунд; Суонсон, Грег; Барбер, Джим; Хильц, Андреа; Пармар, Махеш КБ; Сатья, Джинка; Андерсон, Джон; Хейтер, Чарльз; Хетерингтон, Джон; Сайдс, Мэтью Р.; Парулекар, Венди; для следователей NCIC CTG PR.3/MRC UK PR07 (2011 г.). «Комбинированная андрогенная депривация и лучевая терапия местно-распространенного рака простаты: рандомизированное исследование 3 фазы» . Ланцет . 378 (9809): С2104–2111. дои : 10.1016/s0140-6736(11)61095-7 . ПМК 3243932 . ПМИД 22056152 .
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ) «Комбинированная андрогендепривационная терапия и лучевая терапия местно-распространенного рака простаты: рандомизированное исследование, фаза 3» - ^ Ежедневная газета науки
- ^ Руководство по раку простаты
- ^ Jump up to: а б Нури, М; Скорее, Э; Стилиану, Н; Нельсон, CC; Холлиер, Б.Г.; Уильямс, ЭД (2014). «Андроген-таргетная терапия, индуцированная эпителиально-мезенхимальной пластичностью и нейроэндокринной трансдифференцировкой при раке предстательной железы: возможность вмешательства» . Передний Онкол . 4 : 370. doi : 10.3389/fonc.2014.00370 . ПМЦ 4274903 . ПМИД 25566507 .
- ^ Jump up to: а б с Маццола, ЧР; Малхолл, JP (2012). «Влияние андрогенной депривационной терапии на сексуальную функцию» . Азиатский журнал андрологии . 14 (2): 198–203. дои : 10.1038/aja.2011.106 . ПМК 3735098 . ПМИД 22231298 .
- ^ Jump up to: а б (2012). Тестостероновая терапия: ключ к мужской жизнеспособности? Получено с: http://www.mayoclinic.com/health/testosterone-therapy/MC00030.
- ^ Jump up to: а б Шарифи, Н.; Галли, Дж.Л.; Дахут, WL (2005). «Андрогендепривационная терапия рака простаты» . Журнал Американской медицинской ассоциации . 294 (2): 238–244. дои : 10.1001/jama.294.2.238 . ПМИД 16014598 .
- ^ «Дефицит тестостерона» . Проверено 5 мая 2015 г.
- ^ Нури М., Карадек Дж., Лубик А.А., Ли Н., Холлиер Б.Г., Тахар М., Альтимирано-Димас М., Чен М., Рошан-Монири М., Батлер М., Леман М., Бишоп Дж., Труонг С., Хуанг С.К., Кокрейн Д., Кокс М., Коллинз С., Глив М., Эрхо Н., Альшалафа М., Дависиони Е., Нельсон С., Грегори-Эванс С., Карнес Р.Дж., Дженкинс Р.Б., Кляйн Э.А., Буттян Р. (январь 2017 г.). «Вызванное терапией перепрограммирование развития клеток рака простаты и приобретенная резистентность к терапии» . Онкотаргет . 8 (12): 18949–18967. дои : 10.18632/oncotarget.14850 . ПМЦ 5386661 . ПМИД 28145883 .
- ^ Резюме Medline
- ^ ЖИЗНЬOnADT
- ^ Джавадеваппа, Равишанкар; Чхатре, Сумедха; Малкович, Брюс; Парих, Рави; Гуццо, Томас; Вейн, Алан (3 июля 2019 г.). «Связь между использованием андрогенной депривационной терапии и диагностикой деменции у мужчин с раком простаты» . Открытая сеть JAMA . 20192 (7): e196562. doi : 10.1001/jamanetworkopen.2019.6562 . ПМК 6613289 . PMID 31268539 .
- ^ Нид, Кевин Т.; Гаскин, Грег; Честер, Кариад; Свишер-МакКлюр, Сэмюэл; Дадли, Джоэл Т.; Липер, Николас Дж.; Шах, Нигам Х. (20 февраля 2016 г.). «Андрогендепривационная терапия и риск развития болезни Альцгеймера в будущем» . Журнал клинической онкологии . 34 (6): 566–571. дои : 10.1200/JCO.2015.63.6266 . ISSN 1527-7755 . ПМК 5070576 . ПМИД 26644522 .
- ^ Jump up to: а б Черье, Моник М.; Хигано, Селестия С. (1 февраля 2020 г.). «Влияние андрогенной депривации на настроение, когнитивные функции и риск развития болезни Альцгеймера» . Урологическая онкология: семинары и оригинальные исследования . 38 (2): 53–61. дои : 10.1016/j.urolonc.2019.01.021 . ISSN 1078-1439 . ПМИД 30862408 .
- ^ Джамадар, Рода Дж; Уинтерс, Мэри Дж; Маки, Полина М (март 2012 г.). «Когнитивные изменения, связанные с АДТ: обзор литературы» . Азиатский журнал андрологии . 14 (2): 232–238. дои : 10.1038/aja.2011.107 . ISSN 1008-682X . ПМЦ 3735092 . ПМИД 22343495 .
- ^ МакХью, Диглан Дж.; Рут, Джеймс С.; Нельсон, Кристиан Дж.; Моррис, Майкл Дж. (1 апреля 2018 г.). «Андрогендепривационная терапия, деменция и когнитивная дисфункция у мужчин с раком простаты: сколько дыма и сколько огня?» . Рак . 124 (7): 1326–1334. дои : 10.1002/cncr.31153 . ISSN 0008-543X . ПМЦ 5885282 . ПМИД 29338083 .
Что касается снижения когнитивных функций, хотя авторы предлагают биологически обоснованное объяснение развития когнитивных нарушений при АДТ, многие исследования являются небольшими, методологически ошибочными, но провоцируют гипотезы. Они не образуют объем работы, который может независимо поддержать вывод или изменение в практике.