Перекрестные помехи (биология)
Биологические перекрестные помехи относятся к случаям, когда один или несколько компонентов одного пути передачи сигнала влияют на другой. Этого можно достичь несколькими способами, наиболее распространенным из которых являются перекрестные помехи между белками сигнальных каскадов. В этих путях передачи сигнала часто имеются общие компоненты, которые могут взаимодействовать с любым путем. Более сложный пример перекрестных помех можно наблюдать при трансмембранных перекрестных помехах между внеклеточным матриксом (ECM) и цитоскелетом .
Перекрестные помехи между сигнальными путями
[ редактировать ]Одним из примеров перекрестных помех между белками в сигнальном пути можно увидеть роль циклического аденозинмонофосфата (цАМФ) в регуляции пролиферации клеток путем взаимодействия с киназным путем митоген-активируемого протеина (MAP). цАМФ представляет собой соединение, синтезируемое в клетках аденилатциклазой в ответ на различные внеклеточные сигналы. [1] цАМФ в первую очередь действует как внутриклеточный вторичный мессенджер, основным внутриклеточным рецептором которого является цАМФ-зависимая протеинкиназа (ПКА), которая действует посредством фосфорилирования белков-мишеней. [2] Путь передачи сигнала начинается с внеклеточных взаимодействий лиганд-рецептор. Затем этот сигнал передается через мембрану, стимулируя аденилатциклазу на внутренней поверхности мембраны, которая катализирует превращение АТФ в цАМФ. [3] [4]
ERK, белок, участвующий в сигнальном пути МАРК, может активироваться или ингибироваться цАМФ. [5] цАМФ может ингибировать ERK различными способами, большинство из которых включают цАМФ-зависимую протеинкиназу (PKA) и ингибирование Ras-зависимых сигналов Raf-1. [6] Однако цАМФ также может стимулировать пролиферацию клеток, стимулируя ERK. Это происходит за счет индукции специфических генов посредством фосфорилирования фактора транскрипции CREB с помощью PKA. [5] Хотя ERKs, по-видимому, не являются обязательными для этого фосфорилирования CREB, путь MAPK снова участвует в перекрестных помехах, поскольку ERKs необходимы для фосфорилирования белков, находящихся ниже CREB. [5] Другие известные примеры необходимости ERK для транскрипционных эффектов, индуцированных цАМФ, включают индукцию гена пролактина в клетках гипофиза и гена бета-гидроксилата дофамина в феохромоцитомальных клетках (PC12). [6] Существует ряд разнообразных механизмов, с помощью которых цАМФ может влиять на передачу сигналов ERK. Большинство механизмов, включающих ингибирование цАМФ ERK, отделяют Raf-1 от активации Ras посредством прямого взаимодействия PKA с Raf-1 или косвенно через взаимодействие PKA с ГТФазой Rap1. [6] (см. рисунок 1). PKA также может отрицательно регулировать ERK за счет активации PTPases. Механизмы активации ERK с помощью цАМФ еще более разнообразны, обычно включая Rap1 или Ras и даже непосредственно цАМФ. [6]

Трансмембранные перекрестные помехи
[ редактировать ]Перекрестные помехи можно наблюдать даже через мембраны. Мембранные взаимодействия с внеклеточным матриксом (ECM) и соседними клетками могут вызывать различные реакции внутри клетки. Однако топография и механические свойства ЕСМ также играют важную роль в мощных и сложных перекрестных помехах с клетками, растущими на матрице или внутри нее. [7] Например, интегрином опосредованную сборку цитоскелета и даже подвижность клеток . физическое состояние ЕСМ влияет на [7] Связывание интегрина α5β1 с его лигандом ( фибронектином ) активирует образование фибриллярных спаек и актиновых филаментов . [5] Тем не менее, если ЕСМ иммобилизован, подобная реорганизация матрикса и образование фибриллярных спаек тормозятся. [7] В свою очередь, связывание того же интегрина (α5β1) с иммобилизованным лигандом фибронектина приводит к образованию высокофосфорилированных фокальных контактов/ фокальной адгезии (клеток, участвующих в адгезии матрикса) внутри мембраны и снижает скорость миграции клеток. [7] В другом примере перекрестных помех это изменение состава фокальных контактов в цитоскелете может ингибироваться участниками еще одного пути: ингибиторами киназ легкой цепи миозина или киназ Rho, H-7 или ML-7, которые снижают сократимость клеток. и, следовательно, подвижность. [7] (см. рисунок 2).

Перекрестные помехи при активации лимфоцитов
[ редактировать ]Более сложный и конкретный пример перекрестных помех между двумя основными сигнальными путями можно наблюдать при взаимодействии сигнальных путей цАМФ и МАРК при активации лимфоцитов . В этом случае компоненты пути цАМФ прямо или косвенно влияют на сигнальный путь МАРК, предназначенный для активации генов, участвующих в иммунитете и лимфоцитах.
Новообразованный цАМФ высвобождается из мембраны и диффундирует по внутриклеточному пространству , где служит для активации ПКА. Для активации каталитическая . субъединица ПКА должна связать четыре молекулы цАМФ, после чего активация заключается в расщеплении между регуляторной и каталитической субъединицами [4] Это расщепление, в свою очередь, активирует PKA, обнажая каталитические сайты субъединиц C, которые затем могут фосфорилировать ряд белков в клетке. [4]
В лимфоцитах внутриклеточные уровни цАМФ повышаются при стимуляции антиген-рецепторов и даже в большей степени в ответ на простагландин Е и другие иммуносупрессивные агенты. [8] В этом случае цАМФ служит для подавления иммунитета игроков. ПКА типа I колокализуется с Т- и В-клеток. рецепторами антигена [9] и вызывает ингибирование активации Т- и В-клеток. ПКА даже был отмечен как прямой индуктор генов, способствующих иммуносупрессии. [10]
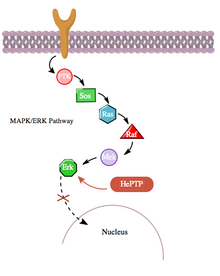
Кроме того, путь цАМФ также взаимодействует с путем МАРК более опосредованно через взаимодействие с гемопоэтической ПТФазой (HePTP). HePTP экспрессируется во всех лейкоцитах. При сверхэкспрессии в Т-клетках HePTP снижает активацию транскрипции интерлейкина-2, промотора обычно индуцируемую активированным рецептором Т-клеток через сигнальный каскад МАРК. [11] Способ, которым HePTP эффективно ингибирует передачу сигналов MAPK, заключается во взаимодействии с MAP-киназами Erk1, Erk2 и p38 через короткую последовательность на некаталитическом N-конце HePTP, называемую мотивом киназного взаимодействия (KIM). [11] [12] Высокоспецифическое связывание Erk и p38 с этой субъединицей HePTP приводит к быстрой инактивации сигнального каскада (см. рисунок 3).
Однако, поскольку и HePTP, и Erk являются цитозольными ферментами , [13] разумно заключить, что существует механизм прекращения ингибирования Erk с помощью HePTP, чтобы обеспечить транслокацию активированного Erk в ядро . Действительно, как и во многих других случаях белок-белкового взаимодействия, HePTP, по-видимому, фосфорилируется Erk и p38 по сайтам Thr45 и Ser72. [11] Однако важно отметить, что на некаталитическом N-конце (область KIM) HePTP был обнаружен третий сайт фосфорилирования, который фосфорилируется до гораздо более высокой стехиометрии по пути цАМФ. [1] это еще один пример перекрестных помех между путями цАМФ и МАРК.
Фосфорилирование этого третьего сайта с помощью PKAs пути цАМФ ингибирует связывание MAP-киназ с HePTP и тем самым активирует сигнальный каскад MAPK/ERK. Путь МАРК через Ras, Raf, Mek и Erk демонстрирует низкую активность в присутствии нефосфорилированного (активного) HePTP. Однако активация пути цАМФ стимулирует активацию PKA, которая, в свою очередь, фосфорилирует HePTP по Ser23. Это предотвращает связывание HePTP с Erk и освобождает путь MAPK от ингибирования, позволяя продолжить передачу сигналов ниже по ходу (см. рисунок 4).

Более того, исследования с участием гладкомышечных клеток предсердий сердца показали, что PKA может снижать активацию MAP-киназ в ответ на фактор роста тромбоцитов ( PDGF ) путем фосфорилирования киназы c-Raf . [14] Таким образом, кажется правдоподобным, что PKA в пути цАМФ может даже в дальнейшем участвовать в регуляции активации лимфоцитов не только путем ингибирования сигнального пути антиген-рецептор MAPK на его конечной стадии, но даже дальше по ходу процесса.
Примечания и ссылки
[ редактировать ]- ^ Jump up to: а б Саксена, М. (1999), «Перекрестная связь между цАМФ-зависимой киназой и MAP-киназой через протеинтирозинфосфатазу», Nat. Клеточная Биол. , 1 (5): 305–311, doi : 10.1038/13024 , PMID 10559944 , S2CID 40413956
- ^ Скотт, JD (1991), «Циклические нуклеотид-зависимые протеинкиназы», Pharmacol. Там. , 50 (1): 123–145, doi : 10.1016/0163-7258(91)90075-W , PMID 1653962
- ^ Крупинский Дж.; и др. (1989), «Аминокислотная последовательность аденилатциклазы: возможная структура, подобная каналу или транспортеру», Science , 244 (4912): 1558–1564, Bibcode : 1989Sci...244.1558K , doi : 10.1126/science.2472670 , PMID 2472670
- ^ Jump up to: а б с Вино, Джеффри. (1999–2008), «Через мембрану; Внутриклеточные мессенджеры: цАМФ и цГМФ», Стэнфордский университет, PSYCH121.
- ^ Jump up to: а б с д Кац; и др. (2000), «Физическое состояние внеклеточного матрикса регулирует структуру и молекулярный состав адгезий клетка-матрикс», Мол. Биол. Cell , 11 (3): 1047–1060, doi : 10.1091/mbc.11.3.1047 , PMC 14830 , PMID 10712519
- ^ Jump up to: а б с д Филип Дж. С. Сторк и Джон М. Шмитт. (2002), «Перекрестная передача сигналов цАМФ и киназы MAP в регуляции клеточной пролиферации» , Trends in Cell Biology , 12 (6): 258–266, doi : 10.1016/S0962-8924(02)02294-8 , PMID 12074885
- ^ Jump up to: а б с д и Гейгер, Б.; и др. (2001), «Физическое состояние внеклеточного матрикса регулирует структуру и молекулярный состав спаек клетка-матрикс», Nature Reviews Molecular Cell Biology , 2 (11): 793–805, doi : 10.1038/35099066 , PMID 11715046 , S2CID 31064504
- ^ Ледбеттер; и др. (1986), «Связывание антител с молекулами поверхности Т-клеток CD5 (Tp67) и Tp44: влияние на циклические нуклеотиды, цитоплазматический свободный кальций и подавление, опосредованное цАМФ», Journal of Immunology , 137 (10): 3299–3305, PMID 3021852
- ^ Леви; и др. (1996), «Циклическая AMP-зависимая протеинкиназа (cAK) в В-клетках человека: совместная локализация cAK типа I (RIα2C2) с антигенным рецептором во время антииммуноглобулин-индуцированной активации B-клеток», Eur. Дж. Иммунол. , 26 (6): 1290–1296, doi : 10.1002/eji.1830260617 , PMID 8647207 , S2CID 84171254
- ^ Уислер; и др. (1991), «Циклическая AMP-модуляция пролиферативных ответов В-клеток человека: роль цАМФ-зависимых протеинкиназ в усилении ответов В-клеток на форболдиэфиры и иономицин», Cell. Иммунол. , 142 (2): 398–415, doi : 10.1016/0008-8749(92)90300-e , PMID 1320464
- ^ Jump up to: а б с Саксена, М.; и др. (1999), «Ингибирование передачи сигналов Т-клеток гематопоэтической тирозинфосфатазой, нацеленной на MAP-киназу (HePTP)», J. Biol. хим. , 274 (17): 11693–700, doi : 10.1074/jbc.274.17.11693 , PMID 10206983
- ^ Пулидо, Р. (1998), «Протеиновые тирозинфосфатазы PTP-SL и STEP регулируют активацию киназ ERK1 и ERK2, регулируемых внеклеточными сигналами, путем ассоциации через мотив взаимодействия киназ», EMBO J. , 17 (24): 7337– 7350, номер doi : 10.1093/emboj/17.24.7337 , PMC 1171079 , PMID 9857190
- ^ Кобб; и др. (1994), "Регуляция MAP-киназного каскада", Cell. Мол. Биол. Рез. , 40 (3): 253–256, PMID 7874203
- ^ Могилы; и др. (1993), «Протеинкиназа А противодействует передаче сигналов, индуцированной тромбоцитарным фактором роста, с помощью митоген-активируемой протеинкиназы в артериальных гладкомышечных клетках человека», Proc. Натл. акад. наук. США , 90 (21): 10300–10304, Bibcode : 1993PNAS...9010300G , doi : 10.1073/pnas.90.21.10300 , PMC 47762 , PMID 7694289