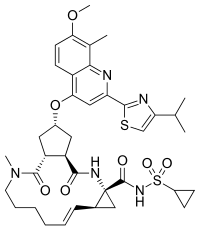
Симепревир
 | |
| Клинические данные | |
|---|---|
| Произношение | / s ɪ ˈ m ɛ p r ə v ɪər / Си- депутат Европарламента -повторно |
| Торговые названия | Олисио, Совриад, Галексос и другие. |
| Другие имена | ТМС435; ТМС435350 |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а614013 |
| Данные лицензии |
|
| Маршруты администрация | Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | 62% (в условиях сытости) |
| Связывание с белками | >99,9% |
| Метаболизм | Печень ( CYP3A , CYP2C8 , CYP2C19 ) |
| Период полувыведения | 10–13 часов (субъекты, не инфицированные ВГС), 41 час (субъекты, инфицированные ВГС) |
| Экскреция | Кал (91%), моча (<1%) |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЕМБЛ | |
| НИАИД Химическая база данных | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.215.933 |
| Химические и физические данные | |
| Формула | С 38 Ч 47 Н 5 О 7 С 2 |
| Молярная масса | 749.94 g·mol −1 |
| 3D model ( JSmol ) | |
Симепревир под торговой маркой Olysio среди прочего, , представляет собой препарат, используемый в сочетании с другими лекарствами для лечения гепатита С. , продаваемый , [2] Он специально используется при гепатите С генотипа 1 и 4. [2] Лекарства, с которыми он используется, включают софосбувир или рибавирин и пегинтерферон-альфа . [2] Показатели излечения составляют от 80 до 90 процентов. [3] [4] [5] Его можно использовать у тех, у кого также есть ВИЧ / СПИД . [2] Его принимают внутрь один раз в день в течение 12 недель. [2]
Общие побочные эффекты включают чувство усталости, головную боль, сыпь, зуд и чувствительность к солнечному свету. [2] У лиц, ранее перенесших гепатит В , активное заболевание может рецидивировать. [2] Не рекомендуется тем, у кого серьезные проблемы с печенью. [2] Во время беременности при использовании с рибавирином он может нанести вред ребенку, тогда как при использовании с софосбувиром его безопасность неясна. [2] [6] Симепревир является ингибитором протеазы вируса гепатита С. [2]
Симепревир был разработан компаниями Medivir AB и Janssen Pharmaceutica . [7] Он был одобрен для медицинского использования в США в 2013 году. [8] В 2019 году он был исключен из списка основных лекарственных средств Всемирной организации здравоохранения . [9] [10] он недоступен в качестве непатентованного лекарства. С 2015 года [update]. [6]
Медицинское использование
[ редактировать ]Симепревир показан для лечения хронической инфекции печени С (ХГС) в составе тройной схемы противовирусного лечения, состоящей из двух других препаратов: пегинтерферона-альфа (ПЭГ-ИФН) и рибавирина (РБВ). [11] Он в первую очередь эффективен при лечении пациентов, инфицированных вирусом гепатита С (ВГС) генотипа 1, с компенсированным заболеванием печени, включая цирроз печени. [11] В настоящее время нет исследований, подтверждающих эффективность Симепревира в качестве монотерапии гепатита С. [11] Симепревир обычно используется у пациентов, инфицированных ВГС генотипа 1, но медицинское применение не по назначению показано и для генотипа 4 типа. [12]
Дозирование
[ редактировать ]Симепревир применяется вместе с пег-ИФН и рибавирином в качестве тройной терапии. [11] Соответствующая дозировка симепревира зависит от функции печени и почек пациента, вирусной нагрузки и генотипа ВГС. [11] Этот препарат не рекомендуется людям с умеренным или тяжелым нарушением функции печени и людям с терминальной стадией заболевания почек, поскольку применение Симпревира у этих групп пациентов не изучалось. [11] Прием симепревира может быть прекращен в зависимости от вирусной нагрузки. [11] Например, если вирусная нагрузка пациента обнаруживается (>25 единиц/мл) в течение 4-й недели лечения, это считается неадекватным лечением и симепревир необходимо прекратить. [11]
Противопоказания
[ редактировать ]Любые противопоказания, применимые к пег-интерферону и рибавирину, относятся и к симепревиру, поскольку их необходимо использовать в комбинации во время лечения ХГС. Например, людям с серповидно-клеточной анемией противопоказана терапия рибавирином и, следовательно, им противопоказана комбинированная терапия симепревиром и пег-интерфероном. [13] Беременным женщинам и мужчинам, партнерши которых беременны, прием симепревира противопоказан, поскольку известно, что пег-ИФН и рибавирин вызывают врожденные дефекты. [11] [13] [14]
Беременность
[ редактировать ]Симепревир избегают беременных женщин или женщин, планирующих беременность, поскольку его будут принимать вместе с рибавирином и пег-интерфероном, которые, как было показано в исследованиях на животных, вызывают проблемы у плода. [11] [13] [14] В исследованиях на животных было показано, что рибавирин вызывает врожденные дефекты и гибель плода. [13] В исследованиях на животных было показано, что пег-ИФН вызывает аборты. [14] Перед началом терапии пациенты должны иметь отрицательный тест на беременность, использовать как минимум два эффективных метода контроля над рождаемостью во время лечения и ежемесячно проходить тесты на беременность. [11] Если беременные женщины принимают какие-либо препараты, содержащие рибавирин, им рекомендуется сообщить об этом через реестр беременных, использующих рибавирин. [13]
Побочные эффекты
[ редактировать ]Сильный зуд (22%), чувствительность к солнечному свету (5%) и сыпь (25%) являются одними из частых побочных эффектов симепревира. [15] Другие побочные эффекты могут включать тошноту, мышечные боли , затруднение дыхания и повышение билирубина . [16] Он может реактивировать гепатит B у тех, кто ранее был инфицирован. [17] Европейское агентство лекарственных средств (EMA) рекомендовало проверять всех людей на гепатит В перед началом приема симепревира на гепатит С, чтобы свести к минимуму риск реактивации гепатита В. [18]
Комбинированное лечение
[ редактировать ]В марте 2015 года компания Gilead Sciences разослала поставщикам медицинских услуг по электронной почте предупреждения о том, что у девяти человек, которые начали принимать лекарства от гепатита С, ледипасвир/софосбувир или софосбувир вместе с амиодароном , даклатасвиром или симепревиром, развилось аномально замедленное сердцебиение, а один умер от остановки сердца . Троим потребовалось кардиостимулятор установить . В компании Gilead заявили, что такие комбинации не рекомендуются, и этикетки продуктов будут обновлены. [19]
Механизм действия
[ редактировать ]Симепревир – вируса гепатита ингибитор протеазы С. [20]
Симепревир является ингибитором протеазы NS3/4A, что предотвращает созревание вируса за счет ингибирования синтеза белка. Симепревир назначают по одной капсуле один раз в день вместе с пегилированным интерфероном и рибавирином для лечения хронического гепатита С генотипа 1 или генотипа 4 у взрослых людей с компенсированным заболеванием печени (включая цирроз), с коинфекцией ВИЧ-1 или без нее, которые проходят лечение. наивные или те, у кого предыдущая терапия интерфероном оказалась неудачной. [21] [22] Генотип 1 является наиболее распространенной формой вируса гепатита С (ВГС) во всем мире. [ нужна ссылка ]
Фармакокинетика
[ редактировать ]Симепревир биодоступен при пероральном приеме. Его абсорбция увеличивается при приеме с пищей, поэтому его рекомендуется принимать во время еды. [11] Ферменты печени CYP3A4 в основном расщепляют симепревир, но ферменты CYP2C8 и CYP2C19 также могут играть определенную роль. [11] Период его полувыведения из плазмы у людей с ВГС составляет 41 час. [11] Максимальный эффект достигается через 4–6 часов после приема лекарства. [11] Выводится преимущественно с калом (91%). [11]
Фармакогеномика
[ редактировать ]Согласно информации, назначающей симепревир, его эффективность в сочетании с пегинтерфероном альфа и рибавирином «существенно снижается у людей с генотипом 1а ВГС с полиморфизмом Q80K NS3 на исходном уровне по сравнению с людьми, инфицированными генотипом 1а ВГС без полиморфизма Q80K». [11] Людям с полиморфизмом Q80K не рекомендуется принимать симепревир. [11]
Взаимодействие с лекарственными средствами
[ редактировать ]Симепревир является субстратом CYP3A4, поэтому его концентрация в плазме значительно увеличивается при приеме с препаратами, являющимися сильными ингибиторами CYP3A4 (например, эритромицин , ритонавир ), и значительно снижается при приеме с сильными индукторами CYP3A4 (например , эфавиренз , рифампицин , зверобой ). [11] Симепревир также ингибирует кишечный (но не печеночный) CYP3A. Например, мидазолам , противосудорожное средство, метаболизируется кишечными CYP3A, и его прием с симепревиром может привести к повышению уровня мидазолама, что может быть токсичным. [11] Симепревир также ингибирует транспортеры OATP1B1/3 и P-гликопротеина (P-gp), которые обычно являются транспортерами, выкачивающими лекарственное средство из плазмы. [11] [23] Таким образом, прием симепревира с препаратами, являющимися субстратами этих переносчиков, может привести к повышению концентрации этих препаратов в плазме. Например, блокаторы кальциевых каналов (например, дилтиазем , амлодипин ) являются субстратами P-gp и могут приводить к повышению концентрации этих препаратов при приеме с симепревиром. [11] Прием циклоспорина , субстрата OATP1B1/3, с симепревиром привел к значительному повышению концентрации циклоспорина, поэтому их не рекомендуется принимать вместе. [11]
Одобрение
[ редактировать ]В США он одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для использования в сочетании с пегинтерфероном-альфа и рибавирином при гепатите С. [24] Симепревир одобрен в Японии для лечения хронического гепатита С генотипа 1. [25]
Клиническое исследование
[ редактировать ]Симепревир тестировался в комбинированных схемах с пегилированным интерфероном альфа-2а и рибавирином . [26] и в схемах без интерферона с другими противовирусными препаратами прямого действия, включая даклатасвир. [27] и софосбувир . [28]
Результаты трех рандомизированных двойных слепых плацебо-контролируемых клинических исследований фазы 3 (C208, C216 и HPC3007) у людей с хроническим гепатитом С GT1 были благоприятными и привели к тому, что FDA поддержало одобрение симепревира для лечения гепатита С генотипа 1. [15] После презентации компании Johnson & Johnson (24 октября 2013 г.) члены FDA отметили, что необходимы постмаркетинговые исследования среди расовых и этнических меньшинств, людей с коинфекцией ВИЧ и других недостаточно представленных групп населения. [ нужна ссылка ]
Исследование SARS-CoV-2
[ редактировать ]В нескольких исследованиях проверялось, может ли виростатический механизм одобренных FDA препаратов прямого действия, включая симепревир в сочетании с ремдесивиром (действующий препарат во время эпидемии Эболы в 2014–2016 гг.), быть полезным в борьбе с глобальной пандемией SARS-Cov-Cov. 2. Паритапревир , еще одна молекула, используемая для лечения гепатита С , также показала многообещающие результаты с точки зрения энергии связывания и стабильности образующегося комплекса. [29]
Преимущество работы с такими соединениями заключается в том, что они уже являются противовирусными препаратами, одобренными FDA, а это означает, что фазы клинических испытаний можно начать быстрее. Скорость медицинской помощи является важнейшим фактором, влияющим на глобальные последствия пандемии; чем быстрее в больших масштабах появятся противоядия, такие как лекарства и/или вакцины, тем более перспективными будут сдерживание болезни и ее (экономических) последствий. Скорость является решающим фактором, особенно в борьбе с вирусами, которые по своей природе имеют чрезвычайно высокую скорость мутаций . [ нужна ссылка ]
В отношении SARS-CoV-2 симепревир действует путем ингибирования основной протеазы (Mpro) и РНК -зависимой РНК- полимеразы , неструктурного белка , необходимого для синтеза вирусной РНК. [29]
Mpro принадлежит к тому же классу ферментов, что и NS3/4A, сериновые протеазы . Он расщепляет транслируемый полипротеин с образованием белков, необходимых для транскрипции и репликации вируса . Ремдесивир сам по себе ингибирует только саму полимеразу; Чтобы остановить синтез вируса, также вводят одобренный препарат против гепатита С , чтобы остановить распространение вируса. [29]
In vitro вирусная инфекция Sars-CoV-2 может быть остановлена, и, кроме того, можно наблюдать, что дальнейшие протеазы вируса ингибируются, и, таким образом, эффект противовирусного препарата может быть усилен. В связи с этим в настоящее время все еще отсутствуют клинические исследования, доказывающие эффективность воздействия на организм, которые необходимы перед использованием комбинации препаратов в больших масштабах в качестве формы терапии против инфекции Sars-CoV-2. [ нужна ссылка ]
Препараты от гепатита считаются потенциальными ингибиторами Mpro SARS-CoV-2 в борьбе с инфекцией COVID-19 , а аффинность связывания и ее механизм, а также стабильность образующихся таким образом комплексов могут служить ориентиром или даже шаблон, когда дело доходит до разработки ингибиторов, специально нацеленных на этот вирус. Сами соединения также могут играть важную роль и должны быть дополнительно изучены в клинических испытаниях . [ нужна ссылка ]
Ссылки
[ редактировать ]- ^ «Лекарства, отпускаемые по рецепту: регистрация новых химических веществ в Австралии, 2014 г.» . Управление терапевтических товаров (TGA) . 21 июня 2022 г. Проверено 10 апреля 2023 г.
- ^ Перейти обратно: а б с д и ж г час я дж «Симепревир» . Американское общество фармацевтов системы здравоохранения. Архивировано из оригинала 1 декабря 2016 года . Проверено 30 ноября 2016 г. .
- ^ «Первичное лечение HCV-инфекции» . www.hcvguidelines.org . Октябрь 2016. Архивировано из оригинала 7 декабря 2016 года . Проверено 1 декабря 2016 г.
- ^ Маджумдар А., Китсон М.Т., Робертс С.К. (июнь 2016 г.). «Систематический обзор: современные концепции и проблемы эры противовирусных препаратов прямого действия при циррозе печени гепатита С» . Алиментарная фармакология и терапия . 43 (12): 1276–92. дои : 10.1111/кв.13633 . ПМИД 27087015 .
- ^ Брошо Э., Хелле Ф., Франсуа К., Кастелен С., Капрон Д., Нгуен-Хак Э., Дюверли Дж. (апрель 2015 г.). «Какой вариант лечения вируса гепатита С генотипа 1?». Скандинавский журнал гастроэнтерологии . 50 (4): 470–8. дои : 10.3109/00365521.2014.978364 . ПМИД 25396710 . S2CID 34382861 .
- ^ Перейти обратно: а б Гамильтон Р. (2015). Карманная фармакопея Тараскон, издание Deluxe Lab-Coat, 2015 г. Джонс и Бартлетт Обучение. п. 80. ИСБН 9781284057560 .
- ^ Граббс Р.Х., О'Лири диджей (2015). Справочник по метатезису, том 2: Применение в органическом синтезе . Джон Уайли и сыновья. п. 699. ИСБН 9783527694020 .
- ^ Дугам М., О'Ши Р. (март 2014 г.). «Вирус гепатита С: вот и полностью пероральное лечение» . Медицинский журнал Кливлендской клиники . 81 (3): 159–72. дои : 10.3949/ccjm.81a.13155 . ПМИД 24591471 . S2CID 37838853 .
- ^ Всемирная организация здравоохранения (2019). Резюме: выбор и использование основных лекарств 2019: доклад 22-го заседания Экспертного комитета ВОЗ по выбору и использованию основных лекарств . Женева: Всемирная организация здравоохранения. hdl : 10665/325773 . ВОЗ/MVP/EMP/IAU/2019.05. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ Всемирная организация здравоохранения (2019). Выбор и использование основных лекарственных средств: доклад Комитета экспертов ВОЗ по выбору и использованию основных лекарственных средств, 2019 г. (включая 21-й Примерный список ВОЗ основных лекарственных средств и 7-й Примерный список ВОЗ основных лекарственных средств для детей) . Женева: Всемирная организация здравоохранения. hdl : 10665/330668 . ISBN 9789241210300 . ISSN 0512-3054 . Серия технических докладов ВОЗ;1021.
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В «ОЛИСИО (симепревир) капсулы для перорального применения ПОЛНАЯ ИНФОРМАЦИЯ ПО ПРЕДПИСЫВАНИЮ» . Сентябрь 2014 года . Проверено 24 октября 2014 г. [ постоянная мертвая ссылка ]
- ^ «Рекомендации по тестированию, ведению и лечению гепатита С» . 2014. Архивировано из оригинала 16 октября 2014 года . Проверено 24 октября 2014 г.
- ^ Перейти обратно: а б с д и «Основные сведения о назначениях Copegus» (PDF) . Август 2011 г. Архивировано (PDF) из оригинала 3 ноября 2014 г. Проверено 24 октября 2014 г.
- ^ Перейти обратно: а б с «Основная информация о назначении ПЕГИНТРОНА» (PDF) . Июль 2014 г. Архивировано (PDF) из оригинала 3 ноября 2014 г. Проверено 24 октября 2014 г.
- ^ Перейти обратно: а б «ЗАСЕДАНИЕ КОНСУЛЬТАТИВНОГО КОМИТЕТА FDA ПО ПРОТИВОВИРУСНЫМ ПРЕПАРАТАМ» (PDF) . Управление по контролю за продуктами и лекарствами . Октябрь 2013 г. Архивировано (PDF) из оригинала 26 декабря 2014 г. Проверено 24 октября 2014 г.
- ^ «Дозировка Олизио (симепревира), показания, взаимодействие, побочные эффекты и многое другое» . ссылка.medscape.com . Архивировано из оригинала 10 ноября 2016 года . Проверено 10 ноября 2016 г. .
- ^ «Противовирусные препараты прямого действия при гепатите С: информация о безопасности лекарств – риск реактивации гепатита В» . FDA . 4 октября 2016 года. Архивировано из оригинала 6 октября 2016 года . Проверено 6 октября 2016 г.
- ^ «Противовирусные препараты прямого действия, показанные для лечения гепатита С (без интерферона)» . Европейское агентство лекарственных средств (EMA) . 17 сентября 2018 года . Проверено 4 февраля 2020 г.
- ^ Уэст, Стивен. «Gilead предупреждает после смерти пациента с гепатитом, принимавшего сердечный препарат». Архивировано 22 марта 2017 г. в Wayback Machine . Опубликовано 21 марта 2015 г.
- ^ Лин Т.И., Ленц О., Фэннинг Г., Вербиннен Т., Делуврой Ф., Шоллерс А. и др. (апрель 2009 г.). «Активность in vitro и доклинический профиль TMC435350, мощного ингибитора протеазы вируса гепатита С» . Антимикробные средства и химиотерапия . 53 (4): 1377–85. дои : 10.1128/AAC.01058-08 . ПМК 2663092 . ПМИД 19171797 .
- ^ Европейская ассоциация по изучению печени (август 2011 г.). «Руководство по клинической практике EASL: ведение инфекции, вызванной вирусом гепатита С» . Журнал гепатологии . 55 (2): 245–64. дои : 10.1016/j.jhep.2011.02.023 . hdl : 10447/88292 . ПМИД 21371579 .
- ^ Зейн Н.Н. (апрель 2000 г.). «Клиническое значение генотипов вируса гепатита С» . Обзоры клинической микробиологии . 13 (2): 223–35. дои : 10.1128/CMR.13.2.223-235.2000 . ПМЦ 100152 . ПМИД 10755999 .
- ^ Фурихата Т., Мацумото С., Фу З., Цубота А., Сунь Ю., Мацумото С. и др. (август 2014 г.). «Различные профили взаимодействия агентов прямого действия против вируса гепатита С с человеческими полипептидами, транспортирующими органические анионы» . Антимикробные средства и химиотерапия . 58 (8): 4555–64. дои : 10.1128/AAC.02724-14 . ПМК 4135986 . ПМИД 24867984 .
- ^ «FDA одобряет новое лечение вируса гепатита С» . Управление по контролю за продуктами и лекарствами . 22 ноября 2013 г. Архивировано из оригинала 16 декабря 2013 г.
- ^ «Медивир: Симепревир был одобрен в Японии для лечения хронического гепатита С генотипа 1» . Уолл-Стрит Джорнал. 27 сентября 2013 г. Архивировано из оригинала 24 ноября 2013 г.
- ^ «Исследования фазы 3 показывают, что симепревир в сочетании с интерфероном/рибавирином излечивает большинство пациентов за 24 недели» . hivandhepatitis.com. 27 декабря 2012 г. Архивировано из оригинала 13 марта 2013 г.
- ^ Medivir объявляет о расширении клинического сотрудничества TMC435 . Медивир. 18 апреля 2012 г.
- ^ Результаты исследования фазы IIa по оценке симепревира и софосбувира у пациентов с гепатитом С, ранее не ответивших на лечение, были представлены в CROI. 6 марта 2013 г. Архивировано 16 октября 2012 г. в Wayback Machine.
- ^ Перейти обратно: а б с Аламри М.А., Тахир Уль Камар М., Мирза М.У., Бхадане Р., Алкахтани С.М., Мунир И. и др. (июнь 2020 г.). «Исследования по моделированию фармакоинформатики и молекулярной динамики выявили потенциальные ковалентные и одобренные FDA ингибиторы основной протеазы 3CL SARS-CoV-2. про « . Журнал биомолекулярной структуры и динамики . 39 (13): 4936–4948. doi : 10.1080/ . PMC 7332866. . PMID 32579061 07391102.2020.1782768
Дальнейшее чтение
[ редактировать ]- Дин Л. (2016). «Терапия симепревиром и генотип IFNL3» . В Пратт В.М., МакЛеод Х.Л., Рубинштейн В.С. и др. (ред.). Краткое изложение медицинской генетики . Национальный центр биотехнологической информации (NCBI). ПМИД 28520373 . Идентификатор книжной полки: NBK385156.
Внешние ссылки
[ редактировать ]- «Симепревир» . Информационный портал о наркотиках . Национальная медицинская библиотека США.