Хигенамин
Эта статья нуждается в более надежных медицинских ссылках для проверки или слишком сильно полагается на первоисточники . ( декабрь 2018 г. ) |  |
 | |
| Имена | |
|---|---|
| Название ИЮПАК 1-[(4-Гидроксифенил)метил]-1,2,3,4-тетрагидроизохинолин-6,7-диол | |
| Другие имена норкоклаурин, деметилклаурин | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| КЕГГ | |
| МеШ | хигенамин |
ПабХим CID | |
| НЕКОТОРЫЙ |
|
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 16 Н 17 Н О 3 | |
| Молярная масса | 271.316 g·mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Хигенамин ( норкоклаурин ) представляет собой химическое соединение, обнаруженное во многих растениях, включая Nandina Domestica (плоды), Aconitum carmichaelii (корень), Asarum гетеротропиоиды , Galium divaricatum (стебель и виноградная лоза), Annona sqamosa и Nelumbo nucifera (семена лотоса).
Хигенамин содержится в пищевых добавках для спорта и похудения, продаваемых в США. [1] Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США получает сообщения о побочных эффектах добавок, содержащих хигенамин, с 2014 года, но риски для здоровья, связанные с хигенамином, остаются плохо изученными. [1]
Законность
[ редактировать ]Хигенамин, также известный как норкоклаурин HCl , разрешен к использованию в пищевых добавках в Великобритании , ЕС , США и Канаде . Его основное применение — пищевые добавки, разработанные для контроля веса, и спортивные добавки. [1] Традиционные препараты с хигенамином использовались в китайской медицине на протяжении тысячелетий и получены из различных источников, включая фрукты и орхидеи. Исследований, сравнивающих безопасность современных препаратов (на основе синтетического хигенамина) с традиционными, нет. Тем не менее, он не будет добавлен в каталог «новых пищевых продуктов» ЕС, в котором подробно описаны все пищевые добавки, перед использованием которых требуется сертификат оценки безопасности. [2]
как и многие другие β2 Хигенамин , агонисты , запрещен Всемирным антидопинговым агентством для использования в спорте. [3] В 2016 году французский футболист Мамаду Сако был временно дисквалифицирован УЕФА после положительного результата теста на хигенамин, из-за которого игрок пропустил финал Лиги Европы 2016 года. Запрет был снят после того, как игрок успешно представил смягчающую аргументацию в пользу отсутствия серьезной халатности, поскольку вещество не было в списке запрещенных веществ, несмотря на то, что препараты той же категории - агонисты β 2 - были запрещены. [4] [5] [6] [7]
Фармакология
[ редактировать ]Поскольку хигенамин присутствует в растениях, которые уже давно используются в традиционной медицине , фармакология этого соединения вызвала научный интерес.
На животных моделях было показано, что хигенамин является агонистом β2 - адренорецепторов . [8] [9] [10] [11] [12] Адренергические рецепторы, или адренорецепторы, относятся к классу рецепторов, связанных с G-белком , и являются наиболее заметными рецепторами в жировой мембране, а также экспрессируются в ткани скелетных мышц. Эти рецепторы жировой мембраны классифицируются как α- или β-адренорецепторы. Хотя эти адренорецепторы имеют один и тот же посредник — циклический аденозинмонофосфат (цАМФ), конкретный путь трансдукции зависит от типа рецептора (α или β). Хигенамин частично оказывает свое действие за счет активации фермента аденилатциклазы , ответственного за повышение клеточной концентрации вторичного адренергического мессенджера цАМФ. [13]
На модели грызунов было обнаружено, что хигенамин оказывает кардиотоническое , сосудистое расслабление и бронхолитическое действие. [14] [15] В частности, хигенамин через механизм бета-адренорецепторов вызывал расслабление кавернозных тел крыс , что приводило к улучшению вазодилатации и эректильной функции.
На животных моделях было показано, что хигенамин, связанный с улучшением сигналов расширения сосудов, обладает антиагрегантной и антитромботической активностью посредством цАМФ-зависимого пути, что позволяет предположить, что хигенамин может способствовать усилению вазодилатации и целостности артерий. [8] [13] [15] [16]
На людях хигенамин изучался в качестве исследуемого препарата в Китае для использования в качестве фармакологического средства при сердечных стресс-тестах, а также для лечения ряда сердечных заболеваний, включая брадиаритмии. [1] Испытания на людях были относительно небольшими (от 10 до 120 субъектов), и хигенамин вводили внутривенно, чаще всего с использованием постепенной инфузии по 2,5 или 5 мг. [1] Хигенамин постоянно увеличивал частоту сердечных сокращений, но имел переменное влияние на артериальное давление. В одном небольшом исследовании описано влияние хигенамина на сердечный выброс: хигенамин привел к увеличению фракции выброса у 15 пациентов с заболеваниями сердца. [1]
Токсичность
[ редактировать ]Безопасность перорального применения хигенамина у людей неизвестна. Во время исследования острой токсичности мышам перорально вводили соединение в дозе 2 г на кг массы тела. За время исследования ни одна мышь не погибла. [17] В ходе испытаний внутривенного введения хигенамина на людях субъекты, получавшие хигенамин, сообщали об одышке, учащенном сердцебиении, головокружении, головных болях, стеснении в груди. [1]
Биосинтез
[ редактировать ](S)-норкоклаурин/хигенамин находится в центре биосинтеза алкалоида бензилизохинолина (BIA). Несмотря на большое структурное разнообразие, все биосинтезы BIA имеют общий первый коммитированный промежуточный продукт (S) - норкоклаурин. [18] (S)-норкоклаурин получают путем конденсации двух производных тирозина, дофамина и 4-гидроксифенилацетальдегида (4-ГПАА).
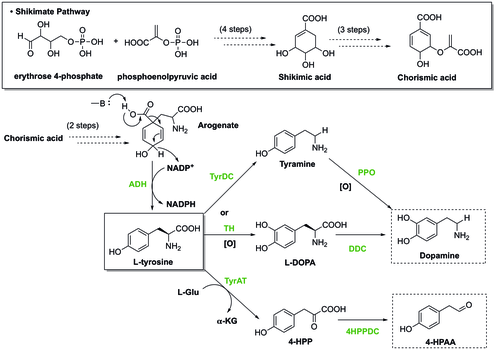
В растениях тирозин синтезируется по шикиматному пути , последний этап которого включает декарбоксилирование и дегидрирование арогената с образованием L-тирозина . Для выработки дофамина из тирозина существует два пути. В одном из путей тирозин подвергается декарбоксилированию, катализируемому тирозиндекарбоксилазой (TyrDC), с образованием тирамина, за которым затем следует окисление полифенолоксидазой (PPO) с образованием дофамина. [19] [20] Альтернативно, тирозин может быть окислен тирозингидроксилазой (TH) с образованием L-ДОФА , который затем позже декарбоксилируется с помощью ДОФА-декарбоксилазы (ДДК) с образованием дофамина. Кроме того, другой исходный материал, 4-HPAA, образуется в результате первого трансаминирования тирозинтрансэаминазой (TyrAT) с образованием 4-гидроксифенилпирувата (4-HPP) и последующего декарбоксилирования декарбоксилазой 4-HPP. [20]
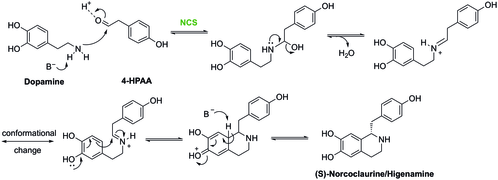
Конденсация дофамина и 4-ГФАА с образованием (S)-норкоклаурина катализируется (S)-норкоклауринсинтазой (NCS). [21] Такая реакция является одним из типов реакции Пикте-Шпенглера . В этой реакции Asp-141 и Glu-110 в активном центре NCS участвуют в активации амина и карбонила соответственно, чтобы облегчить образование имина. Затем молекула будет циклизироваться по механизму, показанному ниже, с образованием (S)-нококлаурина.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г Коэн, Питер А.; Трэвис, Джон К.; Кайзерс, Питер Х.Дж.; Бойер, Фредерик Э.; Венхейс, Бастиан Дж. (6 сентября 2018 г.). «Стимулятор хигенамин в средствах для похудения и спортивных добавках». Клиническая токсикология . 57 (2): 125–130. дои : 10.1080/15563650.2018.1497171 . ПМИД 30188222 . S2CID 52165506 .
- ^ «Каталог новых продуктов питания» . Безопасность пищевых продуктов . Европейская комиссия.
- ^ «Запрещенные вещества во все времена» . Список запрещенных веществ и методов . Всемирное антидопинговое агентство. 1 января 2016 года . Проверено 21 августа 2016 г.
- ^ «Мамаду Сако: защитник «Ливерпуля» расследуется по поводу проваленного теста на допинг» . Би-би-си . 23 апреля 2016 г.
- ^ «Евро-2016: Мамаду Сако может сыграть за Францию, поскольку УЕФА предпочитает не продлевать дисквалификацию» . Би-би-си . 28 мая 2016 г.
- ^ «Мамаду Сахо: Решение УЕФА вызывает ключевые вопросы» . Эхо . 28 мая 2016 г.
- ^ «Мамаду Сахо все равно пропустит ЕВРО-2016, несмотря на то, что с него снят допинг» . Получите французский футбол . 29 мая 2016 г.
- ^ Jump up to: а б Цукияма М, Уэки Т, Ясуда Ю, Кикучи Х, Акаиси Т, Окумура Х, Абэ К (октябрь 2009 г.). «Релаксация трахеи, опосредованная бета2-адренорецепторами, вызванная хигенамином из Нандины домашней Тунберга». Планта Медика . 75 (13): 1393–9. дои : 10.1055/s-0029-1185743 . ПМИД 19468973 . S2CID 260280804 .
- ^ Кашивада Ю., Аошима А., Икеширо Ю., Чен Ю.П., Фурукава Х., Итоигава М., Фудзиока Т., Михаши К., Косентино Л.М., Моррис-Натшке С.Л., Ли К.Х. (январь 2005 г.). «Анти-ВИЧ бензилизохинолиновые алкалоиды и флавоноиды из листьев Nelumbo nucifera и корреляции структура-активность с родственными алкалоидами». Биоорганическая и медицинская химия . 13 (2): 443–8. дои : 10.1016/j.bmc.2004.10.020 . ПМИД 15598565 .
- ^ Кимура И, Чуй Л.Х., Фуджитани К., Кикучи Т., Кимура М. (май 1989 г.). «Инотропные эффекты (+/-)-хигенамина и его химически родственных компонентов, (+)-R-коклаурина и (+)-S-ретикулина, содержащихся в традиционных китайско-японских лекарствах «буси» и «син-и» в изолированной сосочковой мышце морской свинки» . Японский журнал фармакологии . 50 (1): 75–8. дои : 10.1254/jjp.50.75 . ПМИД 2724702 .
- ^ Кан Ю.Дж., Ли Ю.С., Ли Г.В., Ли Д.Х., Рю Дж.К., Юн-Чой Х.С., Чанг К.С. (октябрь 1999 г.). «Подавление активации ядерного фактора каппаВ отвечает за ингибирование индуцибельной экспрессии синтазы оксида азота хигенамином, активным компонентом корня аконита». Журнал фармакологии и экспериментальной терапии . 291 (1): 314–20. ПМИД 10490919 .
- ^ Юн-Чой Х.С., Пё М.К., Пак К.М., Чанг К.С., Ли Д.Х. (октябрь 2001 г.). «Антитромботические эффекты хигенамина». Планта Медика . 67 (7): 619–22. дои : 10.1055/s-2001-17361 . ПМИД 11582538 . S2CID 260279615 .
- ^ Jump up to: а б Кам С.К., До Дж.М., Чхве Дж.Х., Чон Б.Т., Ро Г.С., Чанг К.С., Хён Дж.С. (2012). «Эффект релаксации и механизм действия хигенамина в кавернозных телах крыс» . Международный журнал исследований импотенции . 24 (2): 77–83. дои : 10.1038/ijir.2011.48 . ПМИД 21956762 .
- ^ Бай Г, Ян Ю, Ши Ц, Лю Цз, Чжан Ц, Чжу Ю (октябрь 2008 г.). «Идентификация хигенамина в препарате Radix Aconiti Lateralis как агониста бета2-адренергических рецепторов1» . Акта Фармакологика Синика . 29 (10): 1187–94. дои : 10.1111/j.1745-7254.2008.00859.x . ПМИД 18817623 .
- ^ Jump up to: а б Пё М.К., Ли Д.Х., Ким Д.Х., Ли Дж.Х., Мун Дж.К., Чанг К.С., Юн-Чой Х.С. (июль 2008 г.). «Энантиоселективный синтез (R)-(+)- и (S)-(-)-хигенамина и их аналогов с воздействием на агрегацию тромбоцитов и экспериментальная животная модель диссеминированного внутрисосудистого свертывания». Письма по биоорганической и медицинской химии . 18 (14): 4110–4. дои : 10.1016/j.bmcl.2008.05.094 . ПМИД 18556200 .
- ^ Лю В., Сато Ю., Хосода Ю., Хирасава К., Ханаи Х. (ноябрь 2000 г.). «Влияние хигенамина на регуляцию транспорта ионов в дистальном отделе толстой кишки морской свинки» . Японский журнал фармакологии . 84 (3): 244–51. дои : 10.1254/jjp.84.244 . ПМИД 11138724 .
- ^ Ло CF, Чен CM (февраль 1997 г.). «Острая токсичность хигенамина у мышей». Планта Медика . 63 (1): 95–6. дои : 10.1055/s-2006-957619 . ПМИД 9063102 . S2CID 260281301 .
- ^ Хейгел Дж. М., Факкини П. Дж. (май 2013 г.). «Метаболизм бензилизохинолиновых алкалоидов: век открытий и дивный новый мир» . Физиология растений и клеток . 54 (5): 647–72. дои : 10.1093/pcp/pct020 . ПМИД 23385146 .
- ^ Соарес А.Р., Маркиози Р., Сикейра-Соареш Р.К., Барбоза де Лима Р., Маркиози Р., Дантас душ Сантос В., Феррарезе-Филью О (март 2014 г.). «Роль L-ДОФА в растениях» . Сигнализация и поведение растений . 9 (4): e28275. дои : 10.4161/psb.28275 . ПМК 4091518 . ПМИД 24598311 .
- ^ Jump up to: а б Бодуэн Г.А., Факкини П.Дж. (июль 2014 г.). «Биосинтез бензилизохинолинового алкалоида в опийном маке» . Планта . 240 (1): 19–32. дои : 10.1007/s00425-014-2056-8 . ПМИД 24671624 .
- ^ Личман Б.Р., Сула А., Песно Т., Хейлз ХК, Уорд Дж.М., Keep NH (октябрь 2017 г.). «Структурные доказательства дофаминового механизма норкоклауринсинтазы» . Биохимия . 56 (40): 5274–5277. doi : 10.1021/acs.biochem.7b00769 . ПМК 5637010 . ПМИД 28915025 .