Фенилпропаноламин
Фенилпропаноламин ( PPA ), продаваемый под многими торговыми марками, представляет собой симпатомиметическое средство , которое используется как противозастойное средство и средство для подавления аппетита . [9] [1] [10] [11] Ранее он широко использовался в рецептурных и безрецептурных препаратах от кашля и простуды . Лекарство принимают внутрь . [4] [12]
Побочные эффекты PPA включают, среди прочего, увеличение частоты сердечных сокращений и артериального давления . [13] [14] [15] [12] В редких случаях ППА ассоциировался с геморрагическим инсультом . [11] [16] [13] PPA действует как агент, высвобождающий норадреналин , тем самым косвенно активируя адренергические рецепторы . [17] [18] [19] Таким образом, это симпатомиметик косвенного действия . [17] [18] [19] [10] Ранее считалось, что он действует как симпатомиметик смешанного действия с дополнительным прямым агонистическим действием на адренергические рецепторы, но это оказалось не так. [17] [18] [19] По химическому составу PPA представляет собой замещенный амфетамин и тесно связан с эфедрином , псевдоэфедрином , амфетамином и катиноном . [20] [21] [22] [11]
PPA был впервые синтезирован около 1910 года, а его влияние на артериальное давление впервые было охарактеризовано около 1930 года. [21] [11] Он был введен в медицинское использование в 1930-х годах. [23] [11] Препарат был снят с продажи на многих рынках, начиная с 2000 года, после того, как было обнаружено, что оно связано с повышенным риском геморрагического инсульта. [23] [11] Раньше его можно было купить как без рецепта, так и по рецепту . [23] [2] [24] [25] PPA по-прежнему доступен для медицинского и/или ветеринарного использования в некоторых странах. [2]
Медицинское использование
[ редактировать ]PPA используется как противоотечное средство для лечения заложенности носа . [13] [14] Он также использовался для подавления аппетита и снижения веса при лечении ожирения и показал эффективность по этому показанию. [26] [27] [28]
Доступные формы
[ редактировать ]Ранее PPA был доступен без рецепта и в некоторых комбинированных формах по рецепту в США . [24] [25] Однако все эти формы были прекращены. [24] [25] [2] PPA по-прежнему доступен в некоторых других странах. [2]
Побочные эффекты
[ редактировать ]PPA оказывает симпатомиметическое действие и может вызывать побочные эффекты, такие как увеличение частоты сердечных сокращений и артериального давления . [13] [14] [15] [12] Это редко ассоциировалось с частотой геморрагического инсульта . [23] [16] [13]
Некоторые наркотики увеличивают вероятность возникновения дежавю у потребителя, что приводит к сильному ощущению того, что событие или опыт, переживаемый в данный момент, уже переживались в прошлом. Некоторые фармацевтические препараты, взятые вместе, также могут быть причиной дежавю . [29] сообщили о случае, когда здоровый мужчина начал испытывать сильные и периодические ощущения дежавю после совместного приема препаратов амантадина и PPA для облегчения симптомов гриппа. Этот опыт показался ему настолько интересным, что он прошел полный курс лечения и сообщил о нем психологам, чтобы они описали его в качестве примера. Из-за дофаминергического действия препаратов и предыдущих результатов электродной стимуляции мозга, [30] Было высказано предположение, что дежавю возникает в результате гипердофаминергического действия в мезиальных височных областях мозга.
Взаимодействия
[ редактировать ]Было проведено очень мало исследований по взаимодействию лекарств с PPA. [4] В одном исследовании было обнаружено, что PPA, принимаемый с кофеином, увеличивает уровень кофеина в четыре раза. [4] В другом исследовании PPA снижал теофиллина клиренс на 50%. [4]
Фармакология
[ редактировать ]Фармакодинамика
[ редактировать ]PPA действует главным образом как селективный агент, высвобождающий норадреналин . [19] Он также действует как агент, высвобождающий дофамин , с примерно в 10 раз меньшей эффективностью . [19] Стереоизомеры препарата обладают слабым или незначительным сродством к α- и β-адренергическим рецепторам . [19]
| Сложный | NE | Подсказка DA | 5-HT | Ссылка | ||
|---|---|---|---|---|---|---|
| Декстроамфетамин ( S (+)-амфетамин) | 6.6–7.2 | 5.8–24.8 | 698–1765 | [32] [33] | ||
| S (–)-Катинон | 12.4 | 18.5 | 2366 | [19] | ||
| (-)-Эфедрин | 43.1–72.4 | 236–1350 | >10000 | [32] | ||
| (+)-Эфедрин | 218 | 2104 | >10000 | [32] [19] | ||
| Декстрометамфетамин ( S (+)-метамфетамин) | 12.3–13.8 | 8.5–24.5 | 736–1291.7 | [32] [34] | ||
| Левометамфетамин ( R (–)-метамфетамин) | 28.5 | 416 | 4640 | [32] | ||
| (+)-Фенилпропаноламин ((+)-норэфедрин) | 42.1 | 302 | >10000 | [19] | ||
| (–)-Фенилпропаноламин ((–)-норэфедрин) | 137 | 1371 | >10000 | [19] | ||
| Катин ((+)-норпсевдоэфедрин) | 15.0 | 68.3 | >10000 | [19] | ||
| (–)-норпсевдоэфедрин | 30.1 | 294 | >10000 | [19] | ||
| (–)-Псевдоэфедрин | 4092 | 9125 | >10000 | [19] | ||
| Псевдоэфедрин ((+)-псевдоэфедрин) | 224 | 1988 | >10000 | [19] | ||
| Чем меньше значение, тем сильнее вещество высвобождает нейромедиатор. См. также § Профили активности агента, высвобождающего моноамины, для получения более крупной таблицы с большим количеством соединений. | ||||||
Первоначально считалось, что PPA действует как прямой агонист адренергических рецепторов и, следовательно, действует как симпатомиметик смешанного действия . [21] [22] Однако впоследствии было обнаружено, что PPA проявляет лишь слабое или незначительное сродство к этим рецепторам и вместо этого был охарактеризован как симпатомиметик исключительно косвенного действия. [10] [17] [18] [19] Он действует, вызывая высвобождение норадреналина и тем самым косвенно активируя адренергические рецепторы. [17] [18] [19]
Многие симпатические гормоны и нейротрансмиттеры основаны на фенэтиламиновом скелете и обычно функционируют в реакциях типа «бей или беги», таких как увеличение частоты сердечных сокращений, артериального давления, расширение зрачков, увеличение энергии, высыхание слизистых оболочек, повышенное потоотделение и значительное количество дополнительных эффектов. [ нужна ссылка ]
PPA имеет относительно низкую эффективность как симпатомиметик. [21] По своим симпатомиметическим эффектам он примерно в 100–200 раз менее эффективен, чем адреналин (адреналин) или норэпинефрин (норадреналин), хотя реакции варьируются в зависимости от ткани . [21]
Фармакокинетика
[ редактировать ]Поглощение
[ редактировать ]PPA легко и хорошо всасывается при пероральном приеме . [6] [7] [5] с немедленным высвобождением Формы препарата достигают пиковых уровней примерно через 1,5 часа (диапазон от 1,0 до 2,3 часа) после приема. [4] [7] И наоборот, формы пролонгированного действия PPA достигают пиковых уровней через 3,0–4,5 часа. [4] Фармакокинетика мг PPA линейна в диапазоне пероральных доз от 25 до 100 . [4] Устойчивый уровень PPA достигается в течение 12 часов при приеме препарата один раз в 4 часа. [4] В устойчивом состоянии наблюдается накопление PPA на 62% с точки зрения пиковых уровней, тогда как уровни площади под кривой не увеличиваются в устойчивом состоянии. [4]
Распределение
[ редактировать ]Объем распределения ППА составляет 3,0–4,5 л/кг. [4] Уровни PPA в мозге составляют около 40% от показателей в сердце и 20% от показателей в легких . [6] Гидроксильная группа PPA у β-углерода увеличивает его гидрофильность , уменьшает его проникновение через гематоэнцефалический барьер и ограничивает его воздействие на центральную нервную систему (ЦНС). [6] Следовательно, PPA проникает в мозг лишь в некоторой степени, оказывает лишь слабое воздействие на ЦНС, и большинство его эффектов являются периферическими. [14] [6] [5] [21] В любом случае, PPA может оказывать амфетамину действие , подобное психостимулирующее , в очень высоких дозах. [21] [6] [5] PPA более липофильен, чем структурно родственные симпатомиметики с гидроксильными группами в фенильном кольце , такие как адреналин (адреналин) и фенилэфрин , и обладает большей проницаемостью для мозга, чем эти агенты. [5] [22]
Связывание PPA с белками плазмы составляет примерно 20%. [5] [4] Однако было сказано, что никакие недавние исследования не подтвердили эту ценность. [4]
Метаболизм
[ редактировать ]PPA практически не метаболизируется . [7] [5] Он также не подвергается значительному метаболизму первого прохождения . [7] Метаболизируется только около 3–4% пероральной дозы PPA. [5] Метаболиты включают гиппуровую кислоту (путем окислительного дезаминирования боковой цепи ) и 4-гидроксинорэфедрин (путем пара - гидроксилирования ). [4] [5] [6] Метильная группа α-углерода ППА блокирует метаболизм моноаминоксидазами (МАО). [6] [5] [14] PPA также не является субстратом катехол - О -метилтрансферазы . [14] Гидроксильная группа у β-углерода PPA также помогает повысить метаболическую стабильность . [5]
Устранение
[ редактировать ]Примерно 90% дозы ППА выводится с мочой в неизмененном виде в течение 24 часов. [4] [6] [7] [5] [4] Около 4% выведенного материала находится в форме метаболитов . [4]
Период полувыведения PPA с немедленным высвобождением составляет около 4 часов, а в различных исследованиях он варьируется от 3,7 до 4,9 часов. [6] [7] [4] Период полувыведения PPA пролонгированного действия составляет от 4,3 до 5,8 часов. [4]
Выведение PPA зависит от pH мочи . [4] [5] При более кислом pH мочи выведение PPA ускоряется, а период его полувыведения и продолжительность сокращаются, тогда как при более основном pH мочи выведение PPA замедляется, а период его полувыведения и продолжительность увеличиваются. [5] [4] Агенты, подкисляющие мочу, такие как аскорбиновая кислота и хлорид аммония, могут увеличивать выведение и тем самым снижать воздействие амфетаминов, включая PPA, тогда как агенты, подщелачивающие мочу, включая антациды, такие как бикарбонат натрия , а также ацетазоламид, могут уменьшать выведение этих агентов и тем самым увеличивать воздействие на них. [35] [5] [36]
общий клиренс Сообщается, что PPA из организма составляет 0,546 л/ч/кг, тогда как почечный клиренс составляет 0,432 л/ч/кг. [4]
Разнообразный
[ редактировать ], вероятно, не повлияет на него Поскольку ППА не подвергается интенсивному метаболизму, печеночная недостаточность . [4] И наоборот, вероятно накопление ППА при почечной недостаточности из-за его зависимости от выведения с мочой. [4]
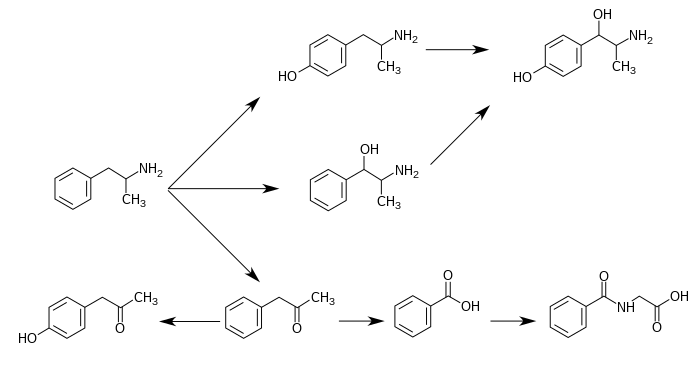
является второстепенным метаболитом амфетамина метамфетамина и Норэфедрин , как показано ниже. [4] Это также второстепенный метаболит эфедрина и основной метаболит катинона . [4] [6] [5]
Метаболические пути амфетамина у человека [источники 1] |
Химия
[ редактировать ]
PPA, также известный как α-метил-β-гидроксифенэтиламин или β-гидроксиамфетамин, представляет собой фенэтиламина и амфетамина замещенное производное . [9] [20] [48] Он тесно связан с катинонами (β-кетоамфетаминами). [20] Соединение существует в виде четырех , которые включают d- ( правовращающий ) и l -норэфедрин ( левовращающий ), а также d- и . l -норпсевдоэфедрин стереоизомеров [48] [10] d -норпсевдоэфедрин также известен как катин . [9] [48] встречается и в природе в Catha edulis ( кат ). [49] Фармацевтические препараты ППА различаются по стереоизомерному составу в разных странах, что может объяснить различия в неправильном использовании и побочных эффектов . профилях [10] В любом случае рацемический дл-норэфедрин, по-видимому, является наиболее часто используемым фармацевтическим составом. [21] [9] [1] Аналоги PPA включают эфедрин , псевдоэфедрин , амфетамин , метамфетамин и катинон . [20]
По своей структуре PPA относится к классу замещенных фенэтиламинов, состоящих из циклической бензольной или фенильной группы, двухуглеродного этильного фрагмента и терминального азота, отсюда и название фенэтиламин . [50] Метильная группа на альфа-углероде (первый атом углерода перед азотистой группой) также делает это соединение членом класса замещенных амфетаминов . [50] Эфедрин является N -метиловым аналогом PPA.
Экзогенные соединения этого семейства слишком быстро разлагаются моноаминоксидазой, чтобы быть активными при любых дозах, кроме самых высоких. [50] Однако добавление α-метиловой группы позволяет соединению избежать метаболизма и оказать эффект. [50] В целом N -метилирование первичных аминов увеличивает их эффективность, тогда как β-гидроксилирование снижает активность ЦНС, но обеспечивает большую селективность в отношении адренергических рецепторов. [50]
ППА представляет собой низкомолекулярное соединение с молекулярной формулой C 9 H 13 NO и молекулярной массой 151,21 г/моль. [51] [8] Его экспериментальный log P равен 0,67, тогда как прогнозируемые значения log P варьируются от 0,57 до 0,89. [51] [8] Соединение относительно липофильно . [5] но он также более гидрофильен, чем другие амфетамины. [6] Липофильность амфетаминов тесно связана с их проницаемостью для мозга. [52] Для сравнения с PPA экспериментальный log P метамфетамина составляет 2,1, [53] амфетамина , – 1,8 [54] [53] эфедрина – 1,1, [55] псевдоэфедрина – 0,7 , [56] фенилэфрина , составляет -0,3 [57] а норадреналина составляет -1,2. [58] Метамфетамин обладает высокой проницаемостью для мозга. [53] тогда как фенилэфрин и норадреналин являются периферически селективными препаратами . [59] [60] Оптимальный log P для проникновения в мозг и центральной активности составляет около 2,1 (диапазон 1,5–2,7). [61]
PPA использовался в фармацевтике исключительно в виде гидрохлоридной соли . [9] [1]
История
[ редактировать ]PPA был впервые синтезирован в начале 20 века, примерно в 1910 году. [21] [11] Он был запатентован как мидриатик в 1913 году. [21] Прессорные . эффекты ППА были охарактеризованы в конце 1920-х — 1930-х годах [21] PPA был впервые использован в медицинских целях в 1930-х годах. [23] [11]
В США ППА больше не продается из-за повышенного риска геморрагического инсульта . [16] Однако в некоторых странах Европы он по-прежнему доступен либо по рецепту, либо иногда без рецепта. В Канаде он был отозван с рынка 31 мая 2001 года. [62] К июлю 2001 года он был добровольно снят с австралийского рынка. [63] В Индии использование человеком PPA и его составов было запрещено 10 февраля 2011 года. [64] но запрет был отменен судебной властью в сентябре 2011 года. [65]
Общество и культура
[ редактировать ]Имена
[ редактировать ]Фенилпропаноламин — это непатентованное название препарата и его МНН , МНН и DCF , а по одобренное в Великобритании название в подсказке для подсказки по международное непатентованное в в случае гидрохлоридная соль . [9] [1] [10] [2] Он также известен под синонимом норэфедрин . [9] [1] [2]
Торговые марки PPA включают Acutrim, Appedrine, Capton Diet, Control, Dexatrim, Emagrin Plus AP, Glifenтол, Kontexin, Merex, Monydrin, Mydriatine, Prolamine, Propadrine, Propagest, Recatol, Rinexin, Tinaroc и Westrim, среди многих других. [9] [1] [2] Он также использовался в комбинациях под торговыми марками, включая Allerest, Demazin, Dimetapp и Sinarest, среди других. [1] [2]
Доступность
[ редактировать ]PPA по-прежнему доступен для медицинского и ветеринарного использования в некоторых странах. [1] [2]
Физические упражнения и спорт
[ редактировать ]Был интерес к PPA как препарату, повышающему работоспособность при физических упражнениях и спорте . [66] Однако клинические исследования показывают, что PPA в этом отношении неэффективен. [66] [6] PPA не входит в Всемирного антидопингового агентства (ВАДА) список запрещенных веществ по состоянию на 2024 год. [67]
Юридический статус
[ редактировать ]В Швеции PPA по-прежнему доступен в составе противозастойных средств, отпускаемых по рецепту; [68] PPA также все еще доступен в Германии. Он используется в некоторых лекарствах- полипиллах , таких как капсулы Wick DayMed.
В Соединенном Королевстве PPA был доступен во многих препаратах от кашля и простуды «все в одном», которые обычно также содержат парацетамол или другой анальгетик и кофеин , и их также можно было приобрести отдельно; однако он больше не одобрен для использования человеком. Для приобретения PPA для академического использования требуется европейская лицензия категории 1.
В США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) выпустило рекомендации по общественному здравоохранению. [69] против использования препарата в ноябре 2000 года. В этой рекомендации FDA потребовало, но не потребовало, чтобы все фармацевтические компании прекратили продажу продуктов, содержащих PPA. По оценкам агентства, PPA вызывает от 200 до 500 инсультов в год среди пользователей в возрасте от 18 до 49 лет. В 2005 году FDA исключило PPA из безрецептурной продажи и лишило его статуса «общепризнанного безопасного и эффективного» (GRASE). [70] Согласно Закону CARES 2020 года , для повторного выхода на рынок требуется одобрение FDA, что фактически запрещает препарат даже в качестве отпускаемого по рецепту. [71]
Из-за его потенциального использования при производстве амфетамина PPA контролируется Законом о борьбе с эпидемией метамфетамина 2005 года . Однако он по-прежнему доступен для ветеринарного применения у собак для лечения недержания мочи .
На международном уровне пункт повестки дня сессии Комиссии по наркотическим средствам 2000 года содержал призыв к включению стереоизомера норэфедрина в Таблицу I Конвенции Организации Объединенных Наций против незаконного оборота наркотических средств и психотропных веществ . [72]
Препараты, содержащие PPA, были запрещены в Индии 27 января 2011 года. [73] 13 сентября 2011 года Высокий суд Мадраса отменил запрет на производство и продажу педиатрических препаратов PPA и нимесулида . [74]
Ветеринарное использование
[ редактировать ]PPA остается доступным для использования в ветеринарной медицине . [25] Он используется для контроля недержания мочи у собак. [75] [76]
Примечания
[ редактировать ]- ^ 4-гидроксиамфетамин Было показано, что метаболизируется в 4-гидроксинорэфедрин под действием дофамин-бета-гидроксилазы (DBH) in vitro , и предполагается, что он метаболизируется аналогичным образом in vivo . [38] [43] Данные исследований, в которых измерялось влияние концентраций DBH в сыворотке крови на метаболизм 4-гидроксиамфетамина у людей, позволяют предположить, что другой фермент может опосредовать превращение 4-гидроксиамфетамина в 4-гидроксинорэфедрин ; [43] [45] однако другие данные исследований на животных позволяют предположить, что эта реакция катализируется DBH в синаптических везикулах норадренергических нейронов головного мозга. [46] [47]
Справочные примечания
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час я Швейцарская ассоциация фармацевтов (2000). Index Nominum 2000: Международный каталог лекарств . Индекс существительного. Научное издательство Медфарм. п. 828. ИСБН 978-3-88763-075-1 . Проверено 1 августа 2024 г.
- ^ Перейти обратно: а б с д и ж г час я дж «Фенилпропаноламин» . веб.архив.орг . 24 марта 2015 года. Архивировано из оригинала 6 мая 2015 года . Проверено 1 августа 2024 г.
{{cite web}}: CS1 maint: неподходящий URL ( ссылка ) - ^ Анвиса (24 июля 2023 г.). «НДК № 804 – Списки наркотических средств, психотропных веществ, прекурсоров и других веществ, находящихся под особым контролем» [Постановление Коллегиального совета № 804 – Списки наркотических средств, психотропных веществ, прекурсоров и других веществ, находящихся под особым контролем» (на бразильском португальском языке). Официальный вестник Союза (опубликовано 25 июля 2023 г.). Архивировано из оригинала 27 августа 2023 года . Проверено 27 августа 2023 г.
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т в v В х и С аа аб и объявление но из в ах Канфер И., Дауз Р., Вума В. (1993). «Фармакокинетика пероральных деконгестантов». Фармакотерапия . 13 (6 Пт 2): 116С–128С, обсуждение 143С–146С. ПМИД 7507589 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с т Чуа С.С., Бенримой С.И., Триггс Э.Дж. (1989). «Фармакокинетика безрецептурных симпатомиметиков». Утилизация биофармацевтических препаратов . 10 (1): 1–14. дои : 10.1002/bdd.2510100102 . ПМИД 2647163 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п Бушар Р., Вебер А.Р., Гейгер Дж.Д. (июль 2002 г.). «Информированное принятие решений об использовании симпатомиметиков в спорте и здоровье». Клин Дж Спорт Мед . 12 (4): 209–224. дои : 10.1097/00042752-200207000-00003 . ПМИД 12131054 .
- ^ Перейти обратно: а б с д и ж г час Джентиле Д.А., Фрайдей Г.А., Сконер Д.П. (2000). «Лечение аллергического ринита: антигистаминные и противозастойные средства». Клиники иммунологии и аллергии Северной Америки . 20 (2): 355–368. дои : 10.1016/S0889-8561(05)70152-1 .
- ^ Перейти обратно: а б с «Фенилпропаноламин: использование, взаимодействие, механизм действия» . ДругБанк Онлайн . 29 июня 2018 года . Проверено 1 августа 2024 г.
- ^ Перейти обратно: а б с д и ж г час Элкс Дж. (2014). Словарь лекарств: Химические данные: Химические данные, структуры и библиография . Спрингер США. п. 71. ИСБН 978-1-4757-2085-3 . Проверено 1 августа 2024 г.
- ^ Перейти обратно: а б с д и ж Мортон И.К., Холл Дж.М. (2012). Краткий словарь фармакологических средств: свойства и синонимы . Спрингер Нидерланды. п. 219. ИСБН 978-94-011-4439-1 . Проверено 1 августа 2024 г.
- ^ Перейти обратно: а б с д и ж г час Иоаннидес-Демос Л.Л., Пройетто Дж., Тонкин А.М., МакНил Дж.Дж. (2006). «Безопасность лекарственных средств, применяемых для снижения веса и лечения ожирения». Препарат Саф . 29 (4): 277–302. дои : 10.2165/00002018-200629040-00001 . ПМИД 16569079 .
- ^ Перейти обратно: а б с Салерно С.М., Джексон Дж.Л., Бербано Э.П. (август 2005 г.). «Влияние перорального фенилпропаноламина на артериальное давление: метаанализ и обзор литературы». Джей Хум Гипертония . 19 (8): 643–652. дои : 10.1038/sj.jhh.1001869 . ПМИД 15944721 .
- ^ Перейти обратно: а б с д и Джонсон Д.А., Хричик Дж.Г. (1993). «Фармакология альфа-адренергических противозастойных средств». Фармакотерапия . 13 (6 Пт 2): 110С–115С, обсуждение 143С–146С. ПМИД 7507588 .
- ^ Перейти обратно: а б с д и ж О'Доннелл С.Р. (март 1995 г.). «Симпатомиметические сосудосуживающие средства как противозастойные средства для носа». Мед Дж. Ауст . 162 (5): 264–267. дои : 10.5694/j.1326-5377.1995.tb139882.x . ПМИД 7534374 .
- ^ Перейти обратно: а б Аарон СК (август 1990 г.). «Симпатомиметики». Emerg Med Clin North Am . 8 (3): 513–526. ПМИД 2201518 .
- ^ Перейти обратно: а б с Юн Б.В., Пэ Х.Дж., Хон К.С., Ли С.М., Пак Б.Дж., Ю К.Х. и др. (январь 2007 г.). «Фенилпропаноламин, содержащийся в средствах от простуды, и риск геморрагического инсульта». Неврология . 68 (2): 146–149. дои : 10.1212/01.wnl.0000250351.38999.f2 . ПМИД 17210897 . S2CID 211233331 .
- ^ Перейти обратно: а б с д и ж Ротман Р.Б., Бауманн М.Х. (2006). «Терапевтический потенциал субстратов-переносчиков моноаминов». Curr Top Med Chem . 6 (17): 1845–1859. дои : 10.2174/156802606778249766 . ПМИД 17017961 .
- ^ Перейти обратно: а б с д и Ротман Р.Б., Бауманн М.Х. (декабрь 2005 г.). «Целевой скрининг переносчиков биогенных аминов: потенциальное применение натуральных продуктов». Наука о жизни . 78 (5): 512–518. дои : 10.1016/j.lfs.2005.09.001 . ПМИД 16202429 .
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п Ротман Р.Б., Ву Н., Партилла Дж.С., Рот Б.Л., Хуфейсен С.Дж., Комптон-Тот Б.А. и др. (октябрь 2003 г.). «Характеристика in vitro родственных эфедрину стереоизомеров биогенных аминопереносчиков и рецептором обнаруживает селективное действие в качестве субстратов переносчика норэпинефрина». J Pharmacol Exp Ther . 307 (1): 138–145. дои : 10.1124/jpet.103.053975 . ПМИД 12954796 .
- ^ Перейти обратно: а б с д Лемке Т.Л., Уильямс Д.А. (2008). Принципы медицинской химии Фоя . Липпинкотт Уильямс и Уилкинс. стр. 643–. ISBN 978-0-7817-6879-5 .
- ^ Перейти обратно: а б с д и ж г час я дж к Джонсон Д.А. (1991). «Фармакология и безопасность фенилпропаноламина». Исследования в области разработки лекарств . 22 (3): 197–207. дои : 10.1002/ddr.430220302 . ISSN 0272-4391 .
- ^ Перейти обратно: а б с Браво Э.Л. (март 1988 г.). «Фенилпропаноламин и другие вазоактивные соединения, отпускаемые без рецепта». Гипертония . 11 (3, часть 2): II7–10. дои : 10.1161/01.hyp.11.3_pt_2.ii7 . ПМИД 3280497 .
- ^ Перейти обратно: а б с д и Мерсфельдер Т.Л. (март 2001 г.). «Фенилпропаноламин и инсульт: исследование, постановление FDA, последствия». Клив Клин, Джей Мед . 68 (3): 208–9, 213–9, 223. doi : 10.3949/ccjm.68.3.208 . ПМИД 11263849 .
- ^ Перейти обратно: а б с «Drugs@FDA: препараты, одобренные FDA» . accessdata.fda.gov . Управление по контролю за продуктами и лекарствами . Проверено 1 августа 2024 г.
- ^ Перейти обратно: а б с д «Результаты поиска фенилпропаноламина» . ДейлиМед . Проверено 1 августа 2024 г.
- ^ Коултер А.А., Ребелло С.Дж., Гринуэй, Флорида (июль 2018 г.). «Агенты центрального действия при ожирении: прошлое, настоящее и будущее» . Наркотики . 78 (11): 1113–1132. дои : 10.1007/s40265-018-0946-y . ПМК 6095132 . ПМИД 30014268 .
- ^ Иоаннидес-Демос Л.Л., Пройетто Дж., МакНил Дж.Дж. (2005). «Фармакотерапия ожирения». Наркотики . 65 (10): 1391–418. дои : 10.2165/00003495-200565100-00006 . ПМИД 15977970 .
- ^ Гринуэй Ф., Хербер Д., Раум В., Хербер Д., Моралес С. (июль 1999 г.). «Двойные слепые рандомизированные плацебо-контролируемые клинические исследования безрецептурных препаратов для лечения ожирения». Обес Рес . 7 (4): 370–378. дои : 10.1002/j.1550-8528.1999.tb00420.x . ПМИД 10440593 .
- ^ Тайминен Т., Яскеляйнен С.К. (сентябрь 2001 г.). «Интенсивные и повторяющиеся переживания дежавю, связанные с амантадином и фенилпропаноламином, у здорового мужчины». Журнал клинической неврологии . 8 (5): 460–462. дои : 10.1054/jocn.2000.0810 . ПМИД 11535020 . S2CID 6733989 .
- ^ Банко Дж., Брюне-Буржен Ф., Шовель П., Халгрен Э. (февраль 1994 г.). «Анатомическое происхождение дежавю и ярких «воспоминаний» при височной эпилепсии человека». Мозг . 117 (Часть 1): 71–90. дои : 10.1093/мозг/117.1.71 . ПМИД 8149215 .
- ^ Ротман Р.Б., Бауманн М.Х. (2003). «Переносчики моноаминов и психостимуляторы». Евро. Дж. Фармакол . 479 (1–3): 23–40. дои : 10.1016/j.ejphar.2003.08.054 . ПМИД 14612135 .
- ^ Перейти обратно: а б с д и Ротман Р.Б., Бауманн М.Х., Дерш К.М., Ромеро Д.В., Райс К.С., Кэрролл Ф.И. и др. (январь 2001 г.). «Стимуляторы центральной нервной системы амфетаминового типа высвобождают норадреналин более эффективно, чем дофамин и серотонин». Синапс . 39 (1): 32–41. doi : 10.1002/1098-2396(20010101)39:1<32::AID-SYN5>3.0.CO;2-3 . ПМИД 11071707 .
- ^ Бауманн М.Х., Партилла Дж.С., Ленер К.Р., Торндайк Э.Б., Хоффман А.Ф., Холи М. и др. (2013). «Мощное кокаиноподобное действие 3,4-метилендиоксипировалерона (МДПВ), основного компонента психоактивных солей для ванн» . Нейропсихофармакология . 38 (4): 552–562. дои : 10.1038/нпп.2012.204 . ПМЦ 3572453 . ПМИД 23072836 .
- ^ Бауманн М.Х., Айестас М.А., Партилла Дж.С., Синк Дж.Р., Шульгин А.Т., Дейли П.Ф. и др. (апрель 2012 г.). «Разработанные аналоги меткатинона, мефедрон и метилон, являются субстратами для переносчиков моноаминов в тканях мозга» . Нейропсихофармакология . 37 (5): 1192–203. дои : 10.1038/нпп.2011.304 . ПМК 3306880 . ПМИД 22169943 .
- ^ Гловацка К., Вела-Гойеньска А (май 2021 г.). «Псевдоэфедрин — преимущества и риски» . Int J Mol Sci . 22 (10): 5146. doi : 10.3390/ijms22105146 . ПМК 8152226 . ПМИД 34067981 .
- ^ Патрик К.С., Марковиц Дж.С. (1997). «Фармакология метилфенидата, энантиомеров амфетамина и пемолина при синдроме дефицита внимания и гиперактивности». Психофармакология человека: клиническая и экспериментальная . 12 (6): 527–546. doi : 10.1002/(SICI)1099-1077(199711/12)12:6<527::AID-HUP932>3.0.CO;2-U . ISSN 0885-6222 .
- ^ «Информация о назначении Adderall XR» (PDF) . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США . Shire US Inc., декабрь 2013 г., стр. 12–13 . Проверено 30 декабря 2013 г.
- ^ Перейти обратно: а б Гленнон Р.А. (2013). «Стимуляторы фенилизопропиламина: агенты, связанные с амфетамином» . В Лемке Т.Л., Уильямс Д.А., Рош В.Ф., Зито В. (ред.). Принципы медицинской химии Фоя (7-е изд.). Филадельфия, США: Wolters Kluwer Health/Lippincott Williams & Wilkins. стр. 646–648. ISBN 9781609133450 .
Простейший незамещенный фенилизопропиламин, 1-фенил-2-аминопропан или амфетамин, служит общей структурной матрицей для галлюциногенов и психостимуляторов. Амфетамин оказывает центральное стимулирующее, аноректическое и симпатомиметическое действие и является прототипом этого класса (39). ... Фаза 1 метаболизма аналогов амфетамина катализируется двумя системами: цитохромом P450 и флавинмонооксигеназой. ... Амфетамин также может подвергаться ароматическому гидроксилированию до п -гидроксиамфетамина. ... Последующее окисление в бензильном положении DA-β-гидроксилазой дает п- гидроксинорэфедрин. Альтернативно, прямое окисление амфетамина DA-β-гидроксилазой может дать норэфедрин.
- ^ Тейлор КБ (январь 1974 г.). «Дофамин-бета-гидроксилаза. Стереохимический ход реакции» (PDF) . Журнал биологической химии . 249 (2): 454–458. дои : 10.1016/S0021-9258(19)43051-2 . ПМИД 4809526 . Проверено 6 ноября 2014 г.
Дофамин-β-гидроксилаза катализирует удаление атома водорода про- R и образование 1-норэфедрина, (2S , 1R ) -2-амино-1-гидроксил-1-фенилпропана из d -амфетамина.
- ^ Крюгер С.К., Уильямс Д.Э. (июнь 2005 г.). «Флавинсодержащие монооксигеназы млекопитающих: структура/функция, генетический полиморфизм и роль в метаболизме лекарств» . Фармакология и терапия . 106 (3): 357–387. doi : 10.1016/j.pharmthera.2005.01.001 . ПМК 1828602 . ПМИД 15922018 .
Таблица 5: N-содержащие препараты и ксенобиотики, оксигенированные FMO - ^ Кэшман-младший, Сюн Ю.Н., Сюй Л., Яновский А. (март 1999 г.). «N-оксигенация амфетамина и метамфетамина человеческой флавинсодержащей монооксигеназой (форма 3): роль в биоактивации и детоксикации». Журнал фармакологии и экспериментальной терапии . 288 (3): 1251–1260. ПМИД 10027866 .
- ^ Сантагати Н.А., Феррара Г., Марраццо А., Ронсисвалле Г. (сентябрь 2002 г.). «Одновременное определение амфетамина и одного из его метаболитов методом ВЭЖХ с электрохимическим обнаружением». Журнал фармацевтического и биомедицинского анализа . 30 (2): 247–255. дои : 10.1016/S0731-7085(02)00330-8 . ПМИД 12191709 .
- ^ Перейти обратно: а б с Сьердсма А., фон Штудниц В. (апрель 1963 г.). «Активность дофамин-бета-оксидазы у человека при использовании гидроксиамфетамина в качестве субстрата» . Британский журнал фармакологии и химиотерапии . 20 (2): 278–284. дои : 10.1111/j.1476-5381.1963.tb01467.x . ПМК 1703637 . ПМИД 13977820 .
Гидроксиамфетамин вводили перорально пяти людям... Поскольку превращение гидроксиамфетамина в гидроксинорэфедрин происходит in vitro под действием дофамин-β-оксидазы, предложен простой метод измерения активности этого фермента и действия его ингибиторов на человека. . ... Отсутствие эффекта от введения неомицина одному пациенту свидетельствует о том, что гидроксилирование происходит в тканях организма. ... основная часть β-гидроксилирования гидроксиамфетамина происходит в тканях, не относящихся к надпочечникам. К сожалению, в настоящее время нельзя быть полностью уверенным в том, что гидроксилирование гидроксиамфетамина in vivo осуществляется тем же ферментом, который превращает дофамин в норадреналин.
- ^ Баденхорст К.П., ван дер Слюс Р., Эразмус Э., ван Дейк А.А. (сентябрь 2013 г.). «Глициновая конъюгация: значение в метаболизме, роль глицин-N-ацилтрансферазы и факторы, влияющие на межиндивидуальные вариации». Экспертное заключение по метаболизму и токсикологии лекарственных средств . 9 (9): 1139–1153. дои : 10.1517/17425255.2013.796929 . ПМИД 23650932 . S2CID 23738007 .
Рисунок 1. Глициновая конъюгация бензойной кислоты. Путь конъюгации глицина состоит из двух этапов. Сначала бензоат лигируется с CoASH с образованием высокоэнергетического тиоэфира бензоил-КоА. Эта реакция катализируется лигазами средней цепи кислоты HXM-A и HXM-B:CoA и требует энергии в виде АТФ. ... Бензоил-КоА затем конъюгируется с глицином с помощью GLYAT с образованием гиппуровой кислоты, высвобождая CoASH. В дополнение к факторам, перечисленным в рамках, уровни АТФ, КоАСГ и глицина могут влиять на общую скорость пути конъюгации глицина.
- ^ Хорвиц Д., Александр Р.В., Ловенберг В., Кейзер Х.Р. (май 1973 г.). «Дофамин-β-гидроксилаза сыворотки человека. Связь с гипертонией и симпатической активностью». Исследование кровообращения . 32 (5): 594–599. дои : 10.1161/01.RES.32.5.594 . ПМИД 4713201 . S2CID 28641000 .
Биологическое значение различных уровней активности DβH в сыворотке изучали двумя способами. Во-первых, способность in vivo β-гидроксилировать синтетический субстрат гидроксиамфетамин сравнивали у двух субъектов с низкой активностью DβH в сыворотке и у двух субъектов со средней активностью. ... В одном исследовании гидроксиамфетамин (паредрин), синтетический субстрат DβH, вводили субъектам с низким или средним уровнем активности DβH в сыворотке. Процент препарата, гидроксилированного до гидроксинорэфедрина, был сопоставим у всех испытуемых (6,5–9,62) (табл. 3).
- ^ Фриман Джей Джей, Сульсер Ф (декабрь 1974 г.). «Образование п-гидроксинорэфедрина в головном мозге после внутрижелудочкового введения п-гидроксиамфетамина». Нейрофармакология . 13 (12): 1187–1190. дои : 10.1016/0028-3908(74)90069-0 . ПМИД 4457764 .
У видов, у которых основным путем метаболизма является ароматическое гидроксилирование амфетамина, п- гидроксиамфетамин (POH) и п- гидроксинорэфедрин (PHN) могут вносить вклад в фармакологический профиль исходного препарата. ... Расположение реакций p- гидроксилирования и β-гидроксилирования важно для видов, у которых ароматическое гидроксилирование амфетамина является преобладающим путем метаболизма. После системного введения амфетамина крысам ПОН был обнаружен в моче и плазме.
Наблюдаемое отсутствие значительного накопления PHN в головном мозге после внутрижелудочкового введения (+)-амфетамина и образование заметных количеств PHN из (+)-POH в ткани головного мозга in vivo подтверждает точку зрения, что ароматическое гидроксилирование амфетамина после его системное введение происходит преимущественно на периферии, и затем POH транспортируется через гематоэнцефалический барьер, поглощаясь норадренергическими нейронами головного мозга, где (+)-POH преобразуется в везикулах-хранилищах под действием дофамин-β-гидроксилазы в PHN. - ^ Мацуда Л.А., Хэнсон Г.Р., Гибб Дж.В. (декабрь 1989 г.). «Нейрохимические эффекты метаболитов амфетамина на центральные дофаминергические и серотонинергические системы». Журнал фармакологии и экспериментальной терапии . 251 (3): 901–908. ПМИД 2600821 .
Метаболизм p -OHA в p -OHNor хорошо известен, и дофамин-β-гидроксилаза, присутствующая в норадренергических нейронах, может легко превращать p -OHA в p -OHNor после внутрижелудочкового введения.
- ^ Перейти обратно: а б с Король Лос-Анджелеса (2009). Судебная химия злоупотребления психоактивными веществами: Руководство по контролю над наркотиками . Королевское химическое общество. стр. 53–. ISBN 978-0-85404-178-7 .
- ^ Балинт Э.Э., Фалькай Г., Балинт Г.А. (2009). «Хат – спорное растение». Венский клинический еженедельник . 121 (19–20): 604–614. дои : 10.1007/s00508-009-1259-7 . ПМИД 19921126 . S2CID 22816940 .
- ^ Перейти обратно: а б с д и Westfall DP, Westfall TC (2010). «Глава 12: Адренергические агонисты и антагонисты: КЛАССИФИКАЦИЯ СИМПАТОМИМЕТИЧЕСКИХ ПРЕПАРАТОВ». В Брантоне Л.Л., Чабнере Б.А., Ноллманне Б.К. (ред.). Фармакологические основы терапии Гудмана и Гилмана (12-е изд.). Нью-Йорк: МакГроу-Хилл. ISBN 9780071624428 .
ХИМИЯ И ВЗАИМОСВЯЗЬ СТРУКТУРА-АКТИВНОСТЬ СИМПАТОМИМЕТИЧЕСКИХ АМИНОВ
β-Фенилэтиламин (таблица 12–1) можно рассматривать как исходное соединение симпатомиметических аминов, состоящее из бензольного кольца и этиламиновой боковой цепи. Структура позволяет производить замены в ароматическом кольце, α- и β-атомах углерода и концевой аминогруппе с образованием множества соединений с симпатомиметической активностью. ...N-метилирование увеличивает активность первичных аминов...
Замещение в атоме α-углерода
Эта замена блокирует окисление МАО, значительно продлевая продолжительность действия некатехоламинов, поскольку их деградация во многом зависит от действия этого фермента. Таким образом, продолжительность действия таких наркотиков, как эфедрин или амфетамин, измеряется часами, а не минутами. Аналогичным образом, соединения с α-метильным заместителем сохраняются в нервных окончаниях и с большей вероятностью высвобождают НЭ из мест хранения. Такие агенты, как метараминол, проявляют большую степень непрямой симпатомиметической активности.
Замещение в атоме β-углерода
Замещение гидроксильной группы у β-углерода обычно снижает активность в ЦНС, главным образом потому, что снижает растворимость в липидах. Однако такая замена значительно усиливает агонистическую активность как α-, так и β-адренергических рецепторов. Хотя эфедрин менее эффективен, чем метамфетамин, в качестве центрального стимулятора, он более эффективен в расширении бронхиол и повышении артериального давления и частоты сердечных сокращений. - ^ Перейти обратно: а б «Фенилпропаноламин» . ПабХим . Проверено 1 августа 2024 г.
- ^ Бхарате СС, Миньяни С, Вишвакарма РА (декабрь 2018 г.). «Почему большинство активных соединений в области ЦНС являются натуральными продуктами? Критический анализ». J Med Chem . 61 (23): 10345–10374. doi : 10.1021/acs.jmedchem.7b01922 . ПМИД 29989814 .
- ^ Перейти обратно: а б с Шеп Л.Дж., Слотер Р.Дж., Бизли Д.М. (август 2010 г.). «Клиническая токсикология метамфетамина». Клин Токсикол (Фила) . 48 (7): 675–694. дои : 10.3109/15563650.2010.516752 . ПМИД 20849327 .
Метамфетамин действует аналогично амфетамину, но с добавлением метильной группы в химическую структуру. Он более липофильен (значение Log p 2,07 по сравнению с 1,76 для амфетамина). 4 тем самым обеспечивая быстрый и обширный транспорт через гематоэнцефалический барьер. 19
- ^ «Амфетамин» . ПабХим . Проверено 26 июля 2024 г.
- ^ «Эфедрин» . ПабХим . Проверено 26 июля 2024 г.
- ^ «Псевдоэфедрин» . ПабХим . Проверено 1 августа 2024 г.
- ^ «Фенилэфрин» . ПабХим . Проверено 21 июля 2024 г.
- ^ «Норэпинефрин» . ПабХим . Проверено 26 июля 2024 г.
- ^ Экклс Р. (январь 2007 г.). «Замена фенилэфрина псевдоэфедрином в качестве противоотечного средства для носа. Нелогичный способ борьбы со злоупотреблением метамфетамином» . Британский журнал клинической фармакологии . 63 (1): 10–14. дои : 10.1111/j.1365-2125.2006.02833.x . ПМК 2000711 . ПМИД 17116124 .
- ^ Фрёзе Л., Дайан Дж., Гомес А., Унгер Б., Зейлер Ф.А. (октябрь 2020 г.). «Цереброваскулярная реакция на норадреналин: обзорный систематический обзор литературы о животных и людях» . Фармакол Рес Перспектива . 8 (5): e00655. дои : 10.1002/prp2.655 . ПМЦ 7510331 . ПМИД 32965778 .
- ^ Пажухеш Х., Ленц Г.Р. (октябрь 2005 г.). «Лекарственные химические свойства успешных препаратов для центральной нервной системы» . НейроРкс . 2 (4): 541–553. дои : 10.1602/neurorx.2.4.541 . ПМК 1201314 . ПМИД 16489364 .
Липофильность была первым из дескрипторов, которые были определены как важные для проникновения в ЦНС. Ханш и Лео54 предположили, что высоколипофильные молекулы будут распределены внутри липидной внутренней части мембран и останутся там. Однако ClogP хорошо коррелирует с LogBBB, причем увеличение липофильности увеличивает проникновение в мозг. Для нескольких классов активных веществ ЦНС Ханш и Лео54 обнаружили, что проникновение через гематоэнцефалический барьер является оптимальным, когда значения LogP находятся в диапазоне 1,5-2,7 со средним значением 2,1. Анализ небольших молекул, подобных лекарствам, показал, что для лучшего проникновения в мозг46 и хорошей кишечной проницаемости55 значения LogD должны быть больше 0 и меньше 3. Для сравнения, среднее значение ClogP для продаваемых препаратов для ЦНС составляет 2,5, что соответствует хорошо согласуется с диапазоном, найденным Ханшем и др.22
- ^ «Рекомендации, предупреждения и отзывы – 2001 г.» . Здоровье Канады . 7 января 2009 г. Архивировано из оригинала 3 мая 2010 г.
- ^ «Тревога Фенилпропаноламин» . Управление терапевтическими товарами . 7 марта 2006 г. Проверено 31 декабря 2018 г.
- ^ «Наркотики запрещены в Индии» . Dte.GHS, Министерство здравоохранения и благосостояния семьи, Правительство Индии . Центральная организация по контролю за стандартами на лекарства. Архивировано из оригинала 13 октября 2013 года . Проверено 7 января 2014 г.
- ^ «Высокий суд Мадраса отменяет запрет на производство и продажу педиатрических препаратов нимесулида и PPA – India Medical Times» .
- ^ Перейти обратно: а б Джонс Дж. (2008). «Кофеин и другие симпатомиметические стимуляторы: способы действия и влияние на спортивные результаты». Очерки биохимии . 44 : 109–123. дои : 10.1042/BSE0440109 . ПМИД 18384286 .
- ^ «Запрещенный список» . Всемирное антидопинговое агентство . 1 января 2024 года . Проверено 1 августа 2024 г.
- ^ «Ринексин in Farmaceutiska Specialiteter i Sverige» [«Ринексин» из фармацевтической отрасли Швеции] (каталог лекарств) (на шведском языке) . Проверено 7 января 2014 г.
- ^ «Рекомендации по фенилпопаноламину» (пресс-релиз). Управление по контролю за продуктами и лекарствами США. 6 ноября 2000 г. Архивировано из оригинала 26 января 2010 г.
- ^ «Информационная страница фенилпропаноламина (PPA) – FDA выводит PPA из безрецептурного отпуска» (пресс-релиз). Управление по контролю за продуктами и лекарствами США. 23 декабря 2005 г. Архивировано из оригинала 12 января 2009 г.
- ^ Обзор лекарств, отпускаемых без рецепта (OTC) | Реформа безрецептурных монографий в Законе CARES
- ^ Реализация международных договоров о контроле над наркотиками: изменения в сфере контроля над веществами . Вена: Комиссия по наркотическим средствам, сорок третья сессия. 6–15 марта 2000 г. Архивировано из оригинала 14 августа 2003 г.
- ^ «Небезопасные препараты – нимесулид, цизаприд, фенилпропаноламин запрещены» . 27 января 2011 г.
- ^ «Высокий суд Мадраса отменяет запрет на производство и продажу PPA» . Scribd.com. 13 сентября 2011 года . Проверено 7 января 2014 г.
- ^ Гупта RC (23 апреля 2012 г.). Ветеринарная токсикология: основные и клинические принципы . Академическая пресса. стр. 458–. ISBN 978-0-12-385927-3 .
- ^ Ривьер Ж. Э., Папич М. Г. (17 марта 2009 г.). Ветеринарная фармакология и терапия . Джон Уайли и сыновья. стр. 1309–. ISBN 978-0-8138-2061-3 .
- Алкалоиды амфетамина
- Аноректики
- Препараты против ожирения
- Противозастойные средства
- Препараты, действующие на сердечно-сосудистую систему
- Препараты, действующие на нервную систему
- Наркотики в спорте
- Энантиочистые препараты
- Эргогенные средства
- Метаболиты лекарственных препаратов человека
- Агенты, высвобождающие норэпинефрин
- Периферически селективные препараты
- Фенилэтаноламины
- Метаболиты рекреационных наркотиков
- Стимуляторы
- Замещенные амфетамины
- Симпатомиметики
- Ветеринарные препараты
- Отменены препараты против ожирения
- Запрещенные вещества Всемирного антидопингового агентства