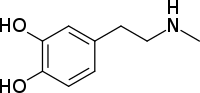
Дезоксиэпинефрин
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК 4-[2-(Метиламино)этил]бензол-1,2-диол | |
| Другие имена Эпинин; N -Метилдофамин; 3,4-Дигидрокси -N -метилфенэтиламин | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.007.200 |
| КЕГГ | |
| МеШ | Дезоксиэпинефрин |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| C9H13NOC9H13NO2 | |
| Молярная масса | 167.21 g/mol |
| Появление | бесцветное кристаллическое твердое вещество |
| Температура плавления | От 188 до 189 ° C (от 370 до 372 ° F; от 461 до 462 К) [1] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Дезоксиэпинефрин , также известный под общими названиями N -метилдофамин и эпинин , представляет собой органическое соединение и природный продукт , который структурно связан с важными нейротрансмиттерами дофамином и адреналином . Все три этих соединения также принадлежат к семейству катехоламинов . Фармакология эпинина во многом напоминает фармакологию его «родителя» — дофамина. Эпинин был обнаружен у растений, насекомых и животных. Он также важен как активный продукт метаболического распада пролекарства ибопамина , который используется для лечения застойной сердечной недостаточности . [2] [3]
возникновение
[ редактировать ]Эпинин, по-видимому, не распространен широко, но он присутствует в качестве второстепенного алкалоида в некоторых растениях, таких как кактус пейот , Lophophora williamsii , [4] и разновидность акации , [5] а также у метлы обыкновенной , Cytisus scoparius . [6] Это соединение также было выделено из мозгового вещества надпочечников свиней и коров. [7] от жабы и Rhinella marina . [8] Он также был обнаружен у саранчи migratoria Locusta . [9]
Химия
[ редактировать ]Подготовка
[ редактировать ]О первом полном синтезе эпинина сообщил Бак, который получил его из 3,4-диметоксифенэтиламина («гомовератриламин») путем сначала превращения последнего в его основание Шиффа с помощью бензальдегида , а затем N -метилирования его метилиодидом ; За гидролизом полученного продукта следовало расщепление метиловых эфиров с использованием иодоводородной кислоты с получением эпинина. [10] Очень похожий синтез, отличающийся только использованием диметилсульфата для N -метилирования и HBr для O -деметилирования, но предоставляющий более подробные экспериментальные детали, был опубликован Боргманом в 1973 году. [11]
Более ранний полусинтез (названный так потому, что начался с натурального продукта лауданозина ) Пимана. [1] неправильно цитируется Баком, [10] и ошибка была перенесена на запись об эпинине (под названием дезоксиэпинефрин) в индексе Merck. [12]
Обычными солями эпинина являются: гидрохлорид, C 9 H 13 NO 2 .HCl, т.пл. 179-180°С; сульфат, (C 9 H 13 NO 2 ) 2 ·H 2 SO 4 , т. пл. 289-290°С; [1] гидробромид, C 9 H 13 NO 2 .HBr, т.пл. 165-166°С. [11]
Структура
[ редактировать ]Сообщалось о рентгеновской структуре гидробромида эпинина. [13]
Фармакология
[ редактировать ]Одна из наиболее выдающихся фармакологических характеристик эпинина, его способность повышать кровяное давление, была отмечена еще в 1910 году Баргером и Дейлом, которые сообщили, что «метиламиноэтилкатехин», как они его называли, имеет около 1/7 в 5 раз выше прессорной активности адреналина, но примерно в 5 раз выше активности дофамина («аминоэтилкатехина») в препаратах для кошек. [14] Компания Buroughs Wellcome Co., на которую работали Баргер, Дейл и Пайман (см. раздел «Химия»), впоследствии продавала гидрохлоридную соль «метиламиноэтилкатехина» под названием «эпинин» в качестве заменителя адреналина. [15] Тейнтер далее количественно оценил прессорную активность эпинина у обработанных атропином и анестезированных интактных кошек, показав, что дозы 0,02-0,2 мг, вводимые внутривенно, были примерно в 1/12 активнее, чем L-адреналин, но эффект длился примерно в два раза дольше. (~3 минуты) и сопровождалось увеличением частоты пульса. [15]
В конечном итоге было установлено, что эпинин является неселективным стимулятором дофаминовых (DA) рецепторов, α- и β- адренорецепторов , причем стимуляция D2 - рецепторов приводит к ингибированию норадренергической и ганглиозной нейротрансмиссии. Эти исследования, проведенные с использованием анестезированных животных, были расширены ван Веркенсом и его коллегами, которые сравнили эффекты эпинина и дофамина на неанестезированных свиньях, чтобы избежать любого возможного влияния анестетика. Дозы лекарственного средства находились в диапазоне 1-10 мкг/кг/мин и вводились путем внутривенной инфузии в течение 10 минут. Результаты этих экспериментов показали, что у свиней в используемом диапазоне доз эпинин был более эффективным, чем дофамин, в качестве агониста D 2 , α- и β 2 -рецепторов, но был слабее, чем дофамин, в качестве D 1 -рецепторов. агонист. Эффект β 1 -агониста обоих соединений был слабым или отсутствовал. [16]
Сопоставимые исследования, в которых кровяное давление, частота сердечных сокращений и уровни пролактина в сыворотке измерялись после введения 0,5-4 мкг/кг/мин эпинина путем внутривенной инфузии в течение 15-минутного периода здоровым людям, впоследствии были опубликованы Даулом и его коллегами. -рабочие. [17] Эти исследователи обнаружили, что при более низких дозах (0,5 или 1,0 мкг/кг/мин), приводящих к концентрации в плазме 20–80 нМ/л, эпинин, как и дофамин, вызывал падение уровня пролактина, но не влиял на артериальное давление. или частота сердечных сокращений. В более высоких дозах (2,0 или 4,0 мкг/кг/мин) эпинин значительно повышал как систолическое, так и диастолическое артериальное давление, а также частоту сердечных сокращений. Напротив, дофамин вызывал увеличение только систолического артериального давления и частоты сердечных сокращений.Оба препарата увеличивают диурез и натрийурез – эффект, который, как полагают, обусловлен активацией почечных D1 - рецепторов.Сделан вывод, что в более низких дозах эпинин и дофамин оказывали действие только на DA(D2 ) -рецепторы, но не активировали α- или β-адренорецепторы. В более высоких дозах эпинин активировал α-, β 1- и β 2 -рецепторы примерно в одинаковой степени, тогда как дофамин лишь слегка стимулировал β 1 -рецепторы без какого-либо влияния на α- или β 2 -рецепторы. Кроме того, было замечено, что эффекты эпинина во многом были обусловлены его прямым действием на рецепторы, в то время как дофамин также оказывал некоторые из своих эффектов косвенно, стимулируя выброс норадреналина .
Токсичность
[ редактировать ]LD 50 для соли HCl: 212 мг/кг (мышь; внутрибрюшинно). Для сравнения можно отметить, что дофамина ЛД 50 составляет 1978 мг/кг в тех же условиях. [18]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с Ф. Л. Пайман (1910). «XXVIII. Производные изохинолина. Часть III. о-Дигидрокси-основания. Превращение 1-кето-6,7-диметокси-2-метилтетрагидроизохинолинов в 3:4-дигидроксифенилэтилалкиламины». Дж. Хим. Соц., Пер. 97 264-280.
- ^ П. А. Цвитен (1994). «Фармакотерапия застойной сердечной недостаточности». Аптечный мир и наука 16 334–342.
- ^ Р. Гиффорд, У. К. Рэндольф, ФК Хейнеман и Дж. А. Зиемняк (1986). «Анализ эпинина и его метаболитов у человека после перорального введения его пролекарства ибопамина с использованием высокоэффективной жидкостной хроматографии с электрохимическим обнаружением». Журнал хроматографии B 381 83-93. дои 10.1016/S0378-4347(00)83567-7
- ^ Дж. Лундстрем (1971). «Биосинтез алкалоидов мескалина и тетрагидроизохинолина в Lophophora williamsii (Lem.) Coult. Возникновение и биосинтез катехоламинов и других промежуточных продуктов». Акта Хим. Скан. 25 3489-3499. http://actachemscand.dk/pdf/acta_vol_25_p3489-3499.pdf
- ^ BA Клемент, CM Goff и TDA Forbes (1998). «Токсичные амины и алкалоиды акации жесткой ». Фитохимия 49 1377-1380.
- ^ Т. А. Смит (1977). «Фенэтиламин и родственные соединения в растениях». Фитохимия 16 9-18.
- ^ П. Ладюрон, П. ван Гомпель, Дж. Лейсен и М. Клейс (1974). « Образование эпинина in vivo в мозговом веществе надпочечников. Возможный этап биосинтеза адреналина». Арка Наунин-Шмидебергс. Фармакол. 286 227-238.
- ^ Ф. Мярки, Дж. Аксельрод и Б. Виткоп (1962). «Катехоламины и N-метилтрансфераза у южноамериканской жабы ( Bufo marinus )». Биохим. Биофиз. Акта 58 367-369.
- ^ С. Танака и Н. Такеда (1997). «Биогенные моноамины в мозге и сердечном теле между альбиносами и нормальными штаммами перелетной саранчи Locusta migratoria ». Комп. Биохим. Физиол. Пт. С: Комп. Фармакол. Токсикол. 117 221-227.
- ^ Jump up to: а б Дж. С. Бак (1930). «Синтез лодала и эпинина». Дж. Ам. хим. Соц. 52 4119-4122.
- ^ Jump up to: а б Р. Боргман и др. (1973). «Синтез и фармакология производных и аналогов дофамина центрального действия в отношении болезни Паркинсона». Дж. Мед. хим. 16 630-633.
- ^ Индекс Merck, 15-е изд. (2013), с. 524 Монография 2904 , О'Нил: Королевское химическое общество. Доступно онлайн по адресу: http://www.rsc.org/Merck-Index/monograph/mono1500002904.
- ^ Дж. Гизеке (1976). «Строение катехоламинов. V. Кристаллическая и молекулярная структура эпининина гидробромида». Acta Crystallographica Раздел B 32 2337-2340.
- ^ Г. Баргер и Х. Х. Дейл (1910). «Химическая структура и симпатомиметическое действие аминов». Дж. Физиол. 41 19-59.
- ^ Jump up to: а б М. Л. Тейнтер (1930). «Сравнительные действия симпатомиметических соединений: производные катехола». Дж. Фармакол. Эксп. Там. 40 43-64.
- ^ LJ ван Веркенс, Ф. Бусма, AJ Man in 't Veld, MM Bevers, PD Verdouw (1992). «Дифференциальные сердечно-сосудистые и нейроэндокринные эффекты эпинина и дофамина у свиней в сознании до и после блокады адренорецепторов». Бр. Дж. Фармакол. 107 303–310.
- ^ А. Даул и др. (1995). «Дозозависимое разделение дофаминергических и адренергических эффектов эпинина у здоровых добровольцев». Арка Наунин-Шмидебергс. Фармакол. 352 429-437
- ^ Дж. З. Гинос и др. (1975). «Холинергические эффекты молекулярных сегментов апоморфина и дофаминергические эффекты N,N-диалкилированных дофаминов». 18 1194-1200.
- Агонисты альфа-1-адренергических рецепторов
- Агонисты альфа-2-адренергических рецепторов
- Бета-адренергические агонисты
- Катехоламины
- Агонисты D1-рецепторов
- Агонисты D2-рецепторов
- Агонисты дофамина
- Метаболиты лекарственных препаратов человека
- Агенты, высвобождающие норадреналин-дофамин
- Периферически селективные препараты