Кетоновые тела
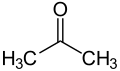
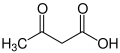
Кетоновые тела — это водорастворимые молекулы или соединения, которые содержат кетоновые группы, вырабатываемые из жирных кислот печенью ( кетогенез ). [1] [2] Кетоновые тела легко транспортируются в ткани за пределами печени, где они превращаются в ацетил-КоА (ацетил-коэнзим А), который затем вступает в цикл лимонной кислоты (цикл Кребса) и окисляется для получения энергии. [3] [4] Эти кетоновые группы, полученные из печени, включают ацетоуксусную кислоту (ацетоацетат), бета-гидроксибутират и ацетон , продукт спонтанного распада ацетоацетата (см. рисунок).
Кетоновые тела вырабатываются печенью в периоды ограничения калорий по различным сценариям: низкое потребление пищи ( голодание ), диеты с ограничением углеводов , голодание , длительные интенсивные физические упражнения , [5] алкоголизм или при нелеченном (или неадекватно леченном) сахарном диабете 1 типа . Кетоновые тела образуются в клетках печени в результате распада жирных кислот. [6] Они попадают в кровь после гликогена истощения запасов в печени. (Запасы гликогена обычно истощаются в течение первых 24 часов голодания.) [2]
Кетоновые тела также производятся в глиальных клетках в периоды ограничения питания для поддержания формирования памяти. [7]
Когда две молекулы ацетил-КоА теряют свои -КоА (или группы кофермента А ), они могут образовывать (ковалентный) димер , называемый ацетоацетатом. β-гидроксибутират — это восстановленная форма ацетоацетата, в которой кетоновая группа превращается в спиртовую (или гидроксильную ) группу (см. иллюстрацию справа). Оба представляют собой четырехуглеродные молекулы, которые могут быть легко преобразованы обратно в ацетил-КоА в большинстве тканей организма, за исключением печени. Ацетон — это декарбоксилированная форма ацетоацетата, которая не может быть преобразована обратно в ацетил-КоА, за исключением процесса детоксикации в печени, где он превращается в молочную кислоту , которая, в свою очередь, может быть окислена в пировиноградную кислоту и только затем в ацетил-КоА.
Кетоновые тела имеют характерный запах, который легко уловить в дыхании людей, находящихся в состоянии кетоза и кетоацидоза . Его часто называют фруктовым или похожим на жидкость для снятия лака (которая обычно содержит ацетон или этилацетат ).
Помимо трех эндогенных кетоновых тел, , могут образовываться другие кетоновые тела, такие как β-кепентаноат и β-гидроксипентаноат в результате метаболизма синтетических триглицеридов , таких как тригептаноин .
Производство
[ редактировать ]
Жиры, хранящиеся в жировой ткани, высвобождаются из жировых клеток в кровь в виде свободных жирных кислот и глицерина, когда уровень инсулина низкий, а уровень глюкагона и адреналина в крови высокий. Это происходит между приемами пищи, во время голодания, голодания и напряженных физических упражнений, когда уровень глюкозы в крови может упасть. Жирные кислоты являются очень высокоэнергетическим топливом и поглощаются всеми метаболизирующими клетками, имеющими митохондрии . Это связано с тем, что жирные кислоты могут метаболизироваться только в митохондриях. [2] [8] Эритроциты не содержат митохондрий и поэтому полностью зависят от анаэробного гликолиза для удовлетворения своих энергетических потребностей. Во всех других тканях жирные кислоты, попадающие в метаболизирующие клетки, соединяются с коферментом А с образованием ацил-КоА цепей . Они переносятся в митохондрии клеток, где расщепляются на единицы ацетил-КоА в результате последовательности реакций, известных как β-окисление . [2] [8]
Ацетил-КоА, образующийся в результате β-окисления, входит в цикл лимонной кислоты в митохондриях, соединяясь с оксалоацетатом с образованием цитрата . В результате происходит полное сгорание ацетильной группы ацетил-КоА (см. схему выше справа) до CO 2 и воды. Энергия, выделяющаяся при этом процессе, улавливается в виде 1 молекулы ГТФ и 9 молекул АТФ на одну окисленную ацетильную группу (или молекулу уксусной кислоты ). [2] [8] Такова судьба ацетил-КоА везде, где происходит β-окисление жирных кислот, за исключением определенных обстоятельств в печени . В печени оксалоацетат полностью или частично перенаправляется по глюконеогенному пути при голодании, голодании, низкоуглеводной диете, длительных физических нагрузках и при неконтролируемом сахарном диабете 1 типа . В этих условиях оксалоацетат гидрируется до малата , который затем удаляется из митохондрий и превращается в глюкозу в цитоплазме клеток печени, откуда глюкоза высвобождается в кровь. [2] Таким образом, в печени оксалоацетат недоступен для конденсации с ацетил-КоА, когда значительный глюконеогенез стимулируется низким (или отсутствующим) уровнем инсулина и высокими концентрациями глюкагона в крови. В этих условиях ацетил-КоА направляется на образование ацетоацетата и бета-гидроксибутират. [2] Ацетоацетат, бета-гидроксибутират и продукт их самопроизвольного распада ацетон. [9] известны как кетоновые тела. Кетоновые тела выбрасываются печенью в кровь. Все клетки с митохондриями могут забирать кетоновые тела из крови и превращать их в ацетил-КоА, который затем можно использовать в качестве топлива в циклах лимонной кислоты, поскольку никакая другая ткань не может направить свой оксалоацетат в глюконеогенный путь так, как это происходит с митохондриями. это делает печень. В отличие от свободных жирных кислот, кетоновые тела могут преодолевать гематоэнцефалический барьер и поэтому доступны в качестве топлива для клеток центральной нервной системы , действуя в качестве заменителя глюкозы, на которой эти клетки обычно выживают. [2] Возникновение высокого уровня кетоновых тел в крови при голодании, низкоуглеводной диете и длительных тяжелых физических нагрузках может привести к кетозу, а в такой крайней форме – к вышедшему из-под контроля сахарному диабету 1 типа, как кетоацидоз .
Ацетоацетат имеет весьма характерный для людей запах, который появляется в дыхании и моче во время кетоза. С другой стороны, большинство людей чувствуют запах ацетона, «сладко-фруктовый» запах которого также характерен для дыхания людей, находящихся в состоянии кетоза или, особенно, кетоацидоза. [10]
Использование топлива в различных органах
[ редактировать ]Кетоновые тела могут использоваться в качестве топлива для сердца , мозга и мышц , но не для печени . они дают 2 молекулы гуанозинтрифосфата (ГТФ) и 22 молекулы аденозинтрифосфата При окислении в митохондриях (АТФ) на молекулу ацетоацетата. Кетоновые тела транспортируются из печени в другие ткани, где ацетоацетат и β-гидроксибутират могут быть повторно преобразованы в ацетил-КоА с образованием восстанавливающих эквивалентов ( НАДН и ФАДН 2 ) посредством цикла лимонной кислоты. Хотя печень является источником кетоновых тел, она не может использовать их для получения энергии, поскольку в ней отсутствует фермент тиофораза (β-кетоацил-КоА-трансфераза). Ацетон поглощается печенью в низких концентрациях и подвергается детоксикации по метилглиоксальному пути , который заканчивается лактатом. Ацетон в высоких концентрациях, что может произойти при длительном голодании или кетогенной диете, поглощается клетками вне печени и метаболизируется другим путем через пропиленгликоль . Хотя этот путь следует другой серии шагов, требующих АТФ, пропиленгликоль в конечном итоге может быть превращен в пируват. [11]
Сердце
[ редактировать ]Сердце преимущественно использует жирные кислоты в качестве топлива при нормальных физиологических условиях. Однако в условиях кетоза сердце может эффективно использовать для этой цели кетоновые тела. [12]
Мозг
[ редактировать ]В течение нескольких десятилетий печень считалась основным поставщиком кетоновых тел, необходимых для энергетического метаболизма мозга. Однако недавние данные показали, что глиальные клетки могут подпитывать нейроны локально синтезируемыми кетоновыми телами для поддержания формирования памяти при ограничении еды. [3]
Мозг получает часть своих потребностей в топливе из кетоновых тел, когда глюкоза менее доступна, чем обычно. В случае низкой концентрации глюкозы в крови большинство других тканей имеют альтернативные источники топлива, помимо кетоновых тел и глюкозы (например, жирных кислот), но исследования показали, что мозгу обязательно требуется некоторое количество глюкозы. [13] После строгого голодания в течение 3 дней мозг получает 25% энергии из кетоновых тел. [14] Примерно через 24 дня кетоновые тела становятся основным топливом мозга, составляя до двух третей потребления топлива мозгом. [15] Многие исследования предполагают, что клетки человеческого мозга могут выжить с небольшим количеством глюкозы или вообще без нее, но доказательство этой точки зрения сомнительно с этической точки зрения . [15] На начальных стадиях кетоза мозг не сжигает кетоны, поскольку они являются важным субстратом для синтеза липидов в мозге. Кроме того, кетоны, полученные из жирных кислот омега-3, могут уменьшить ухудшение когнитивных функций в пожилом возрасте . [16]
Кетогенез способствовал увеличению человеческого мозга в ходе его эволюции. Ранее предполагалось, что кетогенез является ключом к эволюции и жизнеспособности более крупного мозга в целом. Однако потеря HMGCS2 (и, следовательно, этой способности) у трех линий млекопитающих с большим мозгом ( китообразные , слоны - мастодонты , летучие мыши Старого Света ) показывает обратное. Из трех линий только летучие мыши обладают ожидаемой чувствительностью к голоданию; двое других нашли альтернативные способы подпитки организма во время голодания. [17]
Кетоз и кетоацидоз
[ редактировать ]У нормальных людей происходит постоянное производство кетоновых тел печенью и их утилизация внепеченочными тканями. Концентрация кетоновых тел в крови поддерживается на уровне около 1 мг/дл . Их экскреция с мочой очень низкая и не обнаруживается обычными анализами мочи (проба Ротеры). [18]
Когда скорость синтеза кетоновых тел превышает скорость утилизации, их концентрация в крови увеличивается; это известно как кетонемия . За этим следует кетонурия – выделение кетоновых тел с мочой. Общую картину кетонемии и кетонурии обычно называют кетозом. Запах ацетоацетата и/или ацетона в выдыхаемом воздухе является частым признаком кетоза.
Когда диабетик 1 типа страдает от острого биологического стресса (инфекция, сердечный приступ или физическая травма) или ему не удается ввести достаточное количество инсулина, он может перейти в патологическое состояние диабетического кетоацидоза . В этих обстоятельствах низкий уровень инсулина или его отсутствие в крови в сочетании с неадекватно высокими концентрациями глюкагона [19] Заставляют печень производить глюкозу с неадекватно повышенной скоростью, вызывая превращение ацетил-КоА, образующегося в результате бета-окисления жирных кислот, в кетоновые тела. Возникающий в результате очень высокий уровень кетоновых тел снижает pH плазмы крови, что рефлекторно заставляет почки выделять мочу с очень высоким уровнем кислоты. Высокие уровни глюкозы и кетонов в крови также пассивно попадают в мочу (из-за неспособности почечных канальцев реабсорбировать глюкозу и кетоны из канальцевой жидкости, поскольку они подавляются большими объемами этих веществ, фильтрующихся в канальцевую жидкость). ). Возникающий в результате осмотический диурез глюкозы вызывает удаление воды и электролитов из крови, что приводит к потенциально смертельному обезвоживанию .
У людей, соблюдающих низкоуглеводную диету, также развивается кетоз. Этот индуцированный кетоз иногда называют пищевым кетозом , но уровень концентрации кетонов в организме составляет порядка 0,5–5 мМ , тогда как патологический кетоацидоз составляет 15–25 мМ . [ нужна ссылка ]
Процесс кетоза изучался на предмет его влияния на улучшение когнитивных симптомов нейродегенеративных заболеваний, включая болезнь Альцгеймера . [20] Клинические испытания также изучали кетоз у детей при синдроме Ангельмана . [21]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Кэхилл, Джордж Ф.; Вич, Ричард Л. (2003). «Кетокислоты? Хорошее лекарство?» . Труды Американской клинической и климатологической ассоциации . 114 : 149–161, обсуждение 162–163. ISSN 0065-7778 . ПМК 2194504 . ПМИД 12813917 .
- ^ Jump up to: а б с д и ж г час Страйер, Люберт (1995). Биохимия (Четвертое изд.). Нью-Йорк: WH Freeman and Company. стр. 510–515, 581–613, 775–778. ISBN 0-7167-2009-4 .
- ^ Jump up to: а б Сильва Б., Манта О.Л., Шор Дж., Паскуаль А., Пласэ П.Ю., Павловский А. и Преат Т. (2022). Глия подпитывает нейроны локально синтезируемыми кетоновыми телами для поддержания памяти в условиях голодания. Природный метаболизм, 4 (2), 213–224. https://doi.org/10.1038/s42255-022-00528-6. Архивировано 6 марта 2024 г. в Wayback Machine.
- ^ Мэри К. Кэмпбелл; Шон О. Фаррелл (2006). Биохимия (5-е изд.). Cengage Обучение. п. 579 . ISBN 0-534-40521-5 .
- ^ Коэслаг, Дж. Х.; Ноукс, Т.Д.; Слоан, AW (1980). «Посттренировочный кетоз» . Журнал физиологии . 301 : 79–90. doi : 10.1113/jphysicalol.1980.sp013190 . ПМЦ 1279383 . ПМИД 6997456 .
- ^ Берг, Джереми (2019). Биохимия (9-е изд.). Макмиллан. п. 724. ИСБН 9781319402853 .
- ^ Сильва, Брайон; Манта, Оливье Л.; Шор, Иоганн; Паскуаль, Альберто; Пласе, Пьер-Ив; Павловский, Алиса; Преат, Томас (17 февраля 2022 г.). «Глия подпитывает нейроны локально синтезируемыми кетоновыми телами для поддержания памяти в условиях голодания» . Природный метаболизм . 4 (2): 213–224. дои : 10.1038/s42255-022-00528-6 . ПМЦ 8885408 . ПМИД 35177854 .
- ^ Jump up to: а б с «Окисление жирных кислот» . 11 октября 2013 г. Архивировано из оригинала 08 января 2018 г. Проверено 17 декабря 2015 г.
- ^ Метаболизм кетонового тела. Архивировано 22 сентября 2016 г. в Wayback Machine , Университет Ватерлоо.
- ^ «Американская диабетическая ассоциация – кетоацидоз» . Архивировано из оригинала 29 апреля 2010 г. Проверено 2 марта 2010 г.
- ^ «Архивная копия» (PDF) . Архивировано из оригинала (PDF) 24 сентября 2015 г. Проверено 18 сентября 2013 г.
{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка ) - ^ Кодде И.Ф., ван дер Сток Дж., Смоленский Р.Т., де Йонг Дж.В. (январь 2007 г.). «Метаболическая и генетическая регуляция предпочтения субстрата сердечной энергии». Комп. Биохим. Физиол. А. 146 (1): 26–39. дои : 10.1016/j.cbpa.2006.09.014 . ПМИД 17081788 .
- ^ Кларк, Д.Д.; Соколофф, Л (1999). «Субстраты церебрального метаболизма». В Сигеле, Дж. Дж.; Агранов, Б.В.; Альберс, Р.В. (ред.). Базовая нейрохимия: молекулярные, клеточные и медицинские аспекты (6-е изд.). Филадельфия: Липпинкотт-Рэйвен. Архивировано из оригинала 23 марта 2019 г. Проверено 2 сентября 2017 г.
- ^ Хассельбальх, С.Г.; Кнудсен, генеральный менеджер; Якобсен, Дж; Хагеман, LP; Холм, С; Полсон, О.Б. (1994). «Мозговой метаболизм при кратковременном голодании у человека» . Журнал церебрального кровотока и метаболизма . 14 (1): 125–31. дои : 10.1038/jcbfm.1994.17 . ПМИД 8263048 .
- ^ Jump up to: а б Кэхилл Г.Ф. Топливный обмен при голодании. Анну Рев Нутр 2006; 26: 1–22.
- ^ Фримантл, Э.; Вандал, Миннесота; Трамбле-Мерсье, Дж.; Трамбле, SB; Блашер, Дж. К.; Бегин, МЭ; Томас Бренна, Дж.; Виндуст, А.; Каннейн, Южная Каролина (2006). «Жирные кислоты омега-3, энергетические субстраты и функция мозга во время старения». Простагландины, лейкотриены и незаменимые жирные кислоты . 75 (3): 213–20. дои : 10.1016/j.plefa.2006.05.011 . ПМИД 16829066 .
- ^ Джебб, Дэвид; Хиллер, Майкл (16 октября 2018 г.). «Периодическая потеря HMGCS2 показывает, что кетогенез не важен для эволюции мозга крупных млекопитающих» . электронная жизнь . 7 : е38906. doi : 10.7554/eLife.38906 . ПМК 6191284 . ПМИД 30322448 .
- ^ Комсток, Джон П.; Гарбер, Алан Дж. (1990). Уокер, Х. Кеннет; Холл, В. Даллас; Херст, Дж. Уиллис (ред.). Клинические методы: история, физические и лабораторные исследования (3-е изд.). Бостон: Баттервортс. ISBN 040990077X . ПМИД 21250091 . Архивировано из оригинала 10 сентября 2017 г. Проверено 19 декабря 2017 г.
- ^ Коэслаг, Дж. Х.; Сондерс, ПТ; Тербланш, Э. (2003). «Тематический обзор: переоценка гомеостата глюкозы в крови, которая всесторонне объясняет комплекс сахарный диабет 2 типа/синдром X» . Журнал физиологии . 549 (Часть 2): 333–346. дои : 10.1113/jphysicalol.2002.037895 . ПМК 2342944 . ПМИД 12717005 .
- ^ Дженсен, Нью-Джерси; Водшоу, Герцогия; Нильссон, М; Рунгби, Дж. (20 ноября 2020 г.). «Влияние кетоновых тел на метаболизм и функцию мозга при нейродегенеративных заболеваниях» . Международный журнал молекулярных наук . 21 (22): 8767. doi : 10.3390/ijms21228767 . ПМЦ 7699472 . ПМИД 33233502 .
- ^ «Оценка безопасности и переносимости пищевой смеси при синдроме Ангельмана» . 18 августа 2020 года. Архивировано из оригинала 9 февраля 2022 года . Проверено 9 февраля 2022 г.
Внешние ссылки
[ редактировать ]- неотложная помощь / 135 в электронной медицине - диабетический кетоацидоз
- Жировой обмен на unisanet.unisa.edu.au
- Кетон + Тела в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- Макгуайр, LC; Круикшанк, AM; Манро, П.Т. (2006). «Алкогольный кетоацидоз» . Журнал неотложной медицины . 23 (6): 417–420. дои : 10.1136/emj.2004.017590 . ПМЦ 2564331 . ПМИД 16714496 .