Гидроборирование, катализируемое металлами
В химии гидроборирование, катализируемое металлами, — это реакция, используемая в органическом синтезе . Это один из нескольких примеров гомогенного катализа .
История
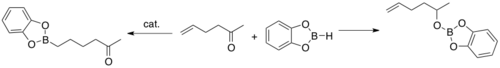
[ редактировать ]В 1975 году Коно и Ито сообщили, что катализатор Уилкинсона (Rh(PPh 3 ) 3 Cl) может подвергаться окислительному присоединению с катехолбораном (HBcat) или 4,4,6-триметил-1,3,2-диоксаборинаном. [ 1 ] В остальном эти два соединения борана медленно участвуют в гидроборировании. [ 2 ] [ 3 ] В 1985 году Мэнниг и Нёт впервые продемонстрировали, что катализатор Уилкинсона действительно катализирует гидроборирование алкенов с помощью HBcat.
В то время как некатализируемое гидроборирование с использованием HBcat приводит к восстановлению карбонильной группы, каталитическая версия является селективной по отношению к алкену. [ 4 ]
Как показали последующие исследования, гидроборирование, катализируемое переходными металлами, протекает с привлекательной функциональной групповой, регио-, стерео- и хемоселективностью.
Механизм
[ редактировать ]Считается, что реакция гидроборирования, катализируемая родием, инициируется диссоциацией трифенилфосфина из центра Rh(I). Окислительное присоединение связи BH боранового реагента к этому 14 e − затем следует координация алкена с 16e − Гидридный комплекс Rh(III). Последующее мигрирующее внедрение алкена по родий-гидридной связи может привести к образованию двух региоизомерных алкилборидных комплексов родия (III). Восстановительное удаление боронатного эфира регенерирует катализатор. Катализатор, приготовленный и обработанный в анаэробных условиях, меняет селективность в пользу вторичного боронатного эфира. Спорным является координация алкена. В диссоциативном механизме, предложенном Мэннигом и Нётом, [ 4 ] при поддержке Эванса и Фу [ 5 ] координация сопровождается потерей одного трифенилфосфинового лиганда.
В ассоциативном механизме (см. ниже), предложенном Берджесом и др., [ 6 ] алкен связывает транс с хлоридом без диссоциации трифенилфосфинового лиганда. Механизм изучен вычислительными методами. [ 7 ] [ 8 ] Дориго и Шлейер исключили ассоциативный механизм в результате ab initio исследования диссоциативного механизма. [ 9 ] тогда как Мусаев и сотрудники поддерживают ассоциативный механизм. [ 10 ]
Селективность
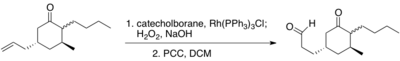
[ редактировать ]Помимо оригинальных доказательств, предоставленных Мэннигом и Нётом, полный синтез (+)-птилокаулина также демонстрирует селективное гидроборирование концевого алкена в присутствии кетона. [ 11 ]
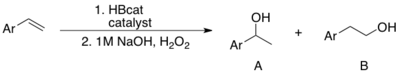
По региоселективности катализируемое гидроборирование отличается от некаталитического аналога. В зависимости от лигандов и алкена образуется либо марковниковский, либо антимарковниковский продукт. Разница в региоселективности более выражена при гидроборировании виниларенов HBcat. Катализатор Уилкинсона или катион Rh(COD) 2 (в присутствии PPh 3 ) дает продукт Марковникова . [ 12 ] [ 13 ] Антимарковниковский продукт производится без катализатора. [ 14 ] Стоит отметить, что использование RhCl 3 ·nH2O избирательно приводит к образованию антимарковниковского продукта. [ 15 ] Чтобы объяснить высокую региоселективность каталитического гидроборирования, Хаяши предложил механизм, включающий η 3 -бензилродиевый комплекс. [ 12 ]
Катализируемое гидроборирование-окисление замещенных алкенов можно сделать энантиоселективным. В 1990 году Браун и его коллеги добились асимметричного гидроборирования, используя ахиральный катализатор и источники хирального борана, полученные из эфедрина и псевдоэфедрина. В большинстве случаев региоселективность была плохой, хотя значения ee могут приближаться к 90%. [ 16 ]
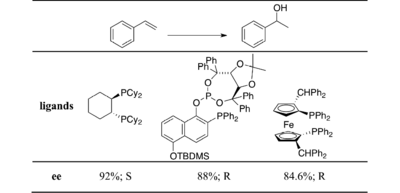
Более распространено использование хирального катализатора и ахирального источника борана, например хиральных дифосфинов, таких как BINAP . [ 17 ] [ 18 ] [ 19 ]
стирол или его простые производные. Прохиральным субстратом обычно является [ 20 ] [ 21 ] [ 22 ]
Энантиоселективность имеет тенденцию снижаться при наличии орто -заместителей в ароматическом кольце, а также при дальнейшем замещении олефина. Успешные результаты были получены и на других реагентах. [ 23 ] [ 24 ] Второй класс лигандов — фосфинаминовые лиганды. В 1993 году Браун впервые сообщил об успешном использовании QUINAP в асимметричном гидроборировании алкенов. [ 25 ] QUINAP улучшает непереносимость замещения в ароматическом кольце, как это наблюдается в случае дифосфиновых лигандов. Реакции с использованием стирола и его производных с электронодонорными группами в пара-положении все еще давали высокие значения ee. Аналогичные результаты были получены и на циклических виниларенах. Такие результаты расширяют сферу применения асимметричного гидроборирования на более стерически требовательные алкены. Также было разработано несколько новых лигандов этого класса. Некоторые недавние результаты кратко изложены ниже. [ 26 ] [ 27 ] [ 28 ]
Во всех вышеприведенных исследованиях использовалось окисление боронатных эфиров для получения спиртов, что является серьезным ограничением синтетических возможностей таких видов, особенно когда их можно получать энантиоселективно. Другим важным классом соединений, которые могут быть получены из боронатных эфиров, являются α-замещенные бензиламины , некоторые из которых коммерчески полезны. Синтез таких хиральных аминов путем каталитического гидроборирования включает превращение сложного эфира катехолбороната в триалкилборан диэтилцинком или хлоридом метилмагния. Реакция триалкилборана с гидроксиламин-О-сульфоновой кислотой дает первичные бензиламины. [ 29 ] Вторичные амины также можно получить путем образования N- хлораминов in situ . [ 30 ]
Ссылки
[ редактировать ]- ^ . Коно, Х.; Ито, К. (1975). «Окислительное присоединение 4,4,6-триметил-1,3,2-диоксаборинана и бензо[1,3,2]диоксаборола к трис (трифенилфосфин)галогенродию». Химические письма . 4 (10): 1095–1096. дои : 10.1246/кл.1975.1095 .
- ^ Браун, ХК; Гупта, СК (1971). «1,3,2-Безодиоксаборол, удобный монофункциональный гидроборирующий агент. Простой новый синтез алканбороновых эфиров и кислот из олефинов посредством гидроборирования». Журнал Американского химического общества . 93 (7): 1816–1818. дои : 10.1021/ja00736a061 .
- ^ Фиш, Р.Х. (1973). «Относительные скорости гидроборирования некоторых олефинов 4,4,6-триметил-1,3,2-диоксаборинаном». Журнал органической химии . 38 : 158–159. дои : 10.1021/jo00941a037 .
- ^ Перейти обратно: а б Мэннинг, Д.; Нёт, Х. (1985). «Каталитическое гидроборирование комплексами родия». Angewandte Chemie, международное издание . 24 (10): 878–879. дои : 10.1002/anie.198508781 .
- ^ Эванс, Д.А.; Фу, ГК; Андерсон, бакалавр (1992). «Механистическое исследование реакции гидроборирования, катализируемой родием (I)». Журнал Американского химического общества . 114 (17): 6679–6685. дои : 10.1021/ja00043a010 .
- ^ Берджесс, К.; Ван дер Донк, Вашингтон; Весткотт, SA; Мардер, ТБ; Томас Бейкер, Р.; Калабрезе, Дж. К. (1992). «Реакции катехолборана с катализатором Уилкинсона: значение для гидроборирования алкенов, катализируемого переходными металлами». Журнал Американского химического общества . 114 (24): 9350–9359. дои : 10.1021/ja00050a015 .
- ^ Видауэр, К.; Грюцмахер, Х.; Зиглер, Т. (2000). «Сравнительное функциональное исследование ассоциативных и диссоциативных механизмов в реакциях гидроборирования олефинов, катализируемых родием (I)». Металлоорганические соединения . 19 (11): 2097–2107. дои : 10.1021/om9909946 .
- ^ Хуан, X.; Лин, З.Ы. (2002). Компьютерное моделирование гомогенного катализа . Нью-Йорк: Издательство Kluwer Academic Publishers. стр. 189–212. ISBN 1-4020-0933-Х .
- ^ Дориго, А.Е.; Шлейер, PR (1995). «Исследование Ab initio катализируемого RhI гидроборирования связей C=C: доказательства миграции водорода на ключевом этапе». Angewandte Chemie, международное издание . 34 : 115–118. дои : 10.1002/anie.199501151 .
- ^ Мусаев, Д.Г.; Мебель, АМ; Морокума, К. (1994). «Изначальное молекулярно-орбитальное исследование механизма реакции гидроборирования олефинов, катализируемой родием (I)». Журнал Американского химического общества . 116 (23): 10693–10702. дои : 10.1021/ja00102a039 .
- ^ Джанин, К.; БузБуз, С. (1996). «Короткий доступ к (+)-птилокалину». Буквы тетраэдра . 37 (29): 5091–5094. дои : 10.1016/0040-4039(96)01032-5 .
- ^ Перейти обратно: а б Хаяши, Т.; Мацумото, Ю.; Ито, Ю. (1991). «Асимметричное гидроборирование стирола, катализируемое катионными хиральными комплексами фосфин-родий (I)». Тетраэдр: Асимметрия . 2 (7): 601–612. дои : 10.1016/S0957-4166(00)86112-1 .
- ^ Чжан, Дж.; Лу, Б.; Го, Г.; Дай, Л. (1991). «Обратная региохимия при гидроборировании виниларенов, катализируемом комплексами нейтрального родия, и связанная с ним асимметричная версия». Журнал органической химии . 56 (4): 1670–1672. дои : 10.1021/jo00004a060 .
- ^ Пельтер, А.; Смит, К. (1979). Комплексная органическая химия, Том. III . Нью-Йорк: Пергамон Пресс.
- ^ Моррилл, ТК; Д'Суза, Калифорния; Ян, Л.; Сампоньяро, Эй Джей (2002). «Гидроборирование алкенов, промотируемое переходными металлами: уникальное изменение региоселективности». Журнал органической химии . 67 : 2481–2484. дои : 10.1021/jo0109321 .
- ^ Браун, Дж. М.; Ллойд-Джонс, GC (1990). «Каталитическое асимметричное гидроборирование оксазаборолидинами». Тетраэдр: Асимметрия . 1 (12): 869–872. дои : 10.1016/S0957-4166(00)82276-4 .
- ^ Хаяши, Т.; Мацумото, Ю.; Ито, Ю. (1989). «Каталитическое асимметричное гидроборирование стирола». Журнал Американского химического общества . 111 (9): 3426–3428. дои : 10.1021/ja00191a049 .
- ^ Берджесс, К.; Олмейер, MJ (1988). «Энантиоселективное гидроборирование, опосредованное гомохиральными родиевыми катализаторами». Журнал органической химии . 53 (21): 5178–5179. дои : 10.1021/jo00256a059 .
- ^ Сато, М.; Мияура, Н. ; Сузуки, А. (1990). «Асимметричное гидроборирование алкенов, катализируемое родием (i), 1,3,2-бензодиоксаборолом». Буквы тетраэдра . 31 (2): 231–234. doi : 10.1016/S0040-4039(00)94379-X .
- ^ Демей, С.; Волант, Ф.; Кнохель, П. (2001). «Новые C 2 -симметричные 1,2-дифосфаны для эффективного родий-катализируемого асимметричного гидроборирования производных стирола». Angewandte Chemie, международное издание . 40 : 1235. doi : 10.1002/1521-3773(20010401)40:7<1235::aid-anie1235>3.0.co;2-y .
- ^ Блюм, Ф.; Земолка, С.; Фей, Т.; Кранич Р.; Шмальц, Х.Г. (2002). «Идентификация подходящих лигандов для реакции, катализируемой переходными металлами: скрининг модульной библиотеки лигандов при энантиоселективном гидроборировании стирола». Расширенный синтез и катализ . 344 : 868. doi : 10.1002/1615-4169(200209)344:8<868::aid-adsc868>3.0.co;2-m .
- ^ Ритц, Монтана; Бюттенмюллер, EW; Годдард, Р.; Пасто, М. (1999). «Новый класс хиральных дифосфинов, обладающих планарной хиральностью». Буквы тетраэдра . 40 (27): 4977–4980. дои : 10.1016/S0040-4039(99)00947-8 .
- ^ Рубина Р.; Рубин, М.; Геворкян (2003). «Каталитическое энантиоселективное гидроборирование циклопропенов». Журнал Американского химического общества . 125 (24): 7198–7199. дои : 10.1021/ja034210y . ПМИД 12797792 .
- ^ Перес Луна, А.; Бонин, М.; Микуэн, Л.; Хассон, Х.-П. (2002). «Обращение энантиоселективности в асимметричном гидроборировании мезосубстратов, катализируемом родием и иридием» (PDF) . Журнал Американского химического общества . 124 (41): 12098–12099. дои : 10.1021/ja026714m .
- ^ Алкок, Северо-Запад; Браун, Дж. М.; Халмс, Д.И. (1993). «Синтез и разделение 1-(2-дифенилфосфино-1-нафтил)изохинолина; P,N-хелатирующего лиганда для асимметричного катализа». Тетраэдр: Асимметрия . 4 : 743–756. дои : 10.1016/S0957-4166(00)80183-4 .
- ^ Клёцинг, Р.Дж.; Лотц, М.; Кнохель, П. (2003). «Новые P,N-ферроценильные лиганды для гидроборирования, катализируемого родием, и аллилового алкилирования, катализируемого палладием». Тетраэдр: Асимметрия . 14 (2): 255–264. дои : 10.1016/S0957-4166(02)00827-3 .
- ^ Квонг, Финляндия; Ян, королевский адвокат; Мак, TCW; Чан, ASC; Чан, К.С. (2002). «Новый атропоизомерный P,N-лиганд для асимметричного гидроборирования, катализируемого родием». Журнал органической химии . 67 (9): 2769–2777. дои : 10.1021/jo0159542 .
- ^ Сын, СУ; Джанг, HY; Хан, JW; Ли, И.С.; Чанг, Ю.К. (1999). «Новые плоские хиральные P,N-лиганды, содержащие трикарбонил(арен)хром, для энантиоселективного асимметричного гидроборирования стиролов». Асимметрия тетраэдра . 10 (2): 347–354. дои : 10.1016/S0957-4166(99)00005-1 .
- ^ Фернандес, Э.; Хупер, МВт; Найт, Финляндия; Браун, Дж. М. (1997). «Каталитическое асимметричное гидроборирование – аминирование». Химические коммуникации (2): 173. doi : 10.1039/A606827H .
- ^ Фернандес, Э.; Маэда, К.; Хупер, МВт; Браун, Дж. М. (2000). «Каталитическое асимметрическое гидроборирование/аминирование и алкилирование родиевыми комплексами 1,1'-(2-диарилфосфино-1-нафтил)изохинолина». Химия: Европейский журнал . 6 : 1840. doi : 10.1002/(sici)1521-3765(20000515)6:10<1840::aid-chem1840>3.0.co;2-6 .