Этерификация Шиины
Этерификация Шиина — это органическая химическая реакция карбоновых кислот синтезируются , в ходе которой сложные эфиры из почти равных количеств карбоновых кислот и спиртов с использованием ангидридов ароматических карбоновых кислот в качестве агентов дегидратационной конденсации . В 1994 году профессор Исаму Сиина ( Токийский университет науки , Япония) сообщил о методе кислотного сочетания с использованием кислоты Льюиса . [ 1 ] [ 2 ] и в 2002 г. - основная этерификация с использованием нуклеофильного катализатора. [ 3 ] [ 4 ]
Механизм
[ редактировать ]Последовательное добавление карбоновых кислот и спиртов в систему, содержащую ангидрид ароматической карбоновой кислоты и катализатор, дает соответствующие эфиры карбоновых кислот посредством процесса, показанного на следующем рисунке. При кислой этерификации Шиины используют катализаторы на основе кислот Льюиса, а при этерификации Шиины в основных условиях используют нуклеофильные катализаторы.
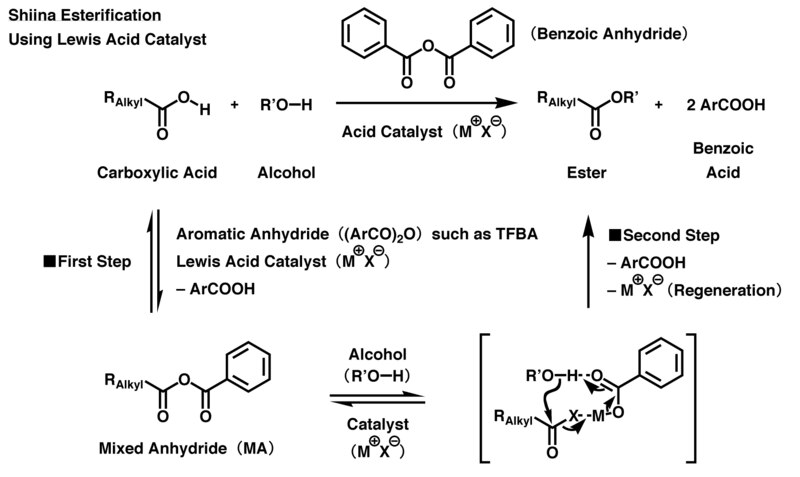
В кислой реакции в качестве агента дегидратационной конденсации в основном используется 4-трифторметилбензойный ангидрид (TFBA). Сначала катализатор на основе кислоты Льюиса активирует TFBA, а затем карбоксильная группа в карбоновой кислоте реагирует с активированным TFBA с однократным образованием смешанного ангидрида (МА). Затем карбонильная группа, полученная из карбоновой кислоты в МА, избирательно активируется и подвергается атаке гидроксильной группы спирта посредством межмолекулярного нуклеофильного замещения. Одновременно остаточная соль ароматической карбоновой кислоты, полученная из МА, действует как агент депротонирования , вызывая развитие этерификации и образование желаемого эфира карбоновой кислоты. Чтобы сбалансировать реакцию, каждый TFBA принимает атомы одной молекулы воды из своих исходных материалов, т.е. карбоновой кислоты и спирта, а затем в конце реакции превращается в две молекулы 4-трифторметилбензойной кислоты. Поскольку катализатор на основе кислоты Льюиса воспроизводится в конце реакции, для продвижения реакции требуется лишь небольшая часть катализатора по отношению к исходному материалу.

В основной реакции 2-метил-6-нитробензойный ангидрид ( MNBA ). в качестве агента дегидратационной конденсации в основном используется [ 5 ] Во-первых, нуклеофильный катализатор воздействует на МНБА с образованием активированного ацилкарбоксилата. Реакция карбоксильной группы карбоновой кислоты с активированным ацилкарбоксилатом дает соответствующий МА так же, как и в кислой реакции. Затем нуклеофильный катализатор избирательно действует на карбонильную группу, полученную из карбоновой кислоты в МА, снова образуя активированный ацилкарбоксилат. Гидроксильная группа спирта атакует молекулу-хозяина путем межмолекулярного нуклеофильного замещения, и в то же время карбоксилат-анион, полученный из 2-метил-6-нитробензойной кислоты, действует как агент депротонирования , способствуя развитию этерификации и образуя желаемый эфир карбоновой кислоты. Чтобы сбалансировать реакцию, каждый MNBA принимает атомы одной молекулы воды из своих исходных материалов, превращаясь в две молекулы аминной соли 2-метил-6-нитробензойной кислоты и, таким образом, прекращая реакцию. Поскольку нуклеофильный катализатор воспроизводится в конце реакции, требуются лишь небольшие стехиометрические количества.
Подробности
[ редактировать ]Все процессы этерификации Шиины представляют собой обратимые реакции, за исключением последней стадии нуклеофильного замещения спиртом. Следовательно, в системе сосуществуют ангидрид ароматической карбоновой кислоты и смешанный ангидрид (МА). Кроме того, в системе одновременно присутствует ангидрид алифатической карбоновой кислоты, полученный диспропорционированием МА; таким образом, его используют непосредственно в виде смеси без разделения. Благодаря активации кислотными катализаторами Льюиса или нуклеофильными катализаторами смесь этих трех компонентов начинает реагировать со спиртом; Помимо целевых эфиров алифатических карбоновых кислот, в качестве побочных продуктов могут образовываться эфиры ароматических карбоновых кислот.
Однако при использовании ангидрида 4-трифторметилбензойной кислоты (TFBA) в качестве ангидрида ароматической карбоновой кислоты в кислых условиях и ангидрида 2-метил-6-нитробензойной кислоты (MNBA) в качестве ангидрида ароматической карбоновой кислоты в основных условиях практически не получаются сложные эфиры ароматических карбоновых кислот. в качестве побочных продуктов. (Хемоселективность составляет 200:1 или выше.)
Ангидриды ароматических карбоновых кислот используются в качестве агентов дегидратационной конденсации не только для межмолекулярного сочетания карбоновых кислот со спиртами, но и для внутримолекулярной циклизации гидроксикарбоновых кислот ( макролактонизация Шиина ). Обе эти межмолекулярные и внутримолекулярные реакции используются для искусственного синтеза различных природных продуктов и фармакологически активных соединений. [ 6 ] [ 7 ] поскольку реакция карбоновой кислоты с амином дает амид или пептид. [ 8 ]
В кислых реакциях высокую активность проявляют кислотные катализаторы Льюиса, такие как трифлаты металлов, тогда как в основных реакциях 4-диметиламинопиридин ( ДМАП используются ), 4-диметиламинопиридин-N-оксид (ДМАПО) и 4-пирролидинопиридин (PPY).
При этерификации Шиина, проводимой в основных условиях, асимметричный синтез реализуется с использованием хиральных нуклеофильных катализаторов. Во-первых, в присутствии хирального нуклеофильного катализатора действием соответствующего ангидрида карбоновой кислоты на рацемическую алифатическую карбоновую кислоту образуется соответствующая МА, что приводит к кинетическому разделению рацемической алифатической карбоновой кислоты после воздействия реакции. с ахиральным спиртом. [ 9 ] С помощью этого метода можно получить оптически активные карбоновые кислоты и оптически активные эфиры карбоновых кислот. Также возможно осуществить кинетическое разделение рацемических спиртов путем модификации составов реагентов, т.е. путем образования МА посредством реакций между ахиральной карбоновой кислотой и соответствующим ангидридом карбоновой кислоты; затем, активируя рацемические спирты с помощью МА, можно получить оптически активные спирты и оптически активные эфиры карбоновых кислот. [ 10 ]
См. также
[ редактировать ]- Макролактонизация Шиины
- Этерификация Фишера-Шпейера
- Этерификация Стеглиха
- Этерификация Ямагучи
- Реакция Мицунобу
Ссылки
[ редактировать ]- ^ Шиина, И.; Миёси, С.; Мияшита, М.; Мукаяма, Т. (1994). «Полезный метод получения эфиров карбоновых кислот из свободных карбоновых кислот и спиртов». хим. Летт. 23 (3): 515–518. дои : 10.1246/кл.1994.515 .
- ^ Шиина, И. (2004). «Эффективный метод синтеза эфиров и лактонов карбоновых кислот с использованием замещенных бензойных ангидридов с катализаторами на основе кислот Льюиса». Тетраэдр . 60 (7): 1587–1599. дои : 10.1016/j.tet.2003.12.013 .
- ^ Шиина, И.; Ибука, Р.; Кубота, М. (2002). «Новая реакция конденсации для синтеза эфиров карбоновых кислот из почти эквимолярных количеств карбоновых кислот и спиртов с использованием 2-метил-6-нитробензойного ангидрида». хим. Летт. 31 (3): 286. doi : 10.1246/cl.2002.286 .
- ^ Шиина, И.; Кубота, М.; Осиуми, Х.; Хасидзуме, М. (2004). «Эффективное использование бензойного ангидрида и его производных для синтеза сложных эфиров и лактонов карбоновых кислот: мощный и удобный метод смешанного ангидрида, поддерживаемый основными катализаторами». Дж. Орг. хим. 69 (6): 1822–1830. дои : 10.1021/jo030367x . ПМИД 15058924 .
- ^ Шиина, И.; Умедзаки, Ю.; Курода, Н.; Иидзуми, Т.; Нагай, С.; Като, Т. (2012). «Образование β-лактона, опосредованное MNBA: механистические исследования и применение для асимметричного полного синтеза тетрагидролипстатина». Дж. Орг. хим. 77 (11): 4885–5701. дои : 10.1021/jo300139r . ПМИД 22553899 .
- ^ Шиина, И. (2007). «Полный синтез природных 8- и 9-членных лактонов: последние достижения в формировании колец среднего размера». хим. Откр. 107 (1): 239–273. дои : 10.1021/cr050045o . ПМИД 17212476 .
- ^ Шиина, И. (2014). «Приключенческое синтетическое путешествие с MNBA от реакционной химии к полному синтезу натуральных продуктов» . Бык. хим. Соц. Япония. 87 (2): 196–233. дои : 10.1246/bcsj.20130216 .
- ^ Шиина, И.; Усияма, Х.; Ямада, Ю.; Кавакита, Ю.; Наката, К. (2008). «4-(Диметиламино)пиридин N-оксид (ДМАПО): эффективный нуклеофильный катализатор в реакции пептидного сочетания с 2-метил-6-нитробензойным ангидридом». хим. Азиатский Дж. 3 (2): 454–461. дои : 10.1002/asia.200700305 . ПМИД 18219641 .
- ^ Шиина, И.; Наката, К.; Оно, К.; Онда, Ю.; Итагаки, М. (2010). «Кинетическое разделение рацемических α-арилалкановых кислот ахиральными спиртами посредством асимметричной этерификации с использованием карбоновых ангидридов и катализаторов ацилпереноса». Дж. Ам. хим. Соц. 132 (33): 11629–11641. дои : 10.1021/ja103490h . ПМИД 20681552 .
- ^ Шиина, И.; Наката, К.; Оно, К.; Сугимото, М.; Секигути, А. (2010). «Кинетическое разделение рацемических 2-гидроксиалканоатов с использованием энантиоселективного метода смешанного ангидрида с пивалиновым ангидридом и хиральным катализатором переноса ацила». хим. Евро. Дж. 16 (1): 167–172. дои : 10.1002/chem.200902257 . ПМИД 19904780 .
Внешние списки
[ редактировать ]- Шиина, И.; Хасидзуме, М.; Ямаи, Ю.; Осиуми, Х.; Симадзаки, Т.; Такасуна, Ю.; Ибука, Р. (2005). «Энантиоселективный полный синтез окталактина А с использованием асимметричных альдольных реакций и быстрой лактонизации с образованием кольца среднего размера». хим. Евро. Дж. 11 (22): 6601–6608. дои : 10.1002/chem.200500417 . ПМИД 16118824 .
- Швейцер, Д.; Кейн, Джей-Джей; Стрэнд, Д.; МакГенри, П.; Теннисвуд, М.; Хелквист, П. (2007). «Полный синтез иеджималида Б. Применение макролактонизации шиины». Орг. Летт. 9 (22): 4619–4622. дои : 10.1021/ol702129w . ПМИД 17915890 .
- Дас, С.; Пол, Д.; Госвами, РК (2016). «Стереоселективный тотальный синтез биоактивного морского природного продукта биселингбиолида B». Орг. Летт. 18 (8): 1908–1911. doi : 10.1021/acs.orglett.6b00713 . ПМИД 27043308 .
- М. В. Хойначка, Р. А. Батей (2018). «Полный синтез (+)-прунустатина А: полезность органотрифторборат-опосредованного пренилирования, этерификации и макролактонизации Shiina MNBA во избежание конкурирующего эффекта Торпа-Ингольда, ускоренной переэтерификации». Орг. Летт. 20 (18): 5671–5675. doi : 10.1021/acs.orglett.8b02396 . ПМИД 30160125 .
- Сюй, С.; Держал, И.; Кемпф, Б.; Майр, Х.; Стеглич, В.; Зипсе, Х. (2005). «Катализируемое DMAP ацетилирование спиртов - механистическое исследование (DMAP = 4-(диметиламино)пиридин)». хим. Евро. Дж. 11 (16): 4751–4757. дои : 10.1002/chem.200500398 . ПМИД 15924289 .