Процесс Рашига – Хукера
Процесс Рашига-Хукера — химический процесс производства хлорбензола и фенола . [ 1 ] [ 2 ]
Процесс Рашига-Хукера был запатентован Фридрихом Рашигом , немецким химиком и политиком, также известным благодаря процессу Рашига , процессу Олина Рашига и кольцу Рашига . [ 3 ] Впервые он начал использовать эту реакцию в 1891 году для производства фенола.
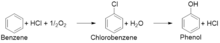
Основными этапами этого процесса являются производство хлорбензола из бензола , соляной кислоты и кислорода и последующий гидролиз хлорбензола до фенола. [ 4 ] На первом этапе используется катализатор на основе хлорида меди или железа , и материалы подвергаются воздействию воздуха при температуре 200–250 °C. [ 5 ] [ 6 ] [ 7 ] [ 8 ] На втором этапе полученный хлорбензол вводится в пар при температуре 450 °C над кремниевым катализатором, который гидролизует хлорбензол с образованием фенола и хлористого водорода, которые затем можно вернуть обратно на первый этап. [ 6 ] [ 7 ] Благодаря двухстадийности процесс Рашига-Хукера можно использовать для производства хлорбензола или фенола.

Способность процесса Рашига-Хукера производить фенол делает его сопоставимым с другими методами, такими как процесс Доу и Байера , который также преобразует бензол в фенол. Фактически, возможность рециркулировать хлористый водород сделала процесс Рашига-Хукера предпочтительнее процесса Доу и Байера, который требует превращения продукта хлорида натрия в хлор и гидроксид натрия. Однако реакция происходит при очень высоких температурах в очень кислой среде с парами хлористого водорода, и поэтому в промышленных условиях высокой коррозионной для реакции необходимо использовать оборудование с стойкостью. Хотя процесс Рашига-Хукера действительно перерабатывает производимый им хлористый водород, его катализатор подвергается отложению углерода и его необходимо часто регенерировать. Жесткая химическая среда, использование катализаторов и большое потребление энергии сделали его мишенью для зеленой химии . альтернатив [ 6 ]
Процесс Рашига-Хукера страдает от проблем с селективностью на обоих этапах. На первом этапе реакция проводится только до конверсии от 10 до 15%, чтобы предотвратить второе присоединение атома хлора к желаемому хлорбензолу. Несмотря на это, общая селективность реакции составляет от 70% до 85%. Это второе добавление можно отменить с помощью модификации Хукера, хотя это также дорого. Второй этап разделяет низкий коэффициент конверсии и высокую селективность первого этапа. Небольшое количество конверсии за реакцию нивелирует денежную выгоду от переработки хлористого водорода из-за больших первоначальных затрат на реакцию. Поэтому процесс Рашига-Хукера необходимо было проводить при высоких концентрациях в больших реакторах, чтобы он был промышленно экономичным. [ 6 ]
Из-за низкой производительности этот процесс сегодня практически не используется. По состоянию на 1997 год [update]В США все заводы, использовавшие процесс Рашига-Хукера, были остановлены, хотя он все еще использовался на некоторых заводах в таких странах, как Аргентина, Индия, Италия и Польша. Вместо использования процесса Рашига-Хукера некоторые компании используют процесс Хока или кумола , который вместо этого синтезирует ацетон и фенол из бензола и пропилена. Этот предпочтительный процесс доминировал на рынке, особенно потому, что ацетон также является весьма желанным веществом. [ 6 ]
Ссылки
[ редактировать ]- ^ Вебер, Манфред; Вебер, Маркус; Кляйне-Бойманн, Майкл (2004). "Фенол". Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a19_299.pub2 . ISBN 3527306730 .
- ^ Кропф, Х. (1964). «Современные технические синтезы фенолов I». Технология инженера-химика . 36 (7): 759–768. doi : 10.1002/cite.330360707 .
- ^ Доктор А.С. Некролог Фридриха Рашига (PDF) .
- ^ Лиднер, Г; Нюберг, К. (06 декабря 2012 г.). Экологическая инженерия: дисциплина химической инженерии . п. 37. ИСБН 9789401026086 .
- ^ Лош, П; Колб, Дж. Ф.; Астафан А; Дау, Ти Джей; Пинар, Л; Пэйл, П; Луи, Б. (2016). «Экологически совместимое непрерывное галогенирование ароматических соединений, катализируемое цеолитом». Зеленая химия . 18 (17): 4714–4724. дои : 10.1039/C6GC00731G .
- ^ Jump up to: а б с д и Вайссермель, Клаус; Арпе, Ханс-Юрген, ред. (27 мая 2003 г.), «Производные бензола» , Промышленная органическая химия , Вайнхайм, Германия: Wiley-VCH Verlag GmbH, стр. 351–352, doi : 10.1002/9783527619191.ch13 , ISBN 978-3-527-61919-1 , получено 20 декабря 2022 г.
- ^ Jump up to: а б Виткофф, Гарольд; Рубен, Брайан; Плоткин, Джеффри (10 декабря 2012 г.). Промышленные органические химикаты . п. 327. ИСБН 9781280556692 .
- ^ Тайман, JHP (21 августа 1996 г.). Синтетические и природные фенолы . п. 7. ISBN 9780080542195 .