натрия Трет -бутоксид
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК натрия Трет -бутоксид | |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.011.584 |
ПабХим CID | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 4 Н 9 Или О | |
| Молярная масса | 96.105 g·mol −1 |
| Плотность | 1,025 г/см 3 |
| Кислотность ( pKa ) | 19 [1] |
| Опасности | |
| точка возгорания | 14 ° C (57 ° F; 287 К) |
| Паспорт безопасности (SDS) | [1] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
натрия Трет -бутоксид (или натрия трет- бутоксид ) представляет собой химическое соединение с формулой (CH 3 ) 3 CONa (сокр. NaOtBu ). [2] Это сильное ненуклеофильное основание . Он горюч и чувствителен к влаге. В химической литературе его иногда называют трет- бутоксидом натрия. По реакционной способности он подобен более распространенному калия трет -бутоксиду .
Соединение можно получить обработкой трет -бутилового спирта гидридом натрия . [3]
Реакции
[ редактировать ]Одним из применений трет -бутоксида натрия является использование в качестве ненуклеофильного основания. Он широко использовался при аминировании Бухвальда-Хартвига , как в этом типичном примере: [4]
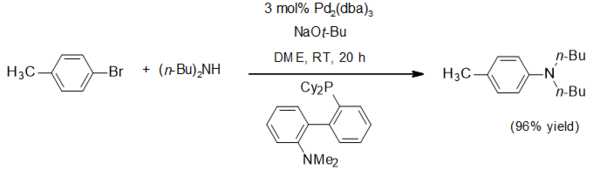
Трет-бутоксид натрия используется для получения комплексов трет-бутоксида. Например, гекса(трет-бутокси)дивольфрам(III) получают реакцией метатезиса соли из гептахлорида дивольфрама: [5]
- NaW 2 Cl 7 (THF) 5 + 6 NaOBu-t → W 2 (OBu-t) 6 + 7 NaCl + 5 THF
Структура
[ редактировать ]-бутоксид натрия Трет образует кластеры в твердом состоянии, оба гексамера. [6] и нонамеры. [7]
 |  |
| гексамер | нонамер |
Родственные соединения
[ редактировать ]- Трет-бутоксид калия
- Трет-бутоксид лития
- Трет-амилоксид натрия ( NaOC(CH 3 ) 2 C 2 H 5 ), хорошо растворимый аналог трет-бутоксида натрия. [8]
Ссылки
[ редактировать ]- ^ Дьюик, Пол М. (20 марта 2013 г.). Основы органической химии: для студентов фармации, медицинской химии и биологической химии . Джон Уайли и сыновья. ISBN 978-1-118-68196-1 .
- ^ http://www.sigmaaldrich.com/catalog/ProductDetail.do?lang=en&N4=359270%7CALDRICH&N5=SEARCH_CONCAT_PNO%7CBRAND_KEY&F=SPEC [ постоянная мертвая ссылка ]
- ^ ПМ. Дьюик, 2013. Основы органической химии: для студентов-фармацевтов, медицинской химии и биологической химии. Джон Уайли и сыновья; п. 157. ISBN 978-1-118-68196-1
- ^ Ян, Брайант Х.; Бухвальд, Стивен Л. (1999). «Катализируемое палладием аминирование арилгалогенидов и сульфонатов». Журнал металлоорганической химии . 576 (1–2): 125–146. дои : 10.1016/S0022-328X(98)01054-7 .
- ^ Бродерик, Эрин М.; Браун, Сэмюэл К.; Джонсон, Марк Дж.А. (2014). «Димолибден и дивольфрам гекса (алкоксиды)». Неорганические синтезы: Том 36 . Том. 36. С. 95–102. дои : 10.1002/9781118744994.ch18 . ISBN 978-1-118-74499-4 .
- ^ Э. Остренг; Х.Х. Сёнстеби; С. Ойен; О. Нильсен; Х. Фьельвог (2014). «Атомно-слоевое осаждение оксидов натрия и калия: оценка прекурсоров и осаждение тонких пленок» . Далтон Транс. 43 (44): 16666–16672. дои : 10.1039/C4DT01930J . hdl : 10852/55422 . ПМИД 25265332 .
- ^ Х. Некола; Ф. Ольбрих; У. Беренс (2002). бутоксида лития и натрия «Кристаллическая и молекулярная структура трет- ». З. Анорг. General Chem. 628 (9–10): 2067–2070. doi : 10.1002/1521-3749(200209)628:9/10<2067::AID-ZAAC2067>3.0.CO;2-N .
- ^ Беннетт, Чад Э. (2008). «Натрий -трет -Амилоксид». Энциклопедия реагентов для органического синтеза . дои : 10.1002/047084289X.rn01008 . ISBN 978-0-471-93623-7 .