Биосовместимость титана

Титан впервые был использован в хирургии в 1950-х годах после того, как десять лет назад он использовался в стоматологии. [ 1 ] В настоящее время это предпочтительный металл для протезирования, внутренней фиксации, внутренних устройств и инструментов. Титан используется с головы до ног в биомедицинских имплантатах. Титан можно найти в нейрохирургии, слуховых аппаратах с костной проводимостью, имплантатах ложного глаза, для спондилодеза клетках , кардиостимуляторах , имплантатах пальцев ног, а также в заменах плечевого/локтевого/бедренного/коленного сустава, а также во многих других областях. Основная причина, по которой титан часто используется в организме, связана с его биосовместимостью и, с модификациями поверхности, биоактивной поверхностью. К характеристикам поверхности, влияющим на биосовместимость, относятся текстура поверхности , стерические препятствия , места связывания и гидрофобность (смачивание). Эти характеристики оптимизированы для создания идеального клеточного ответа. Некоторые медицинские имплантаты, а также детали хирургических инструментов покрыты нитридом титана (TiN).
Биосовместимость
[ редактировать ]Титан считается наиболее биосовместимым металлом из-за его устойчивости к коррозии со стороны телесных жидкостей, биоинертности, способности к остеоинтеграции и высокого предела усталости. Способность титана противостоять суровым физическим условиям является результатом защитной оксидной пленки, которая естественным образом образуется в присутствии кислорода. Оксидная пленка прочно приклеена, нерастворима и химически непроницаема, предотвращая реакции между металлом и окружающей средой. [ нужна ссылка ]
Взаимодействие и пролиферация остеоинтеграции
[ редактировать ]Поверхности с высокой энергией вызывают ангиогенез во время остеоинтеграции.
[ редактировать ]Было высказано предположение, что способность титана к остеоинтеграции обусловлена высокой диэлектрической постоянной его поверхностного оксида, который не денатурирует белки (например, тантала и кобальта сплавы ). [ 2 ] Его способность физически связываться с костью дает титану преимущество перед другими материалами, для сохранения прикрепления которых требуется использование клея. Титановые имплантаты служат дольше, и для разрыва связей, соединяющих их с телом, требуются гораздо более высокие силы по сравнению с их альтернативами. [ 3 ]
Свойства поверхности определяют остеоинтеграцию
[ редактировать ]Поверхностные свойства биоматериала играют важную роль в определении клеточной реакции (адгезии и пролиферации клеток) на материал. Микроструктура титана и высокая поверхностная энергия позволяют ему вызывать ангиогенез, который способствует процессу остеоинтеграции. [ 4 ]
Поверхностная энергия
[ редактировать ]Редокс-потенциал
[ редактировать ]Титан может иметь множество различных стандартных электродных потенциалов в зависимости от степени его окисления. Твердый титан имеет стандартный электродный потенциал -1,63 В. Материалы с более высоким стандартным электродным потенциалом легче восстанавливаются, что делает их лучшими окислителями. [ 5 ] Как видно из таблицы ниже, твердый титан предпочитает подвергаться окислению, что делает его лучшим восстановителем.
| Половина реакции | Стандартный электродный потенциал (В) |
|---|---|
| Из 2+ + 2 и − → Вы(а) | -1.63 [ 5 ] |
| Из 3+ + 3 и − → Вы(а) | -1.21 [ 6 ] |
| ТиО 2 + + 2 ч. + + 4 и − → Ti(s) + H 2 O | -0.86 [ 7 ] |
| 2 TiO 2 (т) + 2 H + + 2 и − → Ti 2 O 3 (т) + H 2 O | -0.56 [ 7 ] |
| Из 2+ (водн.)/М 3+ (вода) | -0.36 [ 6 ] |
Покрытие поверхности
[ редактировать ]
Титан естественным образом пассивируется , образуя оксидную пленку, которая становится неоднородной и поляризованной в зависимости от времени воздействия окружающей среды. [ 8 ] Это приводит к увеличению адсорбции гидроксильных групп, липопротеинов и гликолипидов с течением времени. [ 8 ] Адсорбция этих соединений меняет способ взаимодействия материала с организмом и может улучшить биосовместимость. В титановых сплавах, таких как Ti-Zr и Ti-Nb, ионы циркония и ниобия, высвобождаемые в результате коррозии, не попадают в тело пациента, а добавляются в пассивирующий слой. [ 9 ] Легирующие элементы в пассивном слое добавляют степень биосовместимости и коррозионной стойкости в зависимости от исходного состава сплава основного металла до коррозии.
Поверхностная концентрация белка, ( ), определяется уравнением
где Q ADS — поверхностная плотность заряда в См⋅см. −2 , M – молярная масса белка в г⋅моль −1 , n — количество переданных электронов (в данном случае по одному электрону на каждую протонированную аминогруппу в белке), а F — константа Фарадея в К⋅моль. −1 .
Уравнение для частоты столкновений выглядит следующим образом:
где Д = 8,83 × 10 −7 см 2 ⋅s −1 — коэффициент диффузии молекулы БСА при 310 К, d = 7,2 нм — «диаметр» белка, эквивалентный удвоенному радиусу Стокса, N A = 6,023 × 10 23 моль −1 — постоянная Авогадро, а c * = 0,23 г⋅л. −1 (3,3 мкМ) — критическая объемная концентрация пересыщения.
Смачивание и твердая поверхность
[ редактировать ]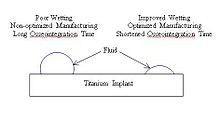
Смачивание происходит в зависимости от двух параметров: шероховатости поверхности и доли поверхности. [ 11 ] Увеличивая смачивание, имплантаты могут сократить время, необходимое для остеоинтеграции, позволяя клеткам более легко связываться с поверхностью имплантата. [ 3 ] Смачивание титана можно изменить путем оптимизации параметров процесса, таких как температура, время и давление (показано в таблице ниже). Титан со стабильными оксидными слоями, состоящими преимущественно из TiO 2 , приводит к улучшению смачивания имплантата при контакте с физиологической жидкостью. [ 12 ]
| Поверхность | Угол смачивания (градусы) | Давление (мбар) во время обработки | Температура (градусы С) во время обработки | Другая обработка поверхности |
|---|---|---|---|---|
| Только десять | ~50 [ 10 ] | - | - | Никто |
| TiO 2 TiO Ti 4 O 7 TiO 4 (Планарный) | ~33 [ 12 ] | 2.2 | 700 | Окисление |
| TiO 2 TiO Ti 4 O 7 (Планарный) | ~45 [ 12 ] | 4 | 700 | Окисление |
| TiO 2 TiO Ti 4 O 7 TiO 4 (полый) | ~32 [ 12 ] | 2.2 | 400 | Окисление |
| TiO 2 TiO Ti 4 O 7 (полый) | ~25 [ 12 ] | 2.6 | 500 | Окисление |
| TiO 2 TiO Ti 4 O 7 (полый) | ~8 [ 12 ] | 4 | 400 | Окисление |
| TiO 2 TiO Ti 4 O 7 (полый) | ~20 [ 12 ] | 4 | 500 | Окисление |
| Ти с шероховатой поверхностью | 79.5 ± 4.6 [ 13 ] | - | - | Обработанная поверхность |
| Ti с обработанной щелочью поверхностью | 27.2 ± 6.9 [ 13 ] | - | - | Био-поверхность |
Адсорбция
[ редактировать ]Коррозия
[ редактировать ]Механическое истирание пленки оксида титана приводит к увеличению скорости коррозии . [ 14 ]
Титан и его сплавы не защищены от коррозии в организме человека. Титановые сплавы чувствительны к абсорбции водорода, что может вызвать осаждение гидридов и вызвать охрупчивание, приводящее к разрушению материала. [ 14 ] «Водородное охрупчивание наблюдалось как механизм деградации in vivo в условиях фреттинг-щелевой коррозии, приводящий к образованию TiH, поверхностной реакции и растрескиванию внутри конусов модульного корпуса Ti/Ti». [ 14 ] Изучение и тестирование поведения титана в организме позволяют нам избежать злоупотреблений, которые могут привести к фатальной поломке имплантата, таких как использование стоматологических продуктов с высокой концентрацией фтора или веществ, способных снизить pH среды вокруг имплантата. [ 15 ]
Адгезия
[ редактировать ]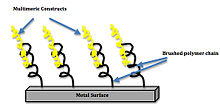
Клетки на границе имплантата очень чувствительны к инородным объектам. Когда имплантаты устанавливаются в организм, клетки инициируют воспалительную реакцию, которая может привести к инкапсуляции, нарушая функционирование имплантированного устройства. [ 16 ]
Идеальный ответ клеток на биоактивную поверхность характеризуется стабилизацией и интеграцией биоматериала, а также уменьшением количества потенциальных участков бактериальной инфекции на поверхности. Одним из примеров интеграции биоматериалов является титановый имплантат с инженерным биоинтерфейсом, покрытым биомиметическими мотивами. Было показано, что поверхности с этими биомиметическими мотивами усиливают связывание и передачу сигналов интегрина, а также дифференцировку стволовых клеток. Увеличение плотности кластеризации лигандов также увеличивало связывание интегрина. Покрытие, состоящее из тримеров и пентамеров, увеличило площадь контакта кости с имплантатом на 75% по сравнению с текущим клиническим стандартом титана без покрытия. [ 17 ] Такое увеличение площади позволяет повысить интеграцию клеток и снижает вероятность отторжения имплантированного устройства. Ленгмюра Изотерма :
, [ 10 ]
где c – концентрация адсорбата – максимальное количество адсорбированного белка, B ADS – сродство молекул адсорбата к местам адсорбции. Изотерму Ленгмюра можно линеаризовать, преобразовав уравнение в следующий вид:
Это моделирование является хорошим приближением адсорбции на поверхности по сравнению с экспериментальными значениями. [ 10 ] Изотерму Ленгмюра адсорбции элементов на поверхности титана можно определить, построив график известных параметров. Эксперимент по адсорбции фибриногена на поверхности титана «подтвердил применимость изотермы Ленгмюра для описания адсорбции фибриногена на поверхности титана». [ 10 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Фишер Дж. (декабрь 2000 г.). «Механический, термический и химический анализ бинарной системы Au-Ti при разработке стоматологического сплава». Дж. Биомед. Матер. Рез . 52 (4): 678–86. doi : 10.1002/1097-4636(20001215)52:4<678::AID-JBM12>3.0.CO;2-P . ПМИД 11033550 .
- ^ Блэк, Джонатан (январь 1994 г.). «Биологическая эффективность тантала». Клинические материалы . 16 (3): 167–173. дои : 10.1016/0267-6605(94)90113-9 .
- ^ Перейти обратно: а б Рейнс, Эндрю Л.; Оливарес-Наваррете, Рене; Виланд, Марко; Кокран, Дэвид Л.; Шварц, Цви; Боян, Барбара Д. (2010). «Регуляция ангиогенеза во время остеоинтеграции с помощью микроструктуры и энергии поверхности титана» . Биоматериалы . 31 (18): 4909–17. doi : 10.1016/j.bimaterials.2010.02.071 . ПМЦ 2896824 . ПМИД 20356623 .
- ^ «Титан» (PDF) .
- ^ Перейти обратно: а б «Стандартные потенциалы восстановления (25oC)» . Архивировано из оригинала 18 июня 2013 г. Проверено 23 октября 2012 г.
- ^ Перейти обратно: а б Браун, док. «Химия титана» .
- ^ Перейти обратно: а б Зима, Марк. «Соединения титана» .
- ^ Перейти обратно: а б Хили, Кевин Э.; Дюшейн, Пол (1991). «Физическая модель интерфейса титан-ткань» . Транзакции ASAIO . 37 (3): М150–1. ПМИД 1751087 .
- ^ Лонг, Марк; Стойка, HJ (1998). «Титановые сплавы при полной замене суставов - взгляд на материаловедение». Биоматериалы . 19 (18): 1621–39. дои : 10.1016/S0142-9612(97)00146-4 . ПМИД 9839998 .
- ^ Перейти обратно: а б с д и ж г Джексон, Дуглас Р.; Оманович, Саша; Роско, Шэрон Г. (2000). «Электрохимические исследования адсорбционного поведения сывороточных белков на титане». Ленгмюр . 16 (12): 5449–57. дои : 10.1021/la991497x .
- ^ Бико, Хосе; Тиле, Уве; Кере, Дэвид (2002). «Смачивание фактурных поверхностей». Коллоиды и поверхности А: Физико-химические и инженерные аспекты . 206 (1–3): 41–6. дои : 10.1016/S0927-7757(02)00061-4 .
- ^ Перейти обратно: а б с д и ж г Сильва, МАМ; Мартинелли, А.Е.; Алвес, К.; Насименто, РМ; Тавора, член парламента; Вилар, компакт-диск (2006). «Модификация поверхности титановых имплантатов методом плазменного окисления в разряде полого катода» . Технология поверхностей и покрытий . 200 (8): 2618–26. doi : 10.1016/j.surfcoat.2004.12.027 .
- ^ Перейти обратно: а б Стрнад, Якуб; Стрнад, Зденек; Шестак, Ярослав; Урбан, Карел; Повышил, Цтибор (2007). «Биоактивированная титановая поверхность, которую можно использовать для миметической костной имплантации в стоматологии. Часть III: Характеристики поверхности и формирование контакта кость-имплантат». Журнал физики и химии твердого тела . 68 (5–6): 841–5. Бибкод : 2007JPCS...68..841S . дои : 10.1016/j.jpcs.2007.02.040 .
- ^ Перейти обратно: а б с Родригес, Даниэли К.; Урбан, Роберт М.; Джейкобс, Джошуа Дж.; Гилберт, Джереми Л. (2009). « Сильная коррозия in vivo и водородное охрупчивание извлеченных имплантатов тазобедренного сустава из титанового сплава с модульным корпусом» . Журнал исследований биомедицинских материалов. Часть B: Прикладные биоматериалы . 88 (1): 206–19. дои : 10.1002/jbm.b.31171 . ПМЦ 2667129 . ПМИД 18683224 .
- ^ «Архивная копия» (PDF) . Архивировано из оригинала (PDF) 4 марта 2016 г. Проверено 1 июня 2015 г.
{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка ) - ^ Франц, Сандра; Раммельт, Стефан; Шарнвебер, Дитер; Саймон, Ян К. (2011). «Иммунный ответ на имплантаты – обзор последствий для создания иммуномодулирующих биоматериалов». Биоматериалы . 32 (28): 6692–709. doi : 10.1016/j.bimaterials.2011.05.078 . ПМИД 21715002 .
- ^ Петри, штат Калифорния; Рейнор, Дж. Э.; Дамбо, Д.В.; Ли, ТТ; Джагтап, С.; Темплман, КЛ; Коллард, DM; Гарсия, Эй Джей (2010). «Многовалентные интегрин-специфичные лиганды улучшают заживление тканей и интеграцию биоматериала» . Наука трансляционной медицины . 2 (45): 45ра60. doi : 10.1126/scitranslmed.3001002 . ПМК 3128787 . ПМИД 20720217 .




