лакмусовая бумажка
В этой статье есть несколько проблем. Пожалуйста, помогите улучшить его или обсудите эти проблемы на странице обсуждения . ( Узнайте, как и когда удалять эти шаблонные сообщения )
|


Лакмус — водорастворимая смесь различных красителей, добываемая из лишайников . Он часто впитывается фильтровальной бумагой для получения одной из старейших форм индикатора pH , используемого для проверки материалов на кислотность . В кислой среде синяя лакмусовая бумага становится красной, а в основной или щелочной среде красная лакмусовая бумага становится синей. Короче говоря, это краситель и индикатор, который используется для размещения веществ по шкале pH.
История [ править ]
Слово «лакмус» происходит от древнескандинавского слова, означающего «мох, используемый для окрашивания». [1] Около 1300 года испанский врач Арнальд де Вилья Нова начал использовать лакмус для изучения кислот и оснований. [2] [3]
Начиная с 16 века, синий краситель добывали из некоторых лишайников , особенно в Нидерландах .
Природные источники [ править ]

Лакмус можно найти в разных видах лишайников . Красители извлекаются из таких видов, как Roccellatinctoria (Южная Америка), Roccella fuciformis (Ангола и Мадагаскар), Roccella pygmaea (Алжир), Roccella phycopsis , Lecanora tartarea (Норвегия, Швеция), Variolaria Dealbata , Ochrolechia parella , Parmotrematinctorum и Пармелия . В настоящее время основными источниками являются Roccella montagnei (Мозамбик) и Dendrographa leucophoea (Калифорния). [2]
Использует [ править ]
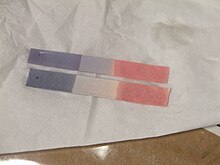
Основное использование лакмусовой бумаги - проверить, является ли раствор кислым или основным , поскольку синяя лакмусовая бумага становится красной в кислых условиях, а красная лакмусовая бумага становится синей в основных или щелочных условиях, при этом изменение цвета происходит в диапазоне pH 4,5–8,3. при 25 ° C (77 ° F). Нейтральная лакмусовая бумага имеет фиолетовый цвет. [2] Влажную лакмусовую бумагу также можно использовать для проверки на наличие водорастворимых газов, влияющих на кислотность или основность ; газ растворяется в воде , и полученный раствор окрашивает лакмусовую бумажку. Например, газообразный аммиак , который является щелочным, окрашивает красную лакмусовую бумажку в синий цвет. Хотя вся лакмусовая бумажка действует как pH-бумага, обратное неверно.
Лакмус также можно приготовить в виде водного раствора , который действует аналогичным образом. В кислой среде раствор имеет красный цвет, а в щелочной – синий.
| Лакмус ( показатель pH ) | ||
| ниже pH 4,5 | выше pH 5 .3 | |
| 4.5 | ⇌ | 5 .3 |
Химические реакции, отличные от кислотно-основных, также могут вызвать изменение цвета лакмусовой бумаги. Например, газообразный хлор превращает синюю лакмусовую бумажку в белую; лакмусовая краска обесцвечивается [4] потому что гипохлорита присутствуют ионы . Эта реакция необратима, поэтому лакмусовая бумажка в данной ситуации не выступает индикатором.
Химия [ править ]
Лакмусовая смесь имеет номер CAS 1393-92-6 и содержит от 10 до 15 различных красителей. Все химические компоненты лакмуса, вероятно, будут такими же, как и в родственной смеси, известной как орсеин, но в других пропорциях. В отличие от орсеина, основной компонент лакмуса имеет среднюю молекулярную массу 3300. [5] Кислотно-основные индикаторы на лакмусе своими свойствами обязаны хромофору -гидроксифеноксазона 7 . [6] Некоторым фракциям лакмуса были присвоены конкретные названия, включая эритролитмин (или эритролеин), азолитмин, спаниолитмин, лейкоорцеин и лейказолитмин. Азолитмин проявляет почти тот же эффект, что и лакмус. [7]
Рецепт приготовления лакмусовой бумажки из лишайников, представленный на веб-сайте Калифорнийского университета в Санта-Барбаре, гласит: [8]
Подробности найти сложно, поскольку процессы держались в секрете.
Это краткое изложение современной производственной процедуры взято из книги «Исчезающие лишайники», DHS Richardson, Лондон, 1975.Лишайники (предпочтительно Lecanora tartarea и Roccella красящая ) измельчают в растворе карбоната натрия и аммиака .
Время от времени перемешивайте лишайники, и примерно через четыре недели цвет изменится с красного на фиолетовый и, наконец, на синий. Затем лишайники сушат и измельчают в порошок. На этой стадии лишайники содержат частично лакмусовые и частично орцеиновые пигменты . Орсеин удаляют экстракцией спиртом , оставляя чистый синий лакмус. Он продается в виде синих комков, масс или таблеток после смешивания с бесцветными соединениями, такими как мел и гипс . Лакмусовая бумага – это бумага, пропитанная этим веществом.
Механизм [ править ]
Красный лакмус содержит слабую дипротоновую кислоту . Когда он подвергается воздействию основного соединения, ионы водорода реагируют с добавленным основанием. Сопряженное основание, образующееся из лакмусовой кислоты, имеет синий цвет, поэтому влажная красная лакмусовая бумага в щелочном растворе синеет.
Ссылки [ править ]
- ^ «Лакмус» . 7 октября 2021 г.
- ^ Jump up to: Перейти обратно: а б с Нойперт, Манфред (31 января 2013 г.). «Лакмус». Römpp Lexikon Chemie (на немецком языке).
- ^ Сурбер, Кристиан; Гумберт, Филипп; Абельс, Кристоф; Майбах, Ховард (2018). Сурбер, Кристиан; Абельс (ред.). pH кожи: проблемы и вызовы – современные проблемы дерматологии . Базель: Медицинское и научное издательство Karger. п. 3. ISBN 9783318063851 . Проверено 1 мая 2023 г.
В начале 14 века испанский ученый Арнальд де Вилья Нова (1235–1311) начал использовать лакмус для изучения кислот и оснований. Это соединение, извлеченное из лишайника, использовалось в качестве красителя, по крайней мере, со времен викингов, но он был первым человеком, который, как известно, использовал его в качестве теста на кислотность.
- ^ О'Лири, Донал (2000). «Хлор» . Химические элементы . Архивировано из оригинала 21 декабря 2008 г.
- ^ Беккен, Х.; ЭМ. Готшальк; У.в. Гижицкий; Х. Кремер; Д. Маассен; Х.-Г. Мэтью; Х. Муссо; К. Ратьен; ул. Здгорский (2003). «Орсеин и лакмус». Биотехника и гистохимия . 78 (6): 289–302. дои : 10.1080/10520290410001671362 . ПМИД 15473576 . S2CID 41944320 .
- ^ Х. Муссо, К. Ратьен (1959). «Орцеиновые красители. X. Светопоглощение и хромофор лакмуса». хим. Бер . 92 (3): 751–753. дои : 10.1002/cber.19590920331 .
- ^ ET Wolf: Полный обзор элементарных аналитических исследований органических веществ, стр. 450–453, опубликовано в 1846 году , Верлаг Э. Антон (Германия).
- ^ «Студенты задают вопросы, ученые UCSB на них отвечают» . UCSB ScienceLine . 2002.