дентатность

монодентатные лиганды
В координационной химии дентальность ( от латинского dentis «зуб») относится к числу донорных групп в данном лиганде , которые связываются с центральным атомом металла в координационном комплексе . [ 1 ] [ 2 ] Во многих случаях только один атом лиганда связывается с металлом, поэтому дентатность равна единице, и лиганд называют монодентатным (иногда его называют недентатным ). Лиганды, имеющие более одного связанного атома, называются полидентатными или мультидентатными . Дентальность лиганда обозначается греческой буквой κ («каппа»). [ 3 ] Например, κ 6 - ЭДТА описывает лиганд ЭДТА, который координирует свои действия через 6 несмежных атомов.
Дентичность отличается от тактильности , поскольку тактильность относится исключительно к лигандам, у которых координирующие атомы расположены рядом. В этих случаях η («эта»). используется обозначение [ 4 ] Мостиковые лиганды используют обозначение μ («мю»). [ 5 ] [ 6 ]
Классы
[ редактировать ]Полидентатные лиганды являются хелатирующими агентами. [ 7 ] и классифицируются по их идентичности. Некоторые атомы не могут образовать максимально возможное количество связей, которые может образовать лиганд. В этом случае один или несколько сайтов связывания лиганда не используются. Такие сайты могут быть использованы для образования связи с другими химическими соединениями .
- Бидентатные (также называемые дидентатными) лиганды связываются двумя атомами, примером является этилендиамин .
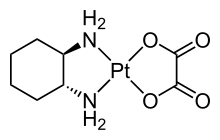
Структура фармацевтического препарата Оксалиплатин , который содержит два разных бидентатных лиганда.
- Тридентатные лиганды связываются тремя атомами, примером является терпиридин . Тридентатные лиганды обычно связываются посредством двух типов связей, называемых «mer» и «fac». «fac» означает «грань», атомы донора расположены треугольником вокруг одной грани октаэдра. «Мер» означает меридиан, где атомы-доноры вытянуты вокруг половины октаэдра. Циклические тридентатные лиганды, такие как TACN и 9-ан-S3, связываются лицевым образом.
- Тетрадентатные лиганды связываются с четырьмя донорными атомами, примером является триэтилентетрамин (сокращенно триен). Для различной геометрии центрального металла может быть разное количество изомеров в зависимости от топологии лиганда и геометрии металлического центра. Для октаэдрических металлов линейный тетрадентатный триен может связываться посредством трех геометрических форм. Триподальные тетрадентатные лиганды, например трис(2-аминоэтил)амин , более скованы и на октаэдрах оставляют два цис-сайта (рядом друг с другом). Многие встречающиеся в природе макроциклические лиганды являются тетрадентативными, примером является порфирин в геме . В октаэдрическом металле они оставляют два свободных места друг напротив друга.
- Пентадентатные лиганды связываются пятью атомами, примером является этилендиаминотриуксусная кислота.
- Шестидентатные лиганды связываются шестью атомами, примером является ЭДТА (хотя она может связываться и тетрадентатно).
- Лиганды с дентностью более 6 хорошо известны. Лиганды 1,4,7,10-тетраазациклододекан-1,4,7,10-тетраацетат (ДОТА) и пентаацетат диэтилентриамина (ДТПА) являются октадентатными. Они особенно полезны для связывания ионов лантаноидов, которые обычно имеют координационные числа больше 6.

Константы устойчивости
[ редактировать ]В целом стабильность металлокомплекса коррелирует с дентальностью лигандов, что можно объяснить хелатным эффектом . Полидентатные лиганды, такие как гекса- или октадентатные лиганды, имеют тенденцию связывать ионы металлов сильнее, чем лиганды с более низкой дентатностью, в первую очередь из-за энтропийных факторов. Константы стабильности являются количественной мерой оценки термодинамической стабильности координационных комплексов.
См. также
[ редактировать ]Внешние ссылки
[ редактировать ]- Конспекты лекций по хелатированию ЭДТА. PDF, 2,4 МБ – Слайд 3 о дентальности
Ссылки
[ редактировать ]- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « Дентность ». два : 10.1351/goldbook.D01594
- ^ фон Зелевский, А. «Стереохимия координационных соединений» Джон Вили: Чичестер, 1995. ISBN 047195599X .
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « κ (каппа) в неорганической номенклатуре ». дои : 10.1351/goldbook.K03366
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « η (эта или гапто) в неорганической номенклатуре ». дои : 10.1351/goldbook.H01881
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « Мостиковый лиганд ». два : 10.1351/goldbook.B00741
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « µ-(мю) в неорганической номенклатуре ». два : 10.1351/goldbook.M03659
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « Хелирование ». два : 10.1351/goldbook.C01012
