Терпиридин

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
1 2 ,2 2 :2 6 ,3 2 -Терпиридин | |
| Другие имена
2,6-Бис(2-пиридил)пиридин, Трипиридил, 2,2 ' :6 ' ,2″-Терпиридин
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.013.235 |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 15 Ч 11 Н 3 | |
| Молярная масса | 233.274 g·mol −1 |
| Появление | белое твердое вещество |
| Температура плавления | 88 ° C (190 ° F; 361 К) |
| Точка кипения | 370 ° С (698 ° F; 643 К) [1] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Терпиридин (2,2';6',2"-терпиридин, часто сокращенно Terpy или Tpy ) представляет собой гетероциклическое соединение , полученное из пиридина . Это белое твердое вещество, растворимое в большинстве органических растворителей. Соединение в основном используется в качестве Лиганд в координационной химии .
Синтез
[ редактировать ]Терпиридин был впервые синтезирован Г. Морганом и Ф. Х. Берстоллом в 1932 г. путем окислительного сочетания пиридинов. Однако этот метод давал низкие выходы. С тех пор были описаны более эффективные синтезы, в основном начиная с 2-ацетилпиридина . [2] Один метод дает енаминон реакцией 2-ацетилпиридина с ,N-диметилформамида N диметилацеталем . [3] Катализируемая основанием реакция 2-ацетилпиридина с сероуглеродом с последующим алкилированием метилиодидом дает C 5 H 4 NCOCH=C(SMe) 2 . Конденсация этого вида с 2-ацетилпиридином образует родственный 1,5-дикетон, который конденсируется с ацетатом аммония с образованием терпиридина. Обработка этого производного никелем Ренея удаляет тиоэфирную группу. [4]
Разработаны другие методы синтеза терпиридина и его замещенных производных. [5] Замещенные терпиридины также синтезируются в результате реакций кросс-сочетания, катализируемых палладием . Его можно получить из бис-триазинилпиридина .
Характеристики
[ редактировать ]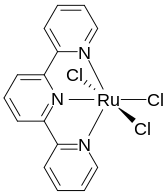
Терпиридин представляет собой тридентатный лиганд , который связывает металлы в трех меридиональных участках, образуя два соседних 5-членных хелатных кольца MN 2 C 2 . [6] Терпиридин образует комплексы с большинством переходных металлов ионов , как и другие полипиридиновые соединения , такие как 2,2'-бипиридин и 1,10-фенантролин . Комплексы, содержащие два терпиридиновых комплекса, т.е. [M(Terpy) 2 ] п+ являются общими. Они структурно отличаются от родственных [M(Bipy) 3 ] п+ комплексы ахиральны.
металл-лиганд Терпиридиновые комплексы, как и другие полипиридиновые комплексы, проявляют характерные оптические и электрохимические свойства: перенос заряда (MLCT) в видимой области, обратимое восстановление и окисление , достаточно интенсивную люминесценцию .
являются пи-акцепторами, они Поскольку терпиридин и бипиридин имеют тенденцию стабилизировать металлы в более низких степенях окисления. Например, в растворе ацетонитрила можно получить [M(Terpy) 2 ] + (М = Ni, Со).
Родственные соединения
[ редактировать ]- бис-триазинилпиридины родственны терпиридину по связыванию с металлами.
- кватерпиридин
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Лиде, Д.Р. (1998), Справочник по химии и физике (87-е изд.), Бока-Ратон, Флорида: CRC Press, стр. 3–510, ISBN 0-8493-0594-2
- ^ Хофмайер, Х.; Шуберт, США (2004). «Последние достижения в супрамолекулярной химии терпиридин-металлических комплексов». хим. Соц. Преподобный . 33 (6): 373–99. дои : 10.1039/B400653B . ПМИД 15280970 .
- ^ Джеймсон, Дональд Л.; Гиз, Лиза Э. (1998). «2,2’:6’,2″-Терпиридин». Неорганические синтезы . Том. 32. С. 46–50. дои : 10.1002/9780470132630.ch7 . ISBN 978-0-471-24921-4 .
- ^ Поттс, Коннектикут; Ралли, П.; Теодоридис, Г.; Уинслоу, П. (1990). «2,2':6',2' - Терпиридин» . Органические синтезы
{{cite journal}}: CS1 maint: multiple names: authors list (link); Сборник томов , т. 7, с. 476 . - ^ Камата К., Сузуки А., Накаи Ю., Наказава Х., «Каталитическое гидросилилирование алкенов комплексами железа, содержащими производные терпиридина в качестве вспомогательных лигандов», Organometallics 2012, 31, 3825. два : 10.1021/om300279t
- ^ Гаврилова А.Л.; Боснич, Б. (2004). «Принципы дизайна мононуклеирующих и бинуклеирующих лигандов». Химические обзоры . 104 (2): 349–383. дои : 10.1021/cr020604g . ПМИД 14871128 .