Фотофармакология
История
[ редактировать ]Фотофармакология — развивающаяся междисциплинарная область, объединяющая фотохимию и фармакологию . [1] Основанный на способности света изменять фармакокинетику и фармакодинамику биоактивных молекул, он направлен на регулирование активности лекарств in vivo с помощью света. [2] Модуляция на основе света достигается за счет включения в фармакофор молекулярных фотопереключателей, таких как азобензол и диарилэтены, или фотоклеток, таких как о-нитробензил, кумарин и соединения BODIPY. [3] Такая избирательная активация биомолекул помогает предотвратить или свести к минимуму нецелевую активность и системные побочные эффекты. Более того, свет, являющийся регуляторным элементом, дает дополнительные преимущества, такие как способность доставляться с высокой пространственно-временной точностью, токсичность от низкой до незначительной, а также возможность контролировать как качественно, так и количественно путем настройки его длины волны и интенсивности. [4]
Хотя фотофармакология является относительно новой областью, концепция использования света в терапевтических целях вошла в практику несколько десятилетий назад. Фотодинамическая терапия (ФДТ) — это хорошо зарекомендовавший себя клинически практикуемый протокол, в котором фотосенсибилизаторы используются для производства синглетного кислорода для разрушения больных или поврежденных клеток или тканей. [2] Оптогенетика — еще один метод, использующий свет для динамического управления биологическими функциями, особенно мозговыми и нервными. [4] Хотя этот подход оказался полезным в качестве инструмента исследования, его клиническая реализация ограничена необходимостью генетических манипуляций. По сути, эти два метода заложили основу фотофармакологии. Сегодня это быстро развивающаяся область с разнообразными применениями как в фундаментальных исследованиях, так и в клинической медицине, которая имеет потенциал для преодоления некоторых проблем, ограничивающих диапазон применения других методов световодной терапии. 
Рисунок 1. Схематическое изображение механизма (а) фотофармакологии (б) фотодинамической терапии и (в) оптогенетики.
Открытие природных фоторецепторов, таких как родопсины, в глазу вдохновило биомедицинское и фармакологическое исследовательское сообщество на разработку светочувствительных белков для терапевтического применения. [2] Разработка синтетических фотопереключаемых молекул — важнейшая веха в истории систем доставки света. Ученые продолжают свои усилия по изучению новых фотопереключателей и стратегий доставки с повышенной эффективностью для воздействия на различные биологические молекулы, такие как ионные каналы, нуклеиновые кислоты и рецепторы ферментов. Исследования в области фотофармакологии перешли от исследований in vitro к исследованиям in vivo за значительно короткий период времени, дав многообещающие результаты в обеих формах. В настоящее время проводятся клинические испытания для дальнейшей оценки безопасности и эффективности этих фотофармакологических методов лечения и подтверждения их потенциала как инновационного подхода к доставке лекарств.
Механизм действия
[ редактировать ]Молекулярные фотопереключатели используются в области фотофармакологии, где энергетикой молекулы можно обратимо управлять с помощью света для достижения пространственного и временного разрешения конкретного эффекта. Фотопереключатели могут функционировать, подвергаясь фотоизомеризации , посредством которой свет используется для конформационной адаптации молекулы к биологическому участку, или посредством воздействия окружающей среды, когда внешний фактор, такой как эффект растворителя или водородная связь, может избирательно разрешать или подавлять излучательное состояние внутри молекулы. Для визуализации фотофизических процессов полезно использовать диаграмму Яблонского . Это диаграмма, на которой электронные и колебательные уровни энергии внутри молекулы изображены в виде вертикальных уровней и показаны возможные пути релаксации из возбужденных состояний. Обычно основное состояние обозначается как S 0 и изображается внизу рисунка, а близлежащие колебательные возбуждения находятся чуть выше него. Поглощение переводит электрон в состояние S 1 на любом колебательном уровне энергии или в возбужденное состояние более высокого порядка, если поглощенная энергия имеет достаточную величину. Затем возбужденное состояние может подвергнуться внутреннему преобразованию, которое представляет собой электронную релаксацию в более низкое состояние с той же колебательной энергетикой или колебательной релаксацией внутри состояния. За этим может последовать межкомбинационный переход, при котором электрон претерпевает переворот спина или радиационный или безызлучательный распад обратно в основное состояние. [5]

Одним из примеров органического соединения, подвергающегося фотоизомеризации, является азобензол . Структура представляет собой два фенильных кольца, соединенных двойной связью N=N, и представляет собой простейшее арилазосоединение. Азобензол и его производные имеют две доступные полосы поглощения: состояние S 1 от перехода n-π*, которое можно возбудить с помощью синего света, и состояние S 2 от перехода π-π*, которое можно возбудить с помощью ультрафиолетового света. . [6] Азобензол и его производные имеют два изомера: транс и цис. Транс-изомер, имеющий фенильные кольца на противоположных сторонах двойной азосвязи, является термически предпочтительным изомером, поскольку в нем меньше стереоэлектронных искажений и больше делокализации. Однако возбуждение транс-изомера в состояние S 2 облегчает переход в цис-изомер. Поглощение S 1 связано с обратным превращением в транс-изомер. Таким образом, азобензол и его производные могут выступать в качестве обратимых накопителей энергии, поддерживая напряженную конфигурацию цис-изомера. Модификации заместителей азобензола позволяют настраивать энергетику этого поглощения, и если они сконструированы таким образом, что две полосы поглощения перекрываются, можно использовать одну длину волны света для переключения между ними. Существует ряд подобных фотопереключателей, которые изомеризуются между E- и Z-конфигурациями по азогруппе (например, азобензол и азопиразол) или этиленовому мостику (например, стильбен и гемитиоиндиго). [7]
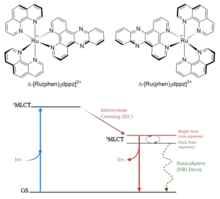
Альтернативно, фотопереключатели сами могут быть излучающими и обеспечивать контроль над своими свойствами со стороны окружающей среды. Одним из таких примеров является класс координационных комплексов полипиридила рутения. Обычно они содержат два бидентатных бипиридиновых или фенантролиновых лиганда и расширенный бидентатный лиганд фенантролин-феназин, такой как дипиридо[3,2-a:2,3-c]феназин (dppz). [8] Эти комплексы имеют доступное возбужденное состояние с переносом заряда металл-лиганд ( 1 MLCT), который подвергается быстрому межсистемному переходу в 3 Состояние MLCT обусловлено сильной спин-орбитальной связью рутениевого центра. Эти возбужденные состояния локализованы на расширенных лигандах феназинового азота, а эмиссия происходит из 3 Состояние МЛКТ. Взаимодействия водородных связей, такие как присутствие воды вокруг этих атомов азота, стабилизируют 3 Состояние MLCT, гасящее процесс эмиссии. Таким образом, контролируя наличие водного или иного протонного полярного растворителя, можно «включить/выключить» эмиссионное поведение и облегчить чередование «ярких состояний» и «темных состояний». Такое поведение переключателя света делает эти и подобные комплексы предметом недавнего интереса в фотофармакологических приложениях, таких как фотодинамическая терапия.
Молекулы
[ редактировать ]Как упоминалось ранее, фотофармакология основана на использовании молекулярных фотопереключателей, встроенных в структуру биологически активных молекул, что позволяет оптически контролировать их активность. [7] Они вводятся в структуру биологически активных соединений путем вставки, удлинения или биоизостерического замещения. [7] Эти включения могут быть подтверждены структурными соображениями молекулы или анализом SAR (отношения структура-активность) для определения оптимального положения. [7] Некоторыми примерами фотопереключаемых молекул, обычно используемых в фотофармакологии, являются азобензолы, диарилэтены и фотоклетки. [9]
Азобензолы
[ редактировать ]Азобензолы представляют собой класс фотопереключаемых молекул и используются в фотофармакологии для их обратимой фотоизомеризации, как описано в предыдущем разделе. Примером фотопереключаемой молекулы, в которой используется азобензол, является фототрексат. Фототрексат является ингибитором дигидрофолатредуктазы человека и является аналогом метотрексата , химиотерапевтического средства. [10] Было показано, что в фотоактивной цис-форме фототрексат является мощным антифолатом и относительно неактивен в транс-форме. [10] Азологизация или включение азобензола в метотрексат позволяет контролировать цитотоксическую активность и считается шагом вперед в разработке таргетных противораковых препаратов с локализованной эффективностью. [10]
Дневникилетены
[ редактировать ]Диарилэтеновые фотопереключатели имеют обратимые реакции циклизации и циклореверсии, которые являются фотоиндуцированными. [11] Это класс соединений, у которых ароматические функциональные группы связаны с каждым концом двойной углерод-углеродной связи. Примером этого класса молекул, который используется в фотофармакологии, является стильбен . Под воздействием света стильбен переключается между двумя своими изомерами (E и Z).
Рисунок 4. Рисунок, показывающий изомеризацию стильбена под действием света от E до Z.
Было показано, что диарилэтены имеют некоторые преимущества перед более изученными азобензольными переключателями, такие как термическая необратимость, высокая эффективность фотопереключения, благоприятная клеточная стабильность и низкая токсичность. [11] Было показано, что диарилэтены перспективны и в других областях, помимо фотофармакологии. Эти области включают оптическое хранение данных, оптоэлектронные устройства, супрамолекулярную самосборку и борьбу с подделками. [11]
Фотоклетки
[ редактировать ]Класс веществ, известный как фотоклетки, содержит «фоточувствительные группы, также известные как «фотоудаляемые защитные группы», из которых целевые вещества высвобождаются при воздействии света определенной длины волны». [12] Светочувствительные группы физически и химически защищают мишень от высвобождения до тех пор, пока молекула не подвергнется фотореакции. [12] Благодаря этим взаимодействиям со светом они часто используются в фотофармакологии. Совсем недавно они сыграли важную роль в фотоактивируемой химиотерапии (PACT). В PACT фотоклетки используют фотоудаляемую защитную группу, которая защищает цитотоксические препараты до тех пор, пока связь не будет расщеплена посредством взаимодействия света и цитотоксический препарат не высвободится. [13] Некоторые хорошо известные фотоклетки включают «производные о-нитробензила, производные кумарина, BODIPY, производные ксантена, производные хинона и диарилена». [12] Однако существуют ограничения на использование фотоклеток в клинических целях, поскольку не так много PPG, которые можно использовать in vivo. Это связано с тем, что конъюгаты ППГ-полезная нагрузка должны иметь приемлемую растворимость и биологическую инертность для биосовместимости, а также необходимость эффективного освобождения от клеток при длине волны выше 600 нм. [13] 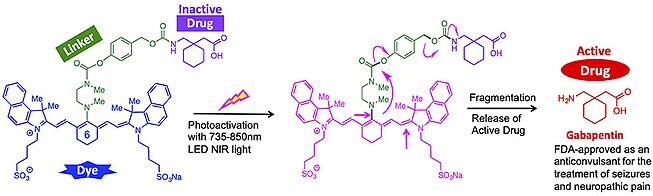
Рисунок 5. Пример системы освобождения фотоклеток, активируемой NIR. [14]
Приложение
[ редактировать ]Фотофармакология, использование света для контроля активности лекарств, стала многообещающим подходом к доставке и терапии лекарств. Используя силу света, исследователи могут добиться точного контроля над высвобождением и активацией лекарств, предлагая новые возможности для целенаправленного и персонализированного лечения. В этом подразделе мы исследуем применение фотофармакологии для доставки лекарств, уделяя особое внимание последним достижениям и потенциальным клиническим применениям.В этом исследовании [15] исследователи разработали ингибиторы HDAC, которые можно активировать или деактивировать светом, обеспечивая точный терапевтический контроль. Этот подход может уменьшить побочные эффекты традиционной химиотерапии за счет нацеливания ингибиторов на определенные участки тела, что потенциально приведет к более эффективному и персонализированному лечению рака.

В этом исследовании [16] исследователи разработали стратегию присоединения фотопереключаемой группы к обычному антибиотику; ципрофлоксацин. Присоединив фотопереключаемую группу, исследователи смогут контролировать активность ципрофлоксацина с помощью света. Этот подход потенциально может привести к новым способам лечения бактериальных инфекций с возможностью включения и выключения активности антибиотика по мере необходимости.В этой статье [17] Разработан протокол in vitro для тестирования различных длин волн света на линиях раковых клеток человека, в результате которого обнаружено, что синий свет наиболее эффективно ингибирует рост клеток. Это говорит о том, что фотофармакология может предложить новые варианты лечения рака, нацеливаясь на определенные длины волн света для модуляции активности лекарств в опухолевых клетках.Еще одно применение фотофармакологии [18] разрабатывает люминесцентный фотокорм, привитый на карбоксиметилхитозан, который при воздействии света выделяет окись углерода (CO), вызывая апоптотическую гибель клеток колоректального рака, демонстрируя точный контроль над высвобождением CO для таргетной терапии рака.Исследователи разработали набор фотопереключаемых антагонистов, которые могут взаимодействовать с GPCR — классом белков, участвующих в различных клеточных процессах. [19] Используя свет для переключения активности этих антагонистов, исследователи могут контролировать взаимодействие между антагонистами и GPCR в реальном времени. Этот подход позволяет точно модулировать активность GPCR, что может привести к новому пониманию клеточных сигнальных путей и потенциальных терапевтических применений.В другом приложении [20] используя свет для управления сборкой нанопор, исследователи потенциально могут регулировать поток ионов или молекул через эти нанопоры. Этот подход может найти применение в различных областях, включая зондирование, доставку лекарств и нанотехнологии.В этой статье [21] они использовали фотофармакологию для контроля активности лекарств; многофункциональные волокна в исследовании доставляют свет и лекарства к определенным участкам тела. Имплантированные волокна активируют светочувствительные лекарства, изменяя их структуру и обеспечивая точную доставку лекарств в условиях, требующих точного времени или дозировки.В другом исследовании [22] лиганды были разработаны таким образом, чтобы переключать режим связывания с ДНК G-квадруплекса под воздействием видимого света. Этот метод потенциально может модулировать активность G-квадруплексной ДНК, имеющей решающее значение для экспрессии генов и поддержания теломер, открывая новые терапевтические возможности, особенно в лечении рака. Исследование подчеркивает перспективность фотофармакологии в воздействии на определенные структуры ДНК, предполагая, что G-квадруплексная ДНК является жизнеспособной мишенью для будущих фотофармакологических вмешательств.Это исследование [23] разработали фотоактивируемые конъюгаты антитело-photoCORM, нацеленные на клетки рака яичников человека, выделяющие CO при воздействии света, чтобы уменьшить жизнеспособность клеток. Этот подход обеспечивает точное нацеливание на раковые клетки, сводя к минимуму вред для здоровых тканей, демонстрируя потенциал фотофармакологии в терапии рака.В этой статье [24] было разработано фотоактивируемое соединение, которое связывается и модулирует активность белка CRY1, регулирующего циркадные часы млекопитающих. Используя свет для контроля активности соединения, исследователи потенциально могут лечить нарушения циркадных ритмов и связанные с ними состояния здоровья, модулируя функцию CRY1. Фотофармакология предполагает использование света для контроля активности лекарств. В другом приложении [25] Исследователи используют фотофармакологию для контроля высвобождения лекарств и сосредотачивают внимание на лекарстве, взаимодействующем с тубулином, визуализируя его высвобождение в реальном времени с помощью серийной кристаллографии с временным разрешением. Этот метод дает представление о взаимодействии лекарств и тубулина и демонстрирует потенциал для разработки лекарств с точным действием.
Будущие направления
[ редактировать ]Будущее фотофармакологии имеет огромные перспективы. Он может совершить революцию в традиционной лекарственной терапии, открыв новые возможности для точной медицины, лечения неврологических расстройств, а также в области онкологии и офтальмологии . [1] Кроме того, это перспективно для области регенеративной медицины , где фотопереключатели можно использовать для модуляции активности сигнальных путей для целенаправленного восстановления и регенерации тканей. [3]
Фотофармакология будет продолжать расти и расширяться благодаря новым открытиям и достижениям в других смежных областях, таких как синтетическая химия, биология, нанотехнологии, фармакология и биоинженерия. Хотя потенциал фотофармакологии огромен, существуют некоторые проблемы, которые необходимо решить, чтобы сделать ее клинической реальностью. Одной из таких задач является разработка стабильных и биосовместимых фотопереключателей, которые избирательно действуют на свои целевые рецепторы без перекрестной активности. [2] Особенно важно, чтобы полосы поглощения этих фотопереключателей находились в диапазоне длин волн от 650 до 900 нм. [2] Следовательно, для достижения упомянутых выше характеристик и желаемого уровня производительности требуется оптимальная молекулярная конструкция фотопереключателей. В настоящее время фотофармакология использует рациональный подход к разработке лекарств, основанный на изучении взаимосвязи структура-активность, однако фенотипический скрининг фотопереключаемых препаратов также может быть полезным.
Для достижения хорошего пространственно-временного контроля над активностью лекарств должна существовать значительная разница между активностью изомеров. Однако понимание структурных изменений во время биологических эффектов, вызванных фотопереключением, ограничено. Этот дефицит знаний также является проблемой для развития этой области, поскольку он препятствует оптимизации активности и эффективности изомеров для получения ожидаемых результатов во время их применения. [3]
Еще одним препятствием и самой большой проблемой в фотофармакологии является поиск подходящих и эффективных способов доставки света в глубокие ткани тела и ткани, избегая таких проблем, как рассеяние и поглощение. В этом отношении были предприняты различные стратегии, одна из которых заключалась в разработке фотопереключаемых лигандов, которые реагируют на проникающие в глубокие ткани длины волн, такие как красный или инфракрасный свет. Более того, некоторые недавние доклинические исследования стимулировали разработку беспроводных, компактных или инъекционных и дистанционно управляемых устройств, способных доставлять свет к нервным тканям с минимальным повреждением. [26] Существуют новые оптофлюидные системы, которые могут одновременно регулировать как доставку лекарств, так и световую активность в определенных местах. Хотя внешняя доставка света является наиболее предпочтительным методом, использование внутренних экзогенных источников света, таких как люминесцентные соединения, позволяет доставлять свет непосредственно в место воздействия. Это позволит избежать проблем, связанных с проникновением света, а также повысить степень селективности. Кроме того, это создает возможность использовать фотофармакологию в качестве тераностического подхода, сочетающего таргетную доставку лекарств и молекулярную визуализацию. [2]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Хюлль, Катарина; Морштейн, Йоханнес; Траунер, Дирк (14 ноября 2018 г.). «Фотофармакология in vivo» . Химические обзоры . 118 (21): 10710–10747. doi : 10.1021/acs.chemrev.8b00037 . ISSN 0009-2665 . ПМИД 29985590 .
- ^ Перейти обратно: а б с д и ж Лерч, Майкл М.; Хансен, Микель Дж.; ван Дам, Гойцен М.; Шиманский, Виктор; Феринга, Бен Л. (05 сентября 2016 г.). «Новые цели в фотофармакологии» . Международное издание «Прикладная химия» . 55 (37): 10978–10999. дои : 10.1002/anie.201601931 . ISSN 1433-7851 . ПМИД 27376241 .
- ^ Перейти обратно: а б с Архипова Валентина; Фу, Хайген; Хоренс, Марк WH; Тринко, Джанлука; Ламейер, Люсьен Н.; Марин, Егор; Феринга, Бен Л.; Поеларендс, Геррит Дж.; Шиманский, Виктор; Слотбум, Дирк Дж.; Гуськов, Альберт (27 января 2021 г.). «Структурные аспекты фотофармакологии: понимание связывания фотопереключаемых и фотоклеточных ингибиторов с гомологом переносчика глутамата» . Журнал Американского химического общества . 143 (3): 1513–1520. дои : 10.1021/jacs.0c11336 . ISSN 0002-7863 . ПМЦ 7844824 . ПМИД 33449695 .
- ^ Перейти обратно: а б Велема, Виллем А.; Шиманский, Виктор; Феринга, Бен Л. (12 февраля 2014 г.). «Фотофармакология: за пределами доказательства принципа» . Журнал Американского химического общества . 136 (6): 2178–2191. дои : 10.1021/ja413063e . ISSN 0002-7863 . ПМИД 24456115 .
- ^ Лакович, Джозеф Р. Принципы флуоресцентной спектроскопии, 3-е издание (2006 г.), стр. 5, Springer Science+Business Media, LLC. ISBN 978-0 387-31278-1.
- ^ Цяо, Чжи. и др. ал. Азобензол-изоксазолин как фотофармакологический лиганд для оптического контроля рецептора ГАМК насекомых и его поведения. Управление по борьбе с вредителями. наук. 78, 467–474 (2022).
- ^ Перейти обратно: а б с д Кобаури, Пьермикеле; Деккер, Фрэнк Дж.; Шиманский, Виктор; Феринга, Бен Л. (2023). «Рациональный дизайн в фотофармакологии с молекулярными фотопереключателями». Angewandte Chemie, международное издание . 62 (30): e202300681. дои : 10.1002/anie.202300681 . ПМИД 37026576 .
- ^ Эндрю В., Линкольн, Пер., Туит, Эймер М. Влияние окружающей среды на фотофизику комплексов переходных металлов с дипиридо[2,3-a:3,2-c]феназином (dppz) и родственными лигандами. Обзоры координационной химии 255, 2676–2692 (2011).
- ^ Архипова Валентина; Фу, Хайген; Хоренс, Марк WH; Тринко, Джанлука; Ламейер, Люсьен Н.; Марин, Егор; Феринга, Бен Л.; Поеларендс, Геррит Дж.; Шиманский, Виктор; Слотбум, Дирк Дж.; Гуськов, Альберт (2021). «Структурные аспекты фотофармакологии: понимание связывания фотопереключаемых и фотоклеточных ингибиторов с гомологом переносчика глутамата». Журнал Американского химического общества . 143 (3): 1513–1520. дои : 10.1021/jacs.0c11336 . ПМИД 33449695 .
- ^ Перейти обратно: а б с Матера, Карло; Гомила, Александр MJ; Камареро, Нурия; Либерголи, Микела; Солер, Консепсьо; Горостиза, Пау (2018). «Фотопереключаемый антиметаболит для таргетной фотоактивируемой химиотерапии». Журнал Американского химического общества . 140 (46): 15764–15773. дои : 10.1021/jacs.8b08249 . hdl : 2445/126377 . ПМИД 30346152 .
- ^ Перейти обратно: а б с Ли, Цзыюн; Цзэн, Сяоянь; Гао, Каймин; Сун, Цзиньчжао; Он, Фан; Он, Тиан; Го, Хуэй; Инь, Джун (2023). «Фотопереключаемые диарилэтены: от молекулярных структур к биологическим применениям». Обзоры координационной химии . 497 . дои : 10.1016/j.ccr.2023.215451 .
- ^ Перейти обратно: а б с Ван, Шэн ) ; Сяоцян . 2023 Маолинь Яцзин , Ли , ( ;
- ^ Перейти обратно: а б Холост, Александра; Немет, Кристина; Мольнар, Тибор А.; Каллай, Михай; Келе, Питер; Бойтар, Мартон (2023). «Покраснеть, не чувствуя смущения — фотоклетки на основе ксантения для фототерапии, активируемой красным светом» . Журнал Американского химического общества . 145 (7): 4026–4034. дои : 10.1021/jacs.2c11499 . ПМЦ 9951246 . ПМИД 36752773 .
- ^ Блэк, Кэролайн Э.; Чжоу, Юджин; Деанджело, Кейтлин М.; Асанте, Исаак; Луи, Стэн Г.; Петасис, Никос А.; Хумаюн, Марк С. (2020). «Цианиновые наноклетки, активируемые ближним инфракрасным светом, для целенаправленного лечения черепно-мозговой травмы» . Границы в химии . 8 : 769. Бибкод : 2020FrCh....8..769B . дои : 10.3389/fchem.2020.00769 . ПМЦ 7489144 . ПМИД 33062635 .
- ^ Шиманский, Виктор; Урайлиду, Мария Э.; Велема, Виллем А.; Деккер, Фрэнк Дж.; Феринга, Бен Л. (2015). «Ингибиторы светоконтролируемой гистондеацетилазы (HDAC): на пути к фотофармакологической химиотерапии» . Химия: Европейский журнал . 21 (46): 16517–16524. дои : 10.1002/chem.201502809 . ПМК 5221732 . ПМИД 26418117 .
- ^ Велема, Виллем А.; Хансен, Микель Дж.; Лерч, Майкл М.; Дриссен, Арнольд Дж.М.; Шиманский, Виктор; Феринга, Бен Л. (2015). «Конъюгаты ципрофлоксацина и фотопереключателя: простая стратегия фотофармакологии» (PDF) . Биоконъюгатная химия . 26 (12): 2592–2597. doi : 10.1021/acs.bioconjchem.5b00591 . ПМИД 26574623 .
- ^ Хопкинс, СЛ; Зиверт, Б.; Аскес, SHC; Вельдхейзен, П.; Цвир, Р.; Хегер, Михал; Бонне, Сильвестр (2016). «Протокол облучения клеток in vitro для тестирования фотофармацевтических препаратов и влияния синего, зеленого и красного света на линии раковых клеток человека» . Фотохимические и фотобиологические науки . 15 (5): 644–653. дои : 10.1039/c5pp00424a . ПМК 5044800 . ПМИД 27098927 .
- ^ Чакраборти, Индранил; Хименес, Хорхе; Масчарак, ПК (2017). «CO-индуцированная апоптозная гибель клеток колоректального рака под действием люминесцентного фотоCORM, привитого на биосовместимый карбоксиметилхитозан» . Химические коммуникации . 53 (40): 5519–5522. дои : 10.1039/c7cc02842c . ПМК 5728991 . ПМИД 28466932 .
- ^ Хауверт, Нильс Дж.; Насмешливо, Тамара А.М.; Да Коста Перейра, Даниэль; Куистра, Альберт Дж.; Вина, Лиза М.; Фрикер, Герда CM; Вервей, Элеонора ВЕ; Де Бур, Альбертус Х.; Смит, Мартин Дж.; ДеГрааф, Крис; Вишер, Генри Ф.; Де Эш, Иван Дж. П.; Вейтманс, Майкель; Леурс, Роб (2018). «Синтез и характеристика набора инструментов двунаправленных фотопереключаемых антагонистов для фотофармакологии GPCR в реальном времени» . Журнал Американского химического общества . 140 (12): 4232–4243. дои : 10.1021/jacs.7b11422 . ПМЦ 5879491 . ПМИД 29470065 .
- ^ Муттер, Натали Л.; Воларич, Яна; Шиманский, Виктор; Феринга, Бен Л.; Маглия, Джованни (2019). «Обратимая фотоуправляемая сборка нанопор» . Журнал Американского химического общества . 141 (36): 14356–14363. дои : 10.1021/jacs.9b06998 . ПМК 6743218 . ПМИД 31469268 .
- ^ Фрэнк, Джеймс А.; Антонини, Марк-Жозеф; Чан, По-Хан; Каналес, Андрес; Конрад, Дэвид Б.; Гарвуд, Инди К.; Раич, Габриэла; Келер, Флориан; Финк, Йоэль; Аникеева, Полина (2020). «Фотофармакология in vivo на основе многофункциональных волокон» . ACS Химическая нейронаука . 11 (22): 3802–3813. дои : 10.1021/acschemneuro.0c00577 . ПМЦ 10251749 . ПМИД 33108719 .
- ^ о'Хаган, Майкл П.; Рамос-Сориано, Хавьер; Халдар, Сусанта; Шейх, Садия; Моралес, Хуан К.; Малхолланд, Адриан Дж.; Галан, М. Кармен (2020). «Фотопереключение режима связывания лиганда в видимом свете предполагает, что ДНК G-квадруплекса является мишенью для фотофармакологии». Химические коммуникации . 56 (38): 5186–5189. дои : 10.1039/d0cc01581d . hdl : 1983/51860d75-af8d-4d5b-ae49-b7e8a1282d12 . ПМИД 32267261 .
- ^ Кавахара, Брайан; Гао, Люси; Кон, Уитакер; Уайтлегг, Джулиан П.; Сен, Суваджит; Янзен, Карла; Масчарак, Прадип К. (2020). «Снижение жизнеспособности клеток рака яичников человека из-за антигенспецифической доставки монооксида углерода с помощью семейства фотоактивируемых конъюгатов антитело-photoCORM» . Химическая наука . 11 (2): 467–473. дои : 10.1039/c9sc03166a . ПМК 7067254 . ПМИД 32190266 .
- ^ Коларски, Душан; Миллер, Саймон; Осима, Цуёси; Нагай, Ёсико; Аоки, Юго; Кобаури, Пьермикеле; Шривастава, Ашутош; Сугияма, Акико; Амайке, Казума; Сато, Аято; Тама, Флоренция; Шиманский, Виктор; Феринга, Бен Л.; Итами, Кенитиро; Хирота, Цуёси (2021). «Фотофармакологическое манипулирование CRY1 млекопитающих для регуляции циркадных часов» . Журнал Американского химического общества . 143 (4): 2078–2087. дои : 10.1021/jacs.0c12280 . ПМЦ 7863067 . PMID 33464888 .
- ^ Враник, Максимилиан; и др. (2023). «Наблюдение за высвобождением фотофармакологического препарата из тубулина с помощью серийной кристаллографии с разрешением во времени». Природные коммуникации . 14 : 903. Бибкод : 2023NatCo..14..903W . дои : 10.1038/s41467-023-36481-5 . hdl : 11585/966526 .
- ^ Бериззи, Алиса Э.; Гуде, Сирил (2020), «Стратегии и соображения фотофармакологии рецепторов, связанных с G-белком» , От структуры к клиническому развитию: аллостерическая модуляция рецепторов, связанных с G-белком , Достижения в фармакологии, том. 88, Elsevier, стр. 143–172, doi : 10.1016/bs.apha.2019.12.001 , ISBN. 978-0-12-820187-9 , PMID 32416866 , получено 15 апреля 2024 г.
