Реакция Перкина
| Реакция Перкина | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Назван в честь | Уильям Генри Перкин | ||||||||||
| Тип реакции | Реакция конденсации | ||||||||||
| Реакция | |||||||||||
| |||||||||||
| Идентификаторы | |||||||||||
| RSC Идентификатор онтологии | RXNO: 0000003 | ||||||||||
| | |||||||||||
Реакция Перкина — органическая реакция, разработанная английским химиком Уильямом Генри Перкином и используемая для получения коричной кислоты . или α-замещенную β-арилакриловую кислоту путем альдольной конденсации ароматического Он дает α,β-ненасыщенную ароматическую кислоту альдегида и ангидрида кислоты в присутствии щелочной соли кислоты. [ 1 ] [ 2 ] Щелочная соль действует как основной катализатор , вместо него можно использовать другие основания. [ 3 ]

Написано несколько обзоров. [ 4 ] [ 5 ] [ 6 ]
Механизм реакции
[ редактировать ]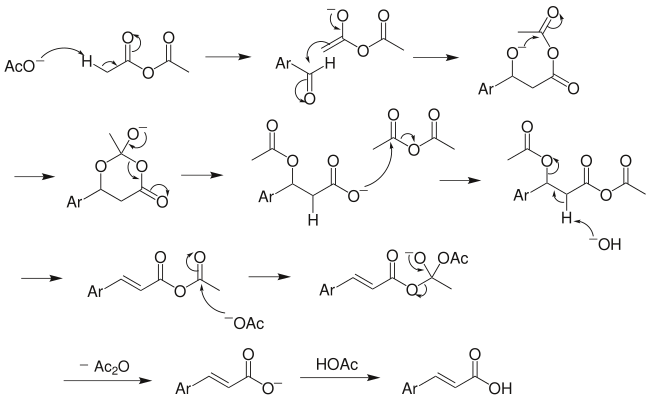
Из механизма реакции ясно, что для протекания реакции ангидрид алифатической кислоты должен содержать не менее 2 α-H. Вышеупомянутый механизм не является общепринятым, поскольку существует несколько других версий, включая декарбоксилирование без переноса уксусной группы. [ 7 ]
Приложения
[ редактировать ]- Салициловый альдегид превращают в кумарин с использованием уксусного ангидрида с ацетатом в качестве основания. [ 8 ]
- коричную кислоту получают из бензальдегида , опять же с использованием уксусного ангидрида в присутствии ацетата натрия или калия.
- ресвератрол (см. fo-ti ), фитоэстрогенный стильбен, является еще одним продуктом этой методологии. [ 9 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перкин, WH (1868 г.). «Об искусственном получении кумарина и образовании его гомологов» . Журнал Химического общества . 21 : 53–61. дои : 10.1039/js8682100053 .
- ^ Перкин, WH (1877 г.). «О некоторых углеводородах, полученных из гомологов коричной кислоты; а также об анетоле и его гомологах» . Журнал Химического общества . 32 : 660–674. дои : 10.1039/js8773200660 .
- ^ Диппи, JFJ; Эванс, Р.М. (1950). «Природа катализатора конденсации Перкина». Дж. Орг. Хим . 15 (3): 451–456. дои : 10.1021/jo01149a001 .
- ^ Джонсон, младший (1942). «Реакция Перкина и родственные реакции». Орг. Реагируйте . 1 : 210–265. дои : 10.1002/0471264180.или001.08 . ISBN 0471264180 .
- ^ Хаус, ХО (1972) Современные синтетические реакции , В.А. Бенджамин, Менло-Парк, Калифорния, 2-е изд., стр. 660–663.
- ^ Розен, Т. (1991). «Реакция Перкина». Компр. Орг. Синтез . 2 : 395–408. дои : 10.1016/B978-0-08-052349-1.00034-2 . ISBN 978-0-08-052349-1 .
- ^ Бансал, Радж К. (1998) Механизмы органических реакций , Тата МакГроу Хилл, 3-е издание, стр. 199–201, ISBN 9780470858585 дои : 10.1002/0470858583 .
- ^ Пантен, Йоханнес; Сурбург, Хорст (2016). «Вкусы и ароматизаторы, 3. Ароматические и гетероциклические соединения». Энциклопедия промышленной химии Ульмана . стр. 1–45. дои : 10.1002/14356007.t11_t02 . ISBN 978-3-527-30673-2 .
- ^ Солладье, Ги; Пастурель-Жакопе, Ясин; Меньян, Жан (2003). «Повторное исследование синтеза ресвератрола по реакции Перкинса. Применение к синтезу арилкоричных кислот». Тетраэдр . 59 (18): 3315–3321. дои : 10.1016/S0040-4020(03)00405-8 . ISSN 0040-4020 .