Изотермическая микрокалориметрия
 | |
| Акроним | ММК |
|---|---|
| Классификация | Термический анализ |
| Другие методы | |
| Связанный | Изотермическая титровальная калориметрия Дифференциальная сканирующая калориметрия |
Изотермическая микрокалориметрия ( ИМК ) — лабораторный метод мониторинга и динамического анализа химических, физических и биологических процессов в режиме реального времени. IMC в течение нескольких часов или дней определяет начало, скорость, степень и энергетику таких процессов для образцов в небольших ампулах (например, 3–20 мл) при постоянной заданной температуре (около 15–150 °C).
IMC выполняет этот динамический анализ путем измерения и записи в зависимости от затраченного времени чистой скорости теплового потока (мкДж/с = мкВт) в ампулу с образцом или из нее, а также совокупного количества тепла (Дж), потребленного или произведенного.
IMC является мощным и универсальным аналитическим инструментом по четырем тесно связанным причинам:
- Все химические и физические процессы являются либо экзотермическими, либо эндотермическими — производят или потребляют тепло.
- Скорость теплового потока пропорциональна скорости происходящего процесса.
- IMC достаточно чувствителен, чтобы обнаруживать и отслеживать либо медленные процессы (реакции, протекающие со скоростью несколько процентов в год) в нескольких граммах материала, либо процессы, которые выделяют незначительное количество тепла (например, метаболизм нескольких тысяч живых клеток).
- Приборы IMC обычно имеют огромный динамический диапазон — уровень теплового потока составляет ок. 1 мкВт и до ок. 50 000 мкВт можно измерить тем же прибором.
Таким образом, метод IMC изучения скорости процессов широко применим, обеспечивает непрерывные данные в реальном времени и является чувствительным. Измерение просто провести, оно происходит без присмотра и не мешает (например, не требуются флуоресцентные или радиоактивные маркеры).
Однако есть два основных предостережения, которые следует учитывать при использовании IMC:
- Пропущенные данные : Если используются приготовленные снаружи ампулы с образцами, требуется ок. 40 минут для медленного введения ампулы в прибор без существенного нарушения заданной температуры в измерительном модуле. При этом любые процессы, происходящие в это время, не отслеживаются.
- Посторонние данные : IMC записывает совокупный чистый тепловой поток, производимый или потребляемый всеми процессами, происходящими внутри ампулы. Поэтому, чтобы быть уверенным, какой процесс или процессы производят измеряемый тепловой поток, необходимо проявлять большую осторожность как при планировании эксперимента, так и при первоначальном использовании соответствующих химических, физических и биологических анализов.
В общем, возможные применения IMC ограничены только воображением человека, который решит использовать его в качестве аналитического инструмента, и физическими ограничениями метода. Помимо двух общих ограничений (основных предостережений), описанных выше, эти ограничения включают размер образца и ампулы, а также температуры, при которых можно проводить измерения. IMC обычно лучше всего подходит для оценки процессов, которые происходят в течение нескольких часов или дней. IMC использовался в чрезвычайно широком спектре приложений, и многие примеры обсуждаются в этой статье, подкрепленные ссылками на опубликованную литературу. Обсуждаемые области применения варьируются от измерения медленной окислительной деградации полимеров и нестабильности опасных промышленных химикатов до обнаружения бактерий в моче и оценки воздействия лекарств на паразитических червей. В данной статье основное внимание уделяется приложениям последнего типа — биологии и медицины.
Обзор
[ редактировать ]Определение, цель и сфера применения
[ редактировать ]Этот раздел нуждается в дополнительных цитатах для проверки . ( февраль 2021 г. ) |
Калориметрия — это наука об измерении теплоты химических реакций или физических изменений. Калориметрию проводят с помощью калориметра .
Изотермическая микрокалориметрия (IMC) — это лабораторный метод непрерывного измерения в режиме реального времени скорости теплового потока (мкДж/с = мкВт) и совокупного количества тепла (Дж), потребляемого или выделяемого при практически постоянной температуре образцом, помещенным в IMC. инструмент. Такое тепло возникает из-за химических или физических изменений, происходящих в образце. Тепловой поток пропорционален совокупной скорости изменений, происходящих в данный момент времени. Совокупное количество тепла, произведенное в течение данного интервала времени, пропорционально совокупному количеству произошедших совокупных изменений.
Таким образом, IMC является средством динамической, количественной оценки скоростей и энергетики широкого спектра скоростных процессов, включая биологические процессы. Скорость процесса определяется здесь как физическое и/или химическое изменение, прогресс которого во времени может быть описан либо эмпирически, либо с помощью математической модели ( Библиография : Гласстон и др., 1941 г. и Джонсон и др., 1974 г. и уравнение скорости ).
Простейшим применением IMC является обнаружение того, что в образце происходит один или несколько скоростных процессов, поскольку тепло выделяется или потребляется со скоростью, превышающей предел обнаружения используемого прибора. Это может быть полезно, например, в качестве общего индикатора того, что твердый или жидкий материал не инертен, а изменяется при заданной температуре. В биологических образцах, содержащих питательную среду, появление с течением времени заметного и возрастающего сигнала теплового потока является простым общим индикатором присутствия определенного типа реплицирующихся клеток.

Рис. 1
Однако для большинства приложений крайне важно каким-либо образом знать, какой процесс или процессы измеряются путем мониторинга теплового потока. Как правило, это предполагает сначала получение детальных физических, химических и биологических знаний об объектах, помещенных в ампулу IMC, прежде чем ее помещать в прибор IMC, для оценки теплового потока с течением времени. В этом случае также необходимо проанализировать содержимое ампулы после проведения IMC-измерений теплового потока в течение одного или нескольких периодов времени. Кроме того, логические изменения содержимого ампул могут использоваться для идентификации конкретного источника или источников теплового потока. Когда установлены зависимости скорости процесса и теплового потока, можно напрямую полагаться на данные IMC.
То, что IMC может измерить на практике, частично зависит от размеров образца, и они обязательно ограничены конструкцией прибора. Данный коммерческий прибор обычно принимает образцы фиксированного диаметра и высоты. Приборы, воспринимающие образцы размером до ок. 1 или 2 см в диаметре x ок. Типичная высота 5 см. В данном приборе более крупные образцы данного типа обычно производят более сильные сигналы теплового потока, и это может повысить точность обнаружения и точность.
Часто образцы представляют собой простые цилиндрические ампулы объемом от 3 до 20 мл (рис. 1), содержащие материалы, скорость процессов которых представляет интерес (например, твердые вещества, жидкости, культивируемые клетки), или любую комбинацию этих или других элементов, которые, как ожидается, приведут к производству или потреблению тепла. . Многие полезные измерения IMC можно провести с использованием простых запечатанных ампул, а стеклянные ампулы являются обычным явлением, поскольку стекло не подвержено химическим или физическим изменениям, вызывающим тепло. Однако иногда используют металлические или полимерные ампулы. Кроме того, доступны системы инструментов/ампул, которые позволяют впрыскивать или контролировать поток газов или жидкостей и/или обеспечивают механическое перемешивание образца.
Коммерческие приборы IMC позволяют измерять тепловой поток при температурах от ок. 15 °С – 150 °С. Диапазон для данного инструмента может быть несколько иным.
IMC чрезвычайно чувствителен – например, тепло медленных химических реакций в образцах весом в несколько граммов, протекающих при расходе реагентов в несколько процентов в год, может быть обнаружено и количественно оценено в течение нескольких дней. Примеры включают постепенное окисление полимерных материалов имплантатов и исследования срока годности твердых фармацевтических лекарственных форм ( Применение: Твердые материалы ).
Также можно измерить скорость метаболического производства тепла, например, несколькими тысячами живых клеток, микроорганизмов или простейших в культуре в ампуле IMC. Количество такого метаболического тепла можно коррелировать (посредством экспериментов) с количеством присутствующих клеток или организмов. Таким образом, данные IMC можно использовать для мониторинга в реальном времени количества присутствующих клеток или организмов, а также чистой скорости роста или снижения этого количества ( Приложения: биология и медицина ).
Хотя обсуждаются некоторые небиологические применения IMC ( Приложения: Твердые материалы ), в данной статье основное внимание уделяется использованию IMC в биологических процессах ( Приложения: Биология и медицина ).
Полученные данные
[ редактировать ]
Рис. 2
Графическое отображение данных IMC общего типа показано на рис. 2. Вверху приведен график зарегистрированного теплового потока (мкДж/с = мкВт) в зависимости от времени от образца в запечатанной ампуле из-за экзотермической скорости. процесс, который начинается, ускоряется, достигает максимального теплового потока, а затем затухает. Такие данные непосредственно полезны (например, обнаружение процесса и его продолжительности при фиксированных условиях), но данные также легко оценить математически для определения параметров процесса. Например, на рис. 2 также показано объединение данных о тепловом потоке, где показано накопленное тепло (Дж) в зависимости от времени. Как показано, такие параметры, как максимальная скорость роста (выделения тепла) процесса и продолжительность лаг-фазы, прежде чем процесс достигнет максимального тепла, могут быть рассчитаны на основе интегрированных данных. [1] Расчеты с использованием данных о расходе тепла, хранящихся в компьютерных файлах, легко автоматизировать. Анализ данных IMC таким образом для определения параметров роста имеет важные применения в науках о жизни ( Приложения: биология и медицина ). Кроме того, скорости теплового потока, полученные при ряде температур, можно использовать для определения энергии активации оцениваемого процесса (Hardison et al. 2003). [2]
История развития
[ редактировать ]Лавуазье и Лапласу приписывают создание и использование первого изотермического калориметра ок. 1780 г. ( Библиография: Лавуазье А. и Лаплас PS 1780 ). В их приборе использовался лед для создания относительно постоянной температуры в замкнутом пространстве. Они поняли, что когда они помещали на лед образец, выделяющий тепло (например, живое животное), масса жидкой воды, выделяемой тающим льдом, была прямо пропорциональна теплу, выделяемому образцом. [ нужна ссылка ]
Многие современные конструкции приборов IMC основаны на работах, проделанных в Швеции в конце 1960-х и начале 1970-х годов (Wadsö 1968, [3] Сууркууск и Вадсё 1974 г. [4] ). В этой работе использовались преимущества параллельной разработки твердотельных электронных устройств, в частности коммерческой доступности небольших устройств с термоэлектрическим эффектом (Пельтье-Зебека) для преобразования теплового потока в напряжение — и наоборот. [ нужна ссылка ]
В 1980-е годы появились многоканальные конструкции (Сууркууск, 1982). [5] которые позволяют проводить параллельную оценку нескольких образцов. Это значительно увеличило мощь и полезность IMC и привело к попыткам усовершенствовать метод (Thorén et al. 1989). [6] Большая часть дальнейшего проектирования и разработки, выполненная в 1990-х годах, также была выполнена в Швеции Вадсё и Сууркууском и их коллегами. В этой работе использовались преимущества параллельного развития технологий персональных компьютеров, которые значительно расширили возможности легкого хранения, обработки и интерпретации данных о зависимости теплового потока от времени. [ нужна ссылка ]
Работа по разработке приборов, начавшаяся с 1990-х годов, позволила еще больше воспользоваться преимуществами продолжающегося развития твердотельной электроники и технологий персональных компьютеров. Это привело к созданию инструментов IMC с повышенной чувствительностью и стабильностью, количеством параллельных каналов и еще большей способностью удобно записывать, хранить и быстро обрабатывать данные IMC. В связи с более широким использованием значительное внимание было уделено созданию стандартов для описания характеристик инструментов IMC (например, прецизионность, достоверность, чувствительность) и методов калибровки (Wadsö and Goldberg 2001). [7]
Приборы и принципы измерения
[ редактировать ]Конфигурации приборов
[ редактировать ]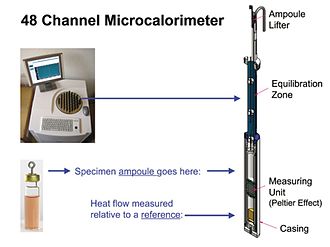
Рис. 3
Современные инструменты IMC на самом деле являются полуадиабатическими, т. е. теплопередача между образцом и его окружением не равна нулю (адиабатическая), поскольку измерение теплового потока IMC зависит от существования небольшого перепада температур - ок. 0,001 °С. [7] Однако, поскольку разница настолько мала, измерения IMC по существу являются изотермическими. На рис. 3 показан обзор прибора IMC, который содержит 48 отдельных модулей измерения теплового потока. Показан один модуль. Измерительным блоком модуля обычно является устройство Пельтье-Зеебека. Устройство создает напряжение, пропорциональное разнице температур между образцом, выделяющим или потребляющим тепло, и термически неактивным эталоном, имеющим температуру радиатора. Разница температур, в свою очередь, пропорциональна скорости, с которой образец выделяет или потребляет тепло (см. «Калибровка» ниже). Все модули в приборе используют один и тот же радиатор и термостат и, таким образом, все выдают данные при одной и той же заданной температуре. Однако, как правило, можно запускать и останавливать измерения в каждой ампуле независимо. В высокопараллельном (например, 48-канальном) приборе, подобном показанному на рис. 3, это позволяет выполнять (начинать и останавливать) несколько различных экспериментов, когда это удобно. [ нужна ссылка ]
Альтернативно, приборы IMC могут быть оснащены дуплексными модулями, которые выдают сигналы, пропорциональные разнице теплового потока между двумя ампулами. Одна из двух таких дуплексных ампул часто является бланком или контролем, т.е. образцом, который не содержит материала, вызывающего интересующий процесс скорости, но содержимое которого в остальном идентично тому, что находится в ампуле для образца. Это дает возможность исключить незначительные реакции с выделением тепла, которые не представляют интереса, например, постепенные химические изменения в течение нескольких дней в среде для культивирования клеток при температуре измерения. Многие полезные измерения IMC можно провести с использованием простых запаянных ампул. Однако, как упоминалось выше, доступны системы инструментов/ампул, которые позволяют или даже контролируют поток газов или жидкостей к образцам и/или от них и/или обеспечивают механическое перемешивание образцов. [ нужна ссылка ]
Справочные вставки
[ редактировать ]Тепловой поток обычно измеряется относительно эталонной вставки, как показано на рис. 3. Обычно это металлический образец , который химически и физически стабилен при любой температуре в рабочем диапазоне прибора и, следовательно, сам не производит и не потребляет тепло. Для достижения наилучших результатов эталон должен иметь теплоемкость, близкую к теплоемкости образца (например, ампула IMC плюс ее содержимое). [ нужна ссылка ]
Режимы работы
[ редактировать ]Режим теплопроводности (hc)
[ редактировать ]Коммерческие приборы IMC часто работают как калориметры теплопроводности (hc), в которых тепло, выделяемое образцом (т.е. материалом в ампуле), течет к радиатору , обычно алюминиевому блоку, помещенному в термостат (например, ванну с постоянной температурой). Как упоминалось выше, прибор IMC, работающий в режиме hc, не является точно изотермическим, поскольку обязательно существуют небольшие различия между заданной температурой и температурой образца, поэтому существует измеримый тепловой поток. Однако небольшие изменения температуры образца не оказывают существенного влияния на температуру радиатора, поскольку теплоемкость радиатора намного выше, чем теплоемкость образца — обычно около 100 мкм. 100×. [ нужна ссылка ]
Передача тепла между образцом и радиатором происходит через устройство Пельтье-Зебека , позволяющее динамически измерять выделяемое или потребляемое тепло. В приборах исследовательского качества температура термостата/радиатора обычно имеет точность < ±0,1 К и поддерживается в пределах ок. < ±100 мкК/24 часа. Точность, с которой поддерживается температура радиатора с течением времени, является основным фактором, определяющим точность измерений теплового потока с течением времени. Преимуществом режима hc является большой динамический диапазон. Тепловые потоки ок. Мощность 50 000 мкВт можно измерить с точностью ок. ±0,2 мкВт. Таким образом, измеряя тепловой поток ок. >0,2 мкВт выше базовой линии представляет собой обнаружение теплового потока, хотя более консервативное обнаружение в 10 раз превышает предел точности. [ нужны разъяснения ] часто используется. [ нужна ссылка ]
Режим компенсации мощности (ПК)
[ редактировать ]Некоторые приборы IMC работают (или могут также работать) как калориметры с компенсацией мощности (ПК). В этом случае для поддержания образца при заданной температуре выделяемое тепло компенсируется с помощью устройства Пельтье-Зебека. Потребляемое тепло компенсируется либо электрическим нагревателем, либо изменением полярности устройства (ван Херваарден, 2000). [8] Если данный прибор работает в режиме pc, а не в режиме hc, точность измерения теплового потока остается той же (например, ±0,2 мкВт). Преимуществом режима компенсации является меньшая постоянная времени – т.е. время, необходимое для обнаружения данного импульса теплового потока, примерно в 10 раз короче, чем в режиме проводимости. Недостатком является ок. Динамический диапазон в 10 раз меньше по сравнению с режимом hc. [ нужна ссылка ]
Калибровка
[ редактировать ]При работе в режиме hc или pc плановая калибровка коммерческих приборов обычно выполняется с помощью встроенных электрических нагревателей. Рабочие характеристики электронагревателей, в свою очередь, можно проверить с использованием образцов с известной теплоемкостью или образцов, которые производят химические реакции, тепловыделение которых на единицу массы известно из термодинамики (Wadsö and Goldberg 2001). [7] В режиме hc или pc результирующий сигнал представляет собой записываемое компьютером напряжение, откалиброванное для представления теплового потока образца в диапазоне мкВт в зависимости от времени. В частности, если в образце не существует значительных температурных градиентов, тогда P = e C [U + t (dU/dt)], где P — тепловой поток (т. е. мкВт), ε C — калибровочная константа, U — измеренная разность потенциалов. на термобатарее и t — постоянная времени. В установившихся условиях, например, при высвобождении постоянного электрического калибровочного тока, это упрощается до P = e C U (Wadsö and Goldberg 2001). [7]
Ампулы
[ редактировать ]Многие весьма полезные измерения IMC могут проводиться в запечатанных ампулах (рис. 1), которые обеспечивают преимущества простоты, защиты от загрязнения и (при необходимости) существенного запаса биологической безопасности для лиц, обращающихся с ампулами или подвергающихся их воздействию. Закрытая ампула может содержать любую желаемую комбинацию твердых веществ, жидкостей, газов или предметов биологического происхождения. Исходный состав газа в головном пространстве ампулы можно контролировать путем герметизации ампулы в желаемой газовой среде. [ нужна ссылка ]
Однако существуют также конструкции приборов/ампул IMC, которые позволяют контролировать поток газа или жидкости через ампулу во время измерения и/или механического перемешивания. Кроме того, при наличии соответствующих принадлежностей некоторые приборы IMC можно использовать как приборы ITC (изотермическая титровальная калориметрия). Тема ITC освещена в другом месте (см. Изотермическая титровальная калориметрия ). Кроме того, некоторые приборы IMC могут регистрировать тепловой поток, в то время как температура медленно изменяется (сканируется) с течением времени. Скорость сканирования должна быть низкой (около ± 2 °C/ч ), чтобы образцы IMC-масштаба (например, несколько граммов) оставались достаточно близкими к температуре радиатора (< примерно 0,1 °C). Быстрое сканирование температуры — это область применения приборов дифференциальной сканирующей калориметрии (ДСК), которые обычно используют образцы гораздо меньшего размера. Некоторые инструменты ДСК могут работать в режиме IMC, но небольшой размер ампулы (и, следовательно, образца), необходимый для сканирования, ограничивает полезность и чувствительность инструментов ДСК, используемых в режиме IMC. [ нужна ссылка ]
Основная методология
[ редактировать ]Установка температуры
[ редактировать ]Измерения скорости теплового потока (мкДж/с = мкВт) выполняются путем установки термостата прибора IMC на выбранную температуру и обеспечения стабилизации теплоотвода прибора при этой температуре. Если прибор IMC, работающий при одной температуре, настроен на новую температуру, повторная стабилизация при новой настройке температуры может занять несколько часов или даже день. Как объяснялось выше, достижение и поддержание точно стабильной температуры имеет основополагающее значение для достижения точных измерений теплового потока в диапазоне мкВт в течение длительного времени (например, дней). [ нужна ссылка ]
Представляем образец
[ редактировать ]После стабилизации температуры, если используется подготовленная снаружи ампула (или какой-либо твердый образец размеров ампулы), ее медленно вводят (например, опускают) в измерительный модуль прибора, обычно поэтапно. Цель состоит в том, чтобы гарантировать, что к моменту нахождения ампулы/образца в положении измерения ее температура будет близка (в пределах примерно 0,001 °C) к температуре измерения. Это делается для того, чтобы любой измеряемый затем тепловой поток был обусловлен процессами скорости образца, а не непрерывным процессом доведения образца до заданной температуры. Время введения образца в ампуле IMC объемом 3–20 мл в положение измерения составляет ок. 40 минут на многих инструментах. Это означает, что тепловой поток от любых процессов, происходящих внутри образца в течение периода введения, не будет зарегистрирован. [ нужна ссылка ]
Если используется ампула на месте и вводится какой-либо агент или образец, это также вызывает период нестабильности, но он составляет порядка ок. 1 минута. На рис. 5 приведены примеры как длительного периода, необходимого для стабилизации инструмента, если ампула вводится напрямую, так и короткого периода нестабильности из-за инъекции. [ нужна ссылка ]
Запись данных
[ редактировать ]После процесса введения тепловой поток образца можно точно регистрировать непрерывно до тех пор, пока он представляет интерес. Чрезвычайная стабильность приборов исследовательского класса (< ±100 мкК/24 часа) означает, что точные измерения могут проводиться (и часто выполняются) в течение нескольких дней. Поскольку сигнал теплового потока по существу считывается в режиме реального времени, он служит средством принятия решения о том, имеет ли место интересующий тепловой поток. Кроме того, современные приборы хранят данные о зависимости теплового потока от времени в виде компьютерных файлов, поэтому возможны как графическое отображение в реальном времени, так и ретроспективное графическое отображение, а также математический анализ данных. [ нужна ссылка ]
Удобство использования
[ редактировать ]Этот раздел нуждается в дополнительных цитатах для проверки . ( февраль 2021 г. ) |
Как указано ниже, IMC имеет множество преимуществ как метод анализа процентных процессов, но есть и некоторые предостережения, на которые следует обратить внимание.
Преимущества
[ редактировать ]Широко применимо
[ редактировать ]Можно изучить любой процесс скорости, если подходящие образцы соответствуют геометрии инструментального модуля IMC, и продолжить со скоростями, подпадающими под методологию IMC (см. выше). Как показано в разделе «Приложения» , IMC используется для количественной оценки чрезвычайно широкого диапазона скоростей процессов in vitro, например, исходя из стабильности полимеров в твердом состоянии (Hardison et al. 2003). [2] эффективности лекарственных соединений против паразитических червей (Maneck et al. 2011). [9] IMC также может определять совокупную частоту нехарактерных, сложных или множественных взаимодействий (Льюис и Дэниелс). [10] Это особенно полезно для сравнительного анализа, например, влияния различных комбинаций состава материала и/или процессов изготовления на общую физико-химическую стабильность.
В режиме реального времени и непрерывно
[ редактировать ]Данные о тепловом потоке IMC получаются как колебания напряжения в зависимости от времени, сохраняются в виде компьютерных файлов и могут отображаться практически в реальном времени — по мере того, как происходит процесс скорости. Напряжение, связанное с тепловым потоком, является постоянным во времени, но в современных приборах оно обычно снимается в цифровом виде. Частоту цифровой выборки можно контролировать по мере необходимости, т. е. частую выборку быстрых изменений теплового потока для лучшего временного разрешения или более медленную выборку медленных изменений, чтобы ограничить размер файла данных.
Чувствительный и быстрый
[ редактировать ]IMC достаточно чувствителен, чтобы за короткое время (часы, дни) обнаружить и количественно оценить реакции, в которых затрачивается лишь несколько процентов реагентов в течение длительного времени (месяцы). Таким образом, IMC позволяет избежать длительного ожидания, часто необходимого для накопления достаточного количества продукта реакции для традиционных (например, химических) анализов. Это относится как к физическим, так и к биологическим образцам (см. «Применение» ).
Прямой
[ редактировать ]При каждой комбинации переменных образца и заданной температуры, представляющей интерес, IMC обеспечивает прямое определение кинетики теплового потока и совокупной теплоты скоростных процессов. Это позволяет избежать необходимости предполагать, что процесс скорости остается неизменным, когда температура или другие контролируемые переменные изменяются перед измерением IMC.
Простой
[ редактировать ]Для сравнения влияния экспериментальных переменных (например, начальных концентраций) на скорость процессов IMC не требует разработки и использования химических или других методов анализа. Если требуются абсолютные данные (например, количество продукта, произведенного в ходе процесса), то анализы можно проводить параллельно с образцами, идентичными тем, которые использовались для ИМК (и/или с образцами ИМК после проведения ИМК). Полученные данные анализа используются для калибровки данных скорости, полученных IMC.
Невмешательство
[ редактировать ]IMC не требует добавления маркеров (например, флуоресцентных или радиоактивных веществ) для регистрации скоростных процессов. Можно использовать неповрежденные образцы, и после проведения IMC образец не изменяется (за исключением происшедших процессов). Образец после IMC может быть подвергнут любому виду физической, химической, морфологической или другой интересующей оценки.
Предостережения
[ редактировать ]Пропущенные данные
[ редактировать ]Как указано в описании методологии, при использовании метода IMC введения запаянной ампулы невозможно уловить тепловой поток в течение первых ок. 40 минут, пока образец медленно доводится до заданной температуры. Таким образом, в этом режиме IMC лучше всего подходит для изучения процессов, которые медленно начинаются или медленно протекают при заданной температуре. Это предостережение также применимо ко времени перед введением, т. е. времени, прошедшему между подготовкой образца (в ходе которой затем может начаться процесс введения) и началом процесса введения IMC (Charlebois et al. 2003). [11] Этот последний эффект обычно минимизируется, если температура, выбранная для IMC, существенно выше (например, 37 °C), чем температура, при которой готовится образец (например, 25 °C).
Посторонние данные
[ редактировать ]IMC фиксирует совокупное производство или потребление тепла в результате всех процессов, происходящих внутри образца, включая, например,
- Возможные изменения физико-химического состояния самой ампулы с образцом; например, релаксация напряжений в металлических компонентах, окисление полимерных компонентов.
- Деградация культуральной среды, в которой изучают метаболизм и рост живых клеток.
Таким образом, при планировании и проектировании эксперимента необходимо проявлять большую осторожность, чтобы выявить все возможные процессы, которые могут иметь место. Часто необходимо разработать и провести предварительные исследования, направленные на систематическое определение того, происходят ли множественные процессы, и если да, то их вклад в совокупный тепловой поток. Одна из стратегий, позволяющая исключить посторонние данные о тепловом потоке, заключается в сравнении теплового потока образца, в котором происходит интересующий процесс скорости, с потоком холостого образца, который включает в себя все, что есть в интересующем образце, за исключением элемента, который будет пройти процентный процесс. Этого можно добиться напрямую с помощью приборов, имеющих дуплексные модули IMC, которые сообщают о разнице чистого теплового потока между двумя ампулами.
Приложения
[ редактировать ]Этот раздел нуждается в дополнительных цитатах для проверки . ( февраль 2021 г. ) |
После обсуждения некоторых специальных источников информации о применении IMC рассматриваются несколько конкретных категорий IMC-анализа скоростных процессов, а также недавние примеры (со ссылками на литературу) обсуждаются в каждой категории.
Специальные источники информации о применении IMC
[ редактировать ]Справочники
[ редактировать ]В библиографии перечислены четыре обширных тома Справочника по термическому анализу и калориметрии: Vol. 1 Принципы и практика (1998), Vol. 2 Приложения к неорганическим и другим материалам (2003), Vol. 3 Приложения к полимерам и пластмассам (2002 г.) и Vol. 4 От макромолекул к человеку (1999). Они представляют собой основной источник информации (и ссылок на литературу) о приложениях и примерах IMC, опубликованных до ок. 2000.
Замечания по применению
[ редактировать ]Некоторые производители приборов IMC собрали рекомендации по применению и сделали их доступными для общественности. Примечания часто (но не всегда) представляют собой адаптацию журнальных статей. Примером может служить Сборник микрокалориметрии Vol. I и II, предложенные TA Instruments, Inc. и перечисленные в библиографии .
«Белки» первый раздел примечаний в т. I не представляет здесь интереса, так как описывает исследования, использующие изотермическую титровальную калориметрию . Последующие разделы Vol. I, Life & Biological Sciences и Pharmaceuticals содержат рекомендации по применению как IMC, так и дифференциальной сканирующей калориметрии . Том. II сборника почти полностью посвящен приложениям IMC. Его разделы озаглавлены «Цемент», «Энергетика», «Материалы» и «Другое». Возможным недостатком этих двух конкретных сборников является то, что ни одна из примечаний не датирована. Хотя сборники были опубликованы в 2009 году, в некоторых примечаниях описываются инструменты IMC, которые использовались много лет назад и больше не доступны. Таким образом, некоторые из заметок, хотя и актуальны и поучительны, часто описывают исследования, проведенные до 2000 года.
Примеры приложений
[ редактировать ]В целом, возможные применения IMC ограничены только воображением человека, который решит использовать IMC в качестве аналитического инструмента — в рамках ранее описанных ограничений, представленных существующими инструментами и методологией IMC. Это связано с тем, что это универсальное средство контроля скорости любого химического, физического или биологического процесса. Ниже приведены некоторые категории приложений IMC с примерами в каждой. В большинстве категорий опубликованных примеров гораздо больше, чем упомянутых и на которые ссылаются. Категории несколько произвольны и часто пересекаются. Другой набор категорий может быть столь же логичным, и можно добавить больше категорий.
Твердые материалы
[ редактировать ]Формирование
[ редактировать ]ИМК широко используется для изучения скорости образования различных материалов различными процессами. Лучше всего он подходит для изучения процессов, которые происходят медленно, т. е. в течение нескольких часов или дней. Ярким примером является изучение реакций гидратации и схватывания составов кальциево-минеральных цементов. В одной статье представлен обзор (Гавлицкий и др., 2010 г.). [12] а другой описывает простой подход (Evju 2003). [13] Другие исследования сосредоточены на понимании гидратации цемента, полученном с помощью IMC в сочетании с ИК-спектроскопией (Ylmen et al. 2010). [14] и об использовании IMC для изучения влияния переменных состава на гидратацию цемента и время схватывания (Xu et al. 2011). [15]
IMC также можно удобно использовать для изучения скорости и количества гидратации (в воздухе известной влажности) минералов кальция или других минералов. Чтобы обеспечить для таких исследований воздух известной влажности, в ампулу ИМС вместе с негидратированным минеральным образцом можно поместить небольшие емкости с насыщенными растворами солей. Затем ампулу запечатывают и вводят в прибор IMC. Насыщенный раствор соли поддерживает температуру воздуха в ампуле при известной относительной влажности, а различные растворы поваренной соли обеспечивают влажность в диапазоне, например, 32-100% относительной влажности. Такие исследования были проведены на частицах гидроксиапатита кальция в диапазоне микронных размеров и «нано» частицах кальцийсодержащего биоактивного стекла (Doostmohammadi et al. 2011). [16]
Стабильность
[ редактировать ]IMC хорошо подходит для быстрого количественного определения скорости медленных изменений материалов (Willson et al. 1995). [17] Такие оценки по-разному описываются как исследования стабильности, деградации или срока годности .

Рис. 4
Например, IMC уже много лет широко используется при изучении срока годности твердых лекарственных форм в фармацевтической промышленности (Pikal et al. 1989, [18] Хансен и др. 1990, [19] Кенигбауэр и др. 1992 год [20] ) IMC обладает способностью обнаруживать медленную деградацию во время имитации хранения на полке гораздо раньше, чем традиционные аналитические методы, и без необходимости использования методов химического анализа. IMC также является быстрым и чувствительным методом определения часто функционально важного аморфного содержания таких лекарств, как нифедипин (Vivoda et al. 2011). [21]
IMC можно использовать для быстрого определения скорости медленных изменений в промышленных полимерах. Например, известно, что стерилизация гамма-излучением материала, часто используемого для хирургических имплантатов, — полиэтилена сверхвысокой молекулярной массы (СВМПЭ), — приводит к образованию свободных радикалов в полимере. Результатом является медленное окисление и постепенное нежелательное охрупчивание полимера на полке или в естественных условиях. IMC смог обнаружить тепло, связанное с окислением, и количественно определить скорость окисления, составляющую ок. 1% в год в облученном СВМПЭ при комнатной температуре на воздухе (Charlebois et al. 2003). [11] В соответствующем исследовании энергия активации была определена на основе измерений при ряде температур (Hardison et al. 2003). [2]
IMC также очень полезен при оценке «потенциала выхода из-под контроля» материалов, которые представляют значительную опасность пожара или взрыва. Например, его использовали для определения автокаталитической кинетики гидропероксида кумола (ГПК), промежуточного продукта, который используется в химической промышленности и внезапное разложение которого привело к ряду пожаров и взрывов. На рис. 4 показаны данные IMC, подтверждающие термическое разложение ГПК при 5 различных температурах (Chen et al. 2008). [22]
Биология и медицина
[ редактировать ]Термин «метаболика» можно использовать [ нужна ссылка ] для описания исследований количественного измерения скорости производства или потребления тепла в зависимости от времени клетками (включая микробы) в культуре, образцами тканей или небольшими целыми организмами. Как будет описано далее, метаболизм может быть полезен в качестве диагностического инструмента; особенно при (а) определении природы образца по его тепловому потоку в зависимости от временной характеристики при заданном наборе условий, или (б) определении воздействия, например, фармацевтических соединений на метаболические процессы, органический рост или жизнеспособность. Метаболизмика связана с метаболомикой . Последнее представляет собой систематическое изучение уникальных химических отпечатков пальцев, которые оставляют после себя определенные клеточные процессы; т.е. изучение профилей их низкомолекулярных метаболитов. Когда IMC используется для определения метаболизма, продукты изученных метаболических процессов впоследствии становятся доступными для метаболомических исследований. Поскольку в IMC не используются биохимические или радиоактивные маркеры, образцы после IMC состоят только из продуктов метаболизма и оставшейся культуральной среды (если таковая использовалась). Если метаболизмика и метаболомика используются вместе, они могут обеспечить полную запись метаболического процесса, происходящего in vitro: его скорости и энергетики, а также продуктов метаболизма.
Чтобы определить метаболизм с использованием IMC, конечно, изначально должно присутствовать достаточное количество клеток, тканей или организмов (или присутствовать позже, если во время измерений IMC происходит репликация), чтобы генерировать сигнал теплового потока, превышающий предел обнаружения данного прибора. Знаковая общая статья 2002 года по теме метаболизма дает прекрасную перспективу для рассмотрения исследований метаболизма IMC (см. Библиографию , West, Woodruff and Brown 2002). Он описывает, как связаны скорости метаболизма и как они масштабируются во всем диапазоне от «молекул и митохондрий до клеток и млекопитающих». Что важно для IMC, авторы также отмечают, что, хотя скорость метаболизма данного типа клеток млекопитающих in vivo заметно снижается с увеличением размера (массы) животного, размер животного-донора не влияет на скорость метаболизма клеток при культивировании. in vitro.
Биология клеток и тканей
[ редактировать ]Клетки млекопитающих в культуре имеют скорость метаболизма ок. 30×10 −12 Вт/клетку (рис. 2 и 3 в библиографии: West, Woodruff and Brown 2002 ). По определению, приборы IMC имеют чувствительность не менее 1×10 −6 Вт (т.е. 1 мкВт). Следовательно, метаболическое тепло ок. Обнаружено 33 000 клеток. Основываясь на этой чувствительности, IMC использовался для выполнения большого количества новаторских исследований метаболизма культивируемых клеток млекопитающих в 1970-х и 1980-х годах в Швеции. Одна статья (Монти, 1990 г.) [23] служит обширным руководством по работе, проделанной до 1990 года. Он включает пояснительный текст и 42 ссылки на исследования IMC теплового потока из культивируемых человеческих эритроцитов , тромбоцитов , лимфоцитов , клеток лимфомы, гранулоцитов , адипоцитов , скелетных мышц и ткани миокарда. Исследования были проведены, чтобы определить, как и где IMC можно использовать в качестве метода клинической диагностики и/или дать представление о метаболических различиях между клетками здоровых людей и людей с различными заболеваниями или проблемами со здоровьем.
События с ок. 2000 год в IMC (например, массово-параллельные инструменты, компьютерное хранение данных в реальном времени и анализ данных о тепловом потоке) стимулировали дальнейшее использование IMC в биологии культивируемых клеток. Например, IMC оценивали для оценки антиген-индуцированной пролиферации лимфоцитов (Murigande et al. 2009). [24] и выявили аспекты пролиферации, не наблюдаемые с помощью обычного метода прерывистого анализа радиоактивных маркеров. IMC также применяется в области тканевой инженерии . Одно исследование (Санторо и др., 2011 г.) [25] продемонстрировали, что IMC можно использовать для измерения скорости роста (т.е. пролиферации) в культуре хондроцитов человека , собранных для использования в тканевой инженерии. Оно показало, что IMC потенциально может служить для определения эффективности различных составов питательных сред, а также для определения того, можно ли выращивать клетки, пожертвованные данным человеком, достаточно эффективно, чтобы рассмотреть возможность их использования для производства инженерной ткани.
IMC также использовался для измерения метаболической реакции культивируемых макрофагов на остатки износа хирургических имплантатов. IMC показала, что реакция была сильнее на частицы полиэтилена размером в микрометр, чем на частицы сплава Co аналогичного размера (Charlebois et al. 2002). [26] Соответствующий документ охватывает общую тему применения IMC в области синтетических твердых материалов, используемых в хирургии и медицине (Lewis and Daniels 2003). [10]
По крайней мере, два исследования показали, что IMC может иметь существенное значение при опухолевой патологии. В одном исследовании (Bäckman 1990) [27] измеряли скорость теплопродукции клеток Т-лимфомы, культивированных в суспензии. Изменения температуры и pH вызывали значительные изменения, но не скорость перемешивания и концентрация клеток. Более прямое исследование возможного диагностического использования (Каллерхофф и др., 1996). [28] дал многообещающие результаты. Для изученных образцов биопсии урогенитальной ткани результаты показали:
«Можно дифференцировать образцы нормальной и опухолевой ткани с помощью микрокалориметрического измерения, основанного на явно более высокой метаболической активности злокачественной ткани. Кроме того, микрокалориметрия позволяет дифференцировать и классифицировать образцы тканей по их гистологической классификации».
Токсикология
[ редактировать ]По состоянию на 2012 год IMC не получил широкого распространения в токсикологии культивируемых клеток, хотя он периодически и успешно использовался с 1980-х годов. IMC полезен в токсикологии, когда желательно наблюдать метаболизм культивируемых клеток в режиме реального времени и количественно определять скорость снижения метаболизма в зависимости от концентрации возможно токсичного агента. Одно из самых ранних сообщений (Анкерст и др., 1986). [29] Одним из вариантов использования ИМК в токсикологии стало изучение антителозависимой клеточной токсичности (ADCC) в отношении клеток меланомы человека различных комбинаций антисыворотки, моноклональных антител, а также лимфоцитов периферической крови в качестве эффекторных клеток. Кинетику метаболического теплового потока клеток меланомы в зависимости от времени в закрытых ампулах измеряли в течение 20 часов. Авторы пришли к выводу, что
«...микрокалориметрия является чувствительным и особенно подходящим методом анализа кинетики цитотоксичности».
IMC также используется в экологической токсикологии. В раннем исследовании (Торен, 1992) [30] токсичность в отношении монослоев альвеолярных макрофагов частиц MnO 2 , TiO 2 и SiO 2 оценивали (кремнезема). Результаты IMC соответствовали результатам, полученным с помощью окрашивания эфиром флуоресцеина и анализа микроскопических изображений, за исключением того, что IMC показал токсическое воздействие кварца, не различимое при анализе изображений. Это последнее наблюдение – в соответствии с известными альвеолярными эффектами – показало авторам, что IMC является более чувствительным методом.

Гораздо позже (Лю и др., 2007 г.) [31] Было показано, что IMC предоставляет динамические метаболические данные, которые оценивают токсичность хромата калия в отношении фибробластов Cr(VI). На рис. 5 показаны исходные результаты определения метаболического теплового потока от культивируемых фибробластов до оценки воздействия Cr(VI). Авторы пришли к выводу, что
«Микрокалориметрия оказывается удобным и простым методом измерения метаболических процессов... в... живых клетках. В отличие от стандартных процедур биоанализа, этот метод позволяет непрерывно измерять метаболизм живых клеток. Таким образом, мы показали, что Cr( VI) нарушает метаболические пути фибробластов человека и особенно утилизацию глюкозы».
Простая IMC в закрытой ампуле также использовалась и пропагандировалась для оценки токсичности культивируемых клеток материалов-кандидатов на хирургические имплантаты и, таким образом, служила методом скрининга биосовместимости. В одном исследовании (Xie et al. 2000) [32] Клетки почечных канальцев свиньи в культуре подвергались воздействию как полимеров, так и металлического титана в форме «микропланшет» с известной площадью поверхности в несколько см2. 2 . Авторы пришли к выводу, что IMC
«...это быстрый метод, удобный в использовании и с хорошей воспроизводимостью. Настоящий метод может в большинстве случаев заменить более трудоемкие световые и электронные микроскопические исследования для количественного определения прилипших клеток».
В другом исследовании материалов для имплантатов (Doostmohammadi et al. 2011) [33] как быстрорастущая культура дрожжей, так и культура хондроцитов человека подвергались воздействию частиц (диаметром <50 мкм) гидроксиапатита кальция (ГА) и биоактивного (кальцийсодержащего) кварцевого стекла. Частицы стекла замедляли или ограничивали рост дрожжей в зависимости от увеличения концентрации частиц. Частицы ГК имели гораздо меньший эффект и никогда полностью не подавляли рост дрожжей в тех же концентрациях. Влияние обоих типов частиц на рост хондроцитов было минимальным при используемой концентрации. Авторы пришли к выводу, что
«Цитотоксичность дисперсных материалов, таких как биоактивное стекло и частицы гидроксиапатита, можно оценить с помощью метода микрокалориметрии. Это современный метод исследования in vitro биосовместимости и цитотоксичности биоматериалов, который можно использовать наряду со старыми традиционными анализами».
Микробиология
[ редактировать ]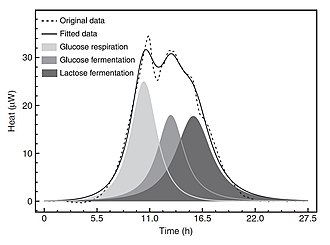
Публикации, описывающие использование IMC в микробиологии, начались в 1980-х годах (Jesperson 1982). [34] Хотя некоторые микробиологические исследования IMC были направлены на вирусы (Heng et al. 2005), [35] и грибы (Antoci et al. 1997), [36] большинство из них были связаны с бактериями. Недавняя статья (Брайссан и др., 2010 г.) [37] представляет общее введение в метаболические методы IMC в микробиологии и обзор их применения в медицинской и экологической микробиологии. В статье также объясняется, как данные о зависимости теплового потока от времени для бактерий в культуре являются точным выражением — как они происходят с течением времени — колебаний метаболической активности микроорганизмов и скорости репликации в данной среде (рис. 6).

В целом бактерии составляют примерно 1/10 размера клеток млекопитающих и производят примерно 1/10 меньше метаболического тепла, т.е. 3x10 −12 Вт/сот. Таким образом, по сравнению с клетками млекопитающих (см. выше) ок. В 10 раз больше бактерий — ок. 330 000 — должно присутствовать для создания обнаруживаемого теплового потока — т.е. 1 мкВт. [37] Однако многие бактерии размножаются в культуре на несколько порядков быстрее, чем клетки млекопитающих, часто удваивая свою численность за считанные минуты (см. « Рост бактерий »). В результате небольшое первоначальное количество бактерий в культуре, первоначально не обнаруживаемое с помощью IMC, быстро образует обнаруживаемое количество. Например, 100 бактерий, удваивающихся каждые 20 минут, менее чем за 4 часа произведут >330 000 бактерий и, таким образом, создадут тепловой поток, обнаруживаемый с помощью IMC. Следовательно, IMC можно использовать для простого и быстрого обнаружения бактерий в медицинской сфере. Примеры включают обнаружение бактерий в продуктах тромбоцитов человеческой крови (Trampuz et al. 2007). [38] и моча (Бонкат и др., 2011 г.) [39] и быстрое выявление туберкулеза (Braissant et al. 2010, [40] Родригес и др. 2011 год [41] ). На рис. 7 показан пример времени обнаружения туберкулезных бактерий в зависимости от исходного количества бактерий, присутствующих в закрытой ампуле IMC, содержащей культуральную среду.
Для микробов в питательной среде в закрытых ампулах данные теплового потока IMC также можно использовать для точной оценки основных параметров роста микробов; т.е. максимальный темп роста и продолжительность лаг-фазы до достижения максимального темпа роста. Это важное специальное применение базового анализа этих параметров, описанное ранее ( Обзор: Полученные данные ).
К сожалению, в литературе IMC есть несколько опубликованных работ, в которых связь между данными о тепловом потоке и ростом микробов в закрытых ампулах была неправильно понята. Однако в 2013 году было опубликовано обширное разъяснение, описывающее (а) детали связи между данными IMC о тепловом потоке и ростом микробов, (b) выбор математических моделей, описывающих рост микробов, и (c) определение параметров роста микробов на основе данных IMC. используя эти модели (Брайссан и др., 2013). [42]
Фармакодинамика
[ редактировать ]В качестве логического расширения способности IMC обнаруживать и количественно определять рост бактерий можно добавлять известные концентрации антибиотиков к бактериальной культуре, а затем использовать IMC для количественной оценки их воздействия на жизнеспособность и рост. Закрытая ампула IMC позволяет легко получить основную фармакологическую информацию, например минимальную ингибирующую концентрацию (МИК) антибиотика, необходимую для остановки роста данного организма. Кроме того, он может одновременно обеспечивать динамические параметры роста — время задержки и максимальную скорость роста (см. рис. 2, Howell et al. 2011, Braissant et al. 2013), [1] [42] которые оценивают механизмы действия. На бактерицидное действие (см. Бактерицид ) указывает увеличение времени задержки в зависимости от увеличения концентрации антибиотика, тогда как на бактериостатическое действие (см. Бактериостатическое средство ) указывает уменьшение скорости роста с увеличением концентрации. Подход IMC к оценке антибиотиков был продемонстрирован для ряда типов бактерий и антибиотиков (фон Ах и др., 2009). [43] IMC в закрытой ампуле также позволяет быстро различать нормальные и резистентные штаммы бактерий, таких как Staphylococcus aureus (von Ah et al. 2008, [44] Бальдони и др. 2009 год [45] ). IMC также использовался для оценки воздействия дезинфицирующих средств на жизнеспособность бактерий полости рта, прикрепившихся к материалам зубных имплантатов (Астасов-Фрауенхоффер и др., 2011). [46] В аналогичном более раннем исследовании IMC использовался для измерения теплоты адгезии зубных бактерий к стеклу (Hauser-Gerspach et al. 2008). [47]
Было продемонстрировано аналогичное успешное использование IMC для определения воздействия противоопухолевых препаратов на опухолевые клетки в культуре в течение нескольких часов (Schön and Wadsö, 1988). [48] Вместо подхода с закрытыми ампулами использовалась установка IMC, которая позволяла вводить лекарственное средство в перемешиваемые образцы.
По состоянию на 2013 год IMC использовался менее широко в фармакодинамических исследованиях in vitro на клетках млекопитающих, чем в микробных исследованиях.
Многоклеточные организмы
[ редактировать ]Можно использовать IMC для изучения метаболизма живых многоклеточных организмов, если они достаточно малы, чтобы их можно было поместить в ампулы IMC (Lamprecht & Becker 1988). [49] Были проведены исследования IMC метаболизма куколки насекомых во время дыхательных движений (Harak et al. 1996). [50] и влияние химических веществ на рост куколки (Kuusik et al. 1995). [51] IMC также доказала свою эффективность при оценке влияния старения на метаболизм нематод (Braekman et al. 2002). [52]
IMC также оказалась весьма полезной для оценки in vitro воздействия фармацевтических препаратов на тропических паразитических червей (Manneck et al. 2011-1, [53] Манек и др. 2011-2, [9] Кирххофер и др. 2011). [54] Интересной особенностью этих исследований является использование простой ручной системы инъекции для введения фармацевтических препаратов в запечатанные ампулы, содержащие червей. Кроме того, IMC не только документирует общее снижение метаболизма с течением времени из-за лекарств, но также общую частоту двигательной активности червей и ее снижение амплитуды с течением времени, что отражается в колебаниях данных о тепловом потоке.
Экологическая биология
[ редактировать ]Благодаря своей универсальности IMC может быть эффективным инструментом в области биологии растений и окружающей среды. В одном из ранних исследований (Hansen et al. 1989) [55] измеряли скорость метаболизма образцов тканей клонов лиственницы. Эта скорость предсказывала долгосрочные темпы роста деревьев, была одинаковой для образцов с данного дерева и, как было обнаружено, коррелировала с известными вариациями в долгосрочном росте клонов разных деревьев.
Бактериальный оксалотрофный метаболизм распространен в окружающей среде, особенно в почвах. Оксалотрофные бактерии способны использовать оксалат в качестве единственного источника углерода и энергии. IMC в закрытой ампуле использовали для изучения метаболизма оксалотрофных почвенных бактерий, подвергавшихся воздействию как оптимизированной среды, содержащей оксалат калия в качестве единственного источника углерода, так и модельной почвы (Bravo et al. 2011). [56] Используя оптимизированную среду, рост шести различных штаммов почвенных бактерий можно было легко контролировать, воспроизводимо количественно определять и дифференцировать в течение нескольких дней. Измерение IMC бактериального метаболического теплового потока в модельной почве было более сложным, но доказательство концепции было продемонстрировано.
Лунное молоко — белый кремовый материал, найденный в пещерах. Это незатвердевающий мелкокристаллический осадок из известняка, состоящий в основном из карбонатов кальция и/или магния. В его образовании могут участвовать микробы. Трудно сделать вывод о микробной активности лунного молока на основе стандартных статических химических и микроскопических анализов состава и структуры лунного молока. Для решения этой проблемы использовалась закрытая ампула IMC (Braissant, Bindscheidler et al. 2011). [57] Определить скорость роста хемогетеротрофных микробных сообществ на лунном молоке удалось после добавления различных источников углерода, имитирующих смеси, которые будут контактировать с лунным молоком в результате таяния снега или осадков. Метаболическая активность была высокой и сравнима с таковой в некоторых почвах.
Харрис и др. (2012), [58] изучая различные режимы внесения удобрений, обнаружили, что, если выразить это как тепловыделение на единицу микробной биомассы почвы, микробные сообщества при режимах использования органических удобрений производят меньше отработанного тепла, чем при неорганических режимах.
Пищевая наука
[ редактировать ]Было показано, что IMC находит разнообразное применение в пищевой науке и технологиях. Обзор (Вадсё и Галиндо, 2009 г.) [59] обсуждаются успешные применения в оценке дыхания на ранах от обрезков овощей, гибели клеток в результате бланширования, ферментации молока, предотвращения микробиологической порчи, термической обработки и срока годности. Другая публикация (Галиндо и др., 2005 г.) [60] рассматривается успешное использование IMC для мониторинга и прогнозирования изменений качества во время хранения минимально обработанных фруктов и овощей.
IMC также доказала свою эффективность при проведении ферментативного анализа оротовой кислоты в молоке (Анастаси и др., 2000). [61] и яблочная кислота во фруктах, винах и других напитках, а также в косметических продуктах (Antonelli et al. 2008). [62] IMC также использовался для оценки эффективности средств против потемнения свежесрезанного картофеля (Rocculi et al. 2007). [63] IMC также доказал свою эффективность при оценке степени, в которой низкоэнергетические импульсные электрические поля (PEF) влияют на теплоту прорастания семян ячменя , что важно в связи с их использованием в производстве солодовых напитков (Dymek et al. 2012). [64]
См. также
[ редактировать ]- Калориметрия
- Химическая термодинамика
- Дифференциальная сканирующая калориметрия
- Изотермическая титровальная калориметрия
- Уравнение скорости
- Сорбционная калориметрия
- Термический анализ
- Термоэлектрический эффект
Библиография
[ редактировать ]- Харрис, Дж.А.; Ритц, К; Кушени, Э; Грайс, С.М.; Лерх, ТЗ; Паулетт, М; Херрманн, AM (2012). «Термодинамическая эффективность почвенных микробных сообществ, подверженных длительному стрессу, ниже, чем при обычных режимах внесения». Биология и биохимия почвы . 47 : 149–157. Бибкод : 2012SBiBi..47..149H . doi : 10.1016/j.soilbio.2011.12.017 .
- Гласстоун С., Лайдлер К.Дж., Эйринг Х. (1941) Теория скоростных процессов: кинетика химических реакций, вязкости, диффузии и электрохимических явлений. МакГроу-Хилл (Нью-Йорк). 611 стр.
- Джонсон Ф.Х., Айринг Х., Стовер Б.Дж. (1974)Теория скоростных процессов в биологии и медицине. Уайли (Нью-Йорк), ISBN 0-471-44485-5 , 703 стр.
- Лавуазье А. и Лаплас П.С. (1780) Мемуары о жаре. Академия наук, Париж.
- Браун М.Э., редактор (1998), Vol. 1 Принципы и практика (691 стр.), в Справочнике по термическому анализу и калориметрии. Галлахер П.К. (редактор серии). Эльзевир (Лондон).
- Браун М.Э. и Галлахер П.К., Редакторы (2003), Том. 2 приложения к неорганическим и другим материалам (905 стр.), в Справочнике по термическому анализу и калориметрии. Галлахер П.К. (редактор серии). Эльзевир (Лондон). ISBN 978-0-444-82086-0
- Ченг СЗД, редактор (2002) Том. 3 приложения к полимерам и пластмассам (828 стр.) в Справочнике по термическому анализу и калориметрии. Галлахер П.К. (редактор серии). Эльзевир (Лондон).
- Кемп Р.Б., редактор (1999) Vol. 4 От макромолекул к человеку (1032 стр.), в Справочнике по термическому анализу и калориметрии. Галлахер П.К. (редактор серии). Эльзевир (Лондон).
- Справочник по микрокалориметрии, том. 1: Белки, биологические и биологические науки, фармацевтика (2009). TA Instruments, Inc. (Нью-Касл, Делавэр, США).
- Справочник по микрокалориметрии, том. 2: Цемент, энергетика, материалы, прочее (2009). TA Instruments, Inc. (Нью-Касл, Делавэр, США).
- Уэст, Великобритания; Вудрафф, Вашингтон; Браун, Дж. Х. (2002). «Аллометрическое масштабирование скорости метаболизма от молекул и митохондрий до клеток и млекопитающих» . ПНАС . 99 (Приложение 1): 2473–2478. Бибкод : 2002PNAS...99.2473W . дои : 10.1073/pnas.012579799 . ПМЦ 128563 . ПМИД 11875197 .
Ссылки
[ редактировать ]- ^ Jump up to: а б Хауэлл, М; Вирц Д; Дэниэлс АУ; Брейссан О (ноябрь 2011 г.). «Применение микрокалориметрического метода определения лекарственной чувствительности видов микобактерий» . Журнал клинической микробиологии . 50 (1): 16–20. дои : 10.1128/JCM.05556-11 . ПМЦ 3256699 . ПМИД 22090404 .
- ^ Jump up to: а б с Хардисон, А; Льюис Г.В.; Дэниелс AU (2003). «Определение энергий активации и совокупных скоростей экзотермических физико-химических изменений в СВМПЭ методом изотермической теплопроводной микрокалориметрии (ИГКМЦ)». Биоматериалы . 24 (28): 5145–51. дои : 10.1016/S0142-9612(03)00461-7 . ПМИД 14568431 .
- ^ Вадсё, Л. (1968). «Проектирование и испытание микрореакционного калориметра» (PDF) . Acta Chemica Scandinavica . 22 : 927–937. doi : 10.3891/acta.chem.scand.22-0927 .
- ^ Сууркууск, Ж; Вадсё, Л. (1974). «Разработка и испытания усовершенствованного прецизионного капельного калориметра для измерения теплоемкости небольших образцов». Дж. Хим. Термодинамика . 6 (7): 667–679. Бибкод : 1974JChTh...6..667S . дои : 10.1016/0021-9614(74)90117-7 .
- ^ Сууркууск Дж, Вадсё I (1982). «Многоканальная микрокалориметрическая система». Химика Скрипта . 20 : 155–163. ISSN 0004-2056 .
- ^ Торен, ЮАР; Сууркууск Ж; Холма Б. (1989). «Работа многоканальной микрокалориметрической системы в микросубмикваттном диапазоне: некоторые методические аспекты». Журнал биохимических и биофизических методов . 18 (2): 149–156. дои : 10.1016/0165-022X(89)90076-6 . ПМИД 2745930 .
- ^ Jump up to: а б с д Вадсё, я; Гольдберг, Р.Н. (2001). «Эталоны в изотермической микрокалориметрии» . Чистое приложение. Хим . 73 (10): 1625–1639. дои : 10.1351/pac200173101625 . S2CID 44976071 .
- ^ ван Херваарден, С. (2000). «17. Калориметрические измерения». В Вебстере, Дж. Г. (ред.). Измерение механических переменных — твердых, жидких и термических . ЦРК Пресс. стр. 17.1–16. дои : 10.1201/9781003418214-17 . ISBN 978-1-003-41821-4 .
- ^ Jump up to: а б Маннек, Т; Брейссан О; Хаггенмюллер Ю; Кейзер Дж (2011). «Изотермическая микрокалориметрия для изучения препаратов против Schistosoma mansoni» . Журнал клинической микробиологии . 49 (4): 1217–25. дои : 10.1128/JCM.02382-10 . ПМК 3122815 . ПМИД 21270220 .
- ^ Jump up to: а б Льюис, Дж; Дэниелс AU (2003). «Использование изотермической теплопроводной микрокалориметрии (IHCMC) для оценки синтетических биоматериалов». Дж. Биомед. Матер. Рез. Б. 66Б (2): 487–501. CiteSeerX 10.1.1.517.6452 . дои : 10.1002/jbm.b.10044 . ПМИД 12861599 .
- ^ Jump up to: а б Шарлебуа, SJ; Дэниэлс АУ; Льюис Дж. (2003). «Изотермическая микрокалориметрия: аналитический метод оценки динамической химической стабильности СВМПЭ». Биоматериалы . 24 (2): 91–296. дои : 10.1016/S0142-9612(02)00317-4 . ПМИД 12419630 .
- ^ Гавлицкий, М; Нокун-Вчелик, Ж; Бак, Л. (2010). «Калориметрия в исследованиях гидратации цемента». J Therm Анальный Калорим . 100 (2): 571–6. дои : 10.1007/s10973-009-0158-5 . S2CID 137241273 .
- ^ Эвью, К. (2003). «Первоначальная гидратация цементирующих систем с использованием простого изотермического калориметра и динамической коррекции». J Therm Анальный Калорим . 71 (3): 829–40. дои : 10.1023/A:1023374125778 . S2CID 93452683 .
- ^ Ильмен, Р; Вадсо, Л; Панас, Я (2010). «Изучение ранней гидратации портландизвестнякового цемента с помощью инфракрасной спектроскопии и изотермической калориметрии». Cem Concr Res . 40 (10): 1541–6. doi : 10.1016/j.cemconres.2010.06.008 .
- ^ Сюй Л, Ван П, Чжан Г (ноябрь 2012 г.). «Калориметрическое исследование влияния сульфата кальция на гидратацию портландцементно-алюминатно-кальциевых цементных смесей». Журнал термического анализа и калориметрии . 110 (2): 725–731. дои : 10.1007/s10973-011-1920-z .
- ^ Дустмохаммади, А; Монши, А; Фатхи, Массачусетс; Брейссан, О (2011). «Сравнительное физико-химическое исследование биоактивного стекла и гидроксиапатита костного происхождения». Керамика Интернешнл . 37 (5): 1601–1607. doi : 10.1016/j.ceramint.2011.03.009 .
- ^ Уилсон, Р.Дж.; Бизер, А.Е.; Митчелл, Джей Си; Ло, В. (1995). «Определение термодинамических и кинетических параметров с помощью изотермической микрокалориметрии теплопроводности: приложения к долгосрочным исследованиям реакций». Дж. Физ. Хим . 99 (18): 7108–7113. дои : 10.1021/j100018a051 .
- ^ Пикал, MJ; Деллерман, К.М. (1989). «Испытание стабильности лекарственных средств методом высокочувствительной изотермической калориметрии при 25°С: цефалоспорины в состоянии твердого и водного раствора». Инт Джей Фармакол . 50 (3): 233–252. дои : 10.1016/0378-5173(89)90127-0 .
- ^ Хансен, LD; Ито, диджей; Льюис, Э.А.; Бергстрем, Р.Г.; Деграфт-Джонсон, Д; Кэссиди-Томпсон, К. (1990). «Прогнозирование срока годности на основе калориметрических измерений индукционного периода материалов, подвергающихся автокаталитическому разложению» . Канадский химический журнал . 68 (11): 2111–2114. дои : 10.1139/v90-321 .
- ^ Кенигбауэр, MJ; Брукс С.Х.; Рулло Дж; Диван РА (1992). «Испытание стабильности лекарственных средств в твердом состоянии методом изотермической калориметрии». Фармацевтические исследования . 9 (7): 933–44. дои : 10.1023/а:1015865319250 . ПМИД 1438010 . S2CID 12884493 .
- ^ Вивода, М; Роскар, Р; Кметек, В. (2011). «Разработка экспресс-метода определения аморфности методом изотермической микрокалориметрии». J Therm Анальный Калорим . 105 (3): 1023–1030. дои : 10.1007/s10973-011-1443-7 . S2CID 95028157 .
- ^ Чен, младший; Ву, Ш; Лин, С.Ю.; Хоу, HY; Шу, CM (2008). «Использование микрокалориметрии для оценки возможности неконтролируемого разложения гидропероксида кумола при низких температурах». J Therm Анальный Калорим . 93 (1): 127–133. дои : 10.1007/s10973-007-8834-9 . S2CID 96305303 .
- ^ Монти, М. (1990). «Применение микрокалориметрии для изучения живых клеток в области медицины». Термохимика Акта . 172 : 53–60. Бибкод : 1990TcAc..172...53M . дои : 10.1016/0040-6031(90)80558-г .
- ^ Муриганде, К; Регенасс С; Вирц Д; Дэниэлс АУ; Тиндалл А. (2009). «Сравнение включения (3H)-тимидина и изотермической микрокалориметрии для оценки антиген-индуцированной пролиферации лимфоцитов». Иммунологические исследования . 38 (1): 67–75. дои : 10.1080/08820130802572160 . ПМИД 19172486 . S2CID 38795681 .
- ^ Санторо, Р; Брейссан О; Мюллер Б; Вирц Д; Дэниэлс АУ; Мартин I; Вендт Д. (2011). «Измерения выработки тепла хондроцитами человека в режиме реального времени во время пролиферации in vitro». Биотехнология и биоинженерия . 108 (12): 3019–24. дои : 10.1002/бит.23268 . ПМИД 21769860 . S2CID 19299843 .
- ^ Шарлебуа, SJ; Дэниэлс АУ; Смит Р.А. (2002). «Метаболическое теплопродуцирование как мера реакции макрофагов на частицы из материалов ортопедических имплантатов». Журнал исследований биомедицинских материалов . 59 (1): 166–175. дои : 10.1002/jbm.1230 . ПМИД 11745550 .
- ^ Бэкман, П. (1990). «Влияние экспериментальных факторов на скорость метаболизма клеток Т-лимфомы, измеренную с помощью микрокалориметрии». Термохимика Акта . 172 (1): 123–130. Бибкод : 1990TcAc..172..123B . дои : 10.1016/0040-6031(90)80566-h .
- ^ Каллерхофф, М; Карнебоген М; Певица Д; Деттенбах А; Гралхер У; Рингерт Р.Х. (1996). «Микрокалориметрические измерения, проведенные на изолированных образцах опухолевых и неопухолевых тканей органов урогенитального тракта в сравнении с гистологическими и импульсно-цитофотометрическими исследованиями». Урологические исследования . 24 (2): 83–91. дои : 10.1007/bf00431084 . ПМИД 8740977 . S2CID 35744559 .
- ^ Анкерст, Дж; Шегрен, ХО; Фельдт, Р. (1986). «Использование микрокалориметрии для анализа кинетики ADCC». Журнал методов иммунологических исследований . 88 (2): 259–264. дои : 10.1016/0022-1759(86)90014-1 . ПМИД 3958501 .
- ^ Торен, SA (1992). «Калориметрия: новый количественный метод in vitro в клеточной токсикологии. Исследование дозы / эффекта альвеолярных макрофагов, подвергшихся воздействию частиц». J Токсикол Здоровье окружающей среды . 36 (4): 307–18. Бибкод : 1992JTEHA..36..307T . дои : 10.1080/15287399209531641 . ПМИД 1507265 .
- ^ Лю, В.; Часпул, Ф.; Берж Лефранк, Д.; Декоме, Л.; Галлис, П. (12 июля 2007 г.). «Микрокалориметрия как инструмент оценки токсичности Cr (VI) фибробластов кожи человека». Журнал термического анализа и калориметрии . 89 (1): 21–24. дои : 10.1007/s10973-006-7918-2 . S2CID 96774590 .
- ^ Се, Ю; Депьер Дж.В.; Нэссбергер Л.Н. (2000). «Биосовместимость микропланшетов для культивирования эпителиальных клеток почек, оцененная микрокалориметрическим методом». Журнал материаловедения: Материалы в медицине . 11 (9): 587–591. дои : 10.1023/А:1008984304821 . ПМИД 15348389 . S2CID 25818381 .
- ^ Дустмохаммади, А; Монши А; Фатхи М.Х.; Карбаси С; Брейссан О; Дэниелс АУ (2011). «Прямая оценка цитотоксичности биоактивного стекла 63S и частиц гидроксиапатита костного происхождения с использованием дрожжевой модели и клеток хондроцитов человека методом микрокалориметрии». Журнал материаловедения: Материалы в медицине . 22 (10): 2293–2300. дои : 10.1007/s10856-011-4400-x . ПМИД 21786131 . S2CID 25271308 .
- ^ Джесперсен, Северная Дакота (1982). Биохимические и клинические применения термометрического и термического анализа . Том. 12. Эльзевир. ISBN 0-444-42062-2 . OCLC 8171558 .
- ^ Хэн, З.; Конги, З.; Кунсин, В.; Джибин, В.; Чаоцзян, Г.; Цзе, Л.; Ювен, Л. (январь 2005 г.). «Микрокалориметрическое исследование вирусной инфекции. Влияние гипертермии и рекомбинантного гомо-интерферона 1b на процесс заражения клеток BHK-21 вирусом ящура». Журнал термического анализа и калориметрии . 79 (1): 45–50. дои : 10.1007/s10973-004-0560-y . S2CID 98578017 .
- ^ Анточе, ОА; Антоси, В; Такахаши, К; Помохачи, Н; Намолосану, Я (1997). «Калориметрическое определение ингибирующего действия н-спиртов С1-С4 на рост некоторых видов дрожжей». Термохимика Акта . 297 (1–2): 33–42. Бибкод : 1997TcAc..297...33A . дои : 10.1016/s0040-6031(97)00162-7 .
- ^ Jump up to: а б Брейссан, О.; Вирц, Д.; Гопферт, Б.; Дэниэлс, Австралия (2010). «Использование изотермической микрокалориметрии для мониторинга активности микроорганизмов» . ФЭМС Микробиол. Летт . 303 (1): 1–8. дои : 10.1111/j.1574-6968.2009.01819.x . ПМИД 19895644 .
- ^ Трампуз, А; Зальцманн С; Антом Ж; Дэниэлс АУ (2007). «Микрокалориметрия: новый метод обнаружения микробного загрязнения тромбоцитарной продукции». Переливание . 47 (9): 1643–50. дои : 10.1111/j.1537-2995.2007.01336.x . ПМИД 17725729 . S2CID 21221691 .
- ^ Бонкат, Г; Брейссан О; Видмер А.Ф.; Фрей Р; Рикен М; Уайлер С; Гассер ТЦ; Вирц Д; Дэниелс AU; Бахманн А (2011). «Экспресс-выявление возбудителей мочевыводящих путей методом микрокалориметрии: принцип, методика и первые результаты» . Британский журнал международной урологии . 110 (6): 892–7. дои : 10.1111/j.1464-410X.2011.10902.x . ПМИД 22313675 . S2CID 34620719 .
- ^ Брейссан, О; Вирц Д; Гопферт Б; Дэниэлс АУ (2010). «Наступает жара: быстрое микрокалориметрическое обнаружение микобактерий в культуре». Туберкулез (Эдинб) . 90 (1): 57–59. дои : 10.1016/j.tube.2009.11.001 . ПМИД 19969505 .
- ^ Родригес, Д; Дэниэлс АУ; Уррусти Дж.Л.; Вирц Д; Брейссан О (октябрь 2011 г.). «Оценка недорогого калориметрического подхода для быстрого обнаружения туберкулеза и других микобактерий в культуре» . Журнал прикладной микробиологии . 111 (4): 1016–24. дои : 10.1111/j.1365-2672.2011.05117.x . ПМИД 21797951 . S2CID 205324227 .
- ^ Jump up to: а б Брейссан, О; Бонкат, Г; Вирц, Д. (2013). «Микробный рост и изотермическая микрокалориметрия: модели роста и их применение к микрокалориметрическим данным». Термохимика Акта . 555 : 64–71. Бибкод : 2013TcAc..555...64B . дои : 10.1016/j.tca.2012.12.005 .
- ^ фон Ах, У; Вирц Д; Дэниэлс АУ (2009). «Изотермическая микрокалориметрия — новый метод определения МПК: результаты для 12 антибиотиков и эталонных штаммов E. coli и S. aureus» . БМК Микробиол . 9 (1): 106. дои : 10.1186/1471-2180-9-106 . ПМЦ 2692853 . ПМИД 19470161 .
- ^ фон Ах, У; Вирц Д; Дэниелс АУ (2008). «Быстрая дифференциация метициллин-чувствительного Staphylococcus aureus от метициллин-резистентного S. aureus и определение МИК с помощью изотермической микрокалориметрии» . J Clin Микробиол . 46 (6): 2083–7. дои : 10.1128/JCM.00611-08 . ПМЦ 2446841 . ПМИД 18417657 .
- ^ Бальдони, Д; Герман Х; Фрей Р; Трампуз А; Штайнхубер А (2009). «Проведение микрокалориметрии для раннего выявления резистентности к метициллину у клинических изолятов золотистого стафилококка» . J Clin Микробиол . 47 (3): 774–776. дои : 10.1128/JCM.02374-08 . ПМК 2650961 . ПМИД 19158262 .
- ^ Астасов-Фрауэнхоффер, М; Брейссан О; Хаузер-Герспах I; Дэниэлс АУ; Вирц Д; Вайгер Р; Уолтимо Т. (2011). «Количественное определение жизнеспособных адгезивных клеток Streptococcus sanguinis на покрытом белком титане после дезинфицирующей обработки» (PDF) . Журнал материаловедения: Материалы в медицине . 22 (9): 2045–51. дои : 10.1007/s10856-011-4377-5 . ПМИД 21670995 . S2CID 11255313 .
- ^ Хаузер-Герспах, я; Скандиуччи де Фрейтас П; Дэниэлс АУ; Мейер Дж (2008). «Адгезия Streptococcus sanguinis к стеклянным поверхностям, измеренная методом изотермической микрокалориметрии (IMC)». J Biomed Mater Res B. 85 (1): 42–9. дои : 10.1002/jbm.b.30914 . ПМИД 17696148 .
- ^ Шён, Вадсё I (1988). «Потенциальное использование микрокалориметрии в прогностических тестах действия противоопухолевых препаратов на клетки млекопитающих». Цитобиос . 55 (220): 33–39. ПМИД 3265371 .
- ^ Лампрехт, я; Беккер, В. (1988). «Сочетание калориметрии и эндоскопии для мониторинга двигательной активности мелких животных». Термохимика Акта . 130 : 87–93. Бибкод : 1988TcAc..130...87L . дои : 10.1016/0040-6031(88)87053-9 .
- ^ Харак, М; Лампрехт, я; Куузик, А (1996). «Метаболические затраты на дыхательные движения куколок Tenebrio molitor и Galleria mellonella, изученные методом прямой калориметрии». Термохимика Акта . 276 : 41–47. Бибкод : 1996TcAc..276...41H . дои : 10.1016/0040-6031(95)02750-5 .
- ^ Куузик, А; Харак, М; Хийесаар, К; Мецпалу, Л; Тартес, У (1995). «Исследования регулирования роста насекомых (IGR) и токсического воздействия экстрактов Ledum palustre на куколок Tenebrio molitor (Coleoptera, Tenebrionidae) с использованием калориметрических записей». Термохимика Акта . 251 : 247–253. Бибкод : 1995TcAc..251..247K . дои : 10.1016/0040-6031(94)02048-с .
- ^ Брэкман, Б.П.; Хаутхофд К; Де Врез А; Ванфлетерен-младший (2002). «Анализ метаболической активности стареющего Caenorhabditis elegans». Механизмы старения и развития . 123 (2002): 105–119. дои : 10.1016/S0047-6374(01)00331-1 . ПМИД 11718805 . S2CID 26024344 .
- ^ Маннек, Т; Брейссан О; Эллис В; Кейзер Дж (2011). «Schistosoma mansoni: антишистосомальная активность четырех оптических изомеров и двух рацематов мефлохина на шистосомулах и взрослых червях in vitro и in vivo». Экспериментальная паразитология . 127 (1): 260–9. дои : 10.1016/j.exppara.2010.08.011 . ПМИД 20732321 .
- ^ Кирххофер, К; Варгас М; Брейссан О; Донг Ю; Ван Х; Веннерстрем Дж.Л.; Кейзер Дж (2011). «Активность аналогов OZ78 против Fasciola hepatica и Echinostoma caproni» . Акта Тропика . 118 (1): 56–62. doi : 10.1016/j.actatropica.2011.02.003 . ПМК 3066657 . ПМИД 21316331 .
- ^ Хансен, LD; Льюис, Э.А.; Ито, диджей; Фаулер, ДП; Криддл, RS (1989). «Прогнозирование долгосрочных темпов роста клонов лиственницы путем калориметрического измерения скорости метаболического тепла». Канадский журнал лесных исследований . 19 (5): 606–611. дои : 10.1139/x89-095 .
- ^ Браво, Д; Брейссан О; Солохина А; Клерк М; Дэниэлс АУ; Верреккья Э; Джунье П. (2011). «Использование изотермического микрокалориметрического анализа для характеристики микробной оксалотрофной активности» . ФЭМС Микробиология Экология . 78 (2): 266–74. Бибкод : 2011FEMME..78..266B . дои : 10.1111/j.1574-6941.2011.01158.x . ПМИД 21696406 .
- ^ Брейссан О., Биндшедлер С., Дэниэлс А.У., Верреккья Э.П., Кайо Г. (апрель 2012 г.). «Микробиологическая активность лунного молока контролируется с помощью изотермической микрокалориметрии (пещера Вершез-ле-Брандт, Невшатель, Швейцария)» (PDF) . Журнал исследований пещер и карста . 74 (1): 116–126. дои : 10.4311/2011JCKS0213 .
- ^ Харрис, Дж.А.; Ритц, К; Кушени, Э; Грайс, С.М.; Лерх, ТЗ; Паулетт, М; Херрманн, AM (2012). «Термодинамическая эффективность почвенных микробных сообществ, подверженных длительному стрессу, ниже, чем при обычных режимах внесения». Биология и биохимия почвы . 47 : 149–157. Бибкод : 2012SBiBi..47..149H . doi : 10.1016/j.soilbio.2011.12.017 .
- ^ Вадсё, Л; Гомес Галиндо, форвард (2009). «Изотермическая калориметрия для биологических применений в пищевой науке и технологиях» . Пищевой контроль . 20 (10): 956–961. doi : 10.1016/j.foodcont.2008.11.008 . S2CID 73702189 .
- ^ Гомес Галиндо, нападающий; Роккули, П; Вадсё, Л; Сьёхольм, я (2005). «Потенциал изотермической калориметрии в мониторинге и прогнозировании изменений качества при переработке и хранении минимально обработанных фруктов и овощей». Тенденции пищевых наук и технологий . 16 (8): 325–331. дои : 10.1016/j.tifs.2005.01.008 .
- ^ Анастази, Г; Антонелли МЛ; Бионди Б; Винчи Дж. (2000). «Оротовая кислота: компонент молока. Ферментативное определение с помощью нового микрокалориметрического метода». Таланта . 52 (5): 947–952. дои : 10.1016/S0039-9140(00)00433-1 . ПМИД 18968055 .
- ^ Антонелли, ML; Спадаро С; Торнелли РФ (2008). «Микрокалориметрический датчик для пищевого и косметического анализа: определение L-яблочной кислоты». Таланта . 74 (5): 1450–4. дои : 10.1016/j.talanta.2007.09.035 . ПМИД 18371803 .
- ^ Роккули, П; Гомес Галиндо, нападающий; Мендозак, Ф; Вадсё, Л; Романи, С; Далла Роза, М; Сьёхольм, я (2007). «Влияние применения веществ, препятствующих потемнению, на метаболическую активность и сахарный состав свеженарезанного картофеля». Послеуборочная биология и технология . 43 : 151–157. doi : 10.1016/j.postharvbio.2006.08.002 .
- ^ Дымек К., Деймек П., Панарезе В., Висенте А.А., Вадсё Л., Финни С., Галиндо Ф.Г. (июнь 2012 г.). «Влияние импульсного электрического поля на прорастание семян ячменя». LWT – Пищевая наука и технология . 47 (1): 161–6. дои : 10.1016/j.lwt.2011.12.019 . hdl : 1822/22504 .
Внешние ссылки
[ редактировать ]- Некоторые источники инструментов, аксессуаров, расходных материалов и программного обеспечения IMC
- Калметрикс
- ТА Инструменты
- сетарам
- Симсел
- Конфигурации приборов проточно-адсорбционного микрокалориметра Microscal Ltd (архив 2005 г.)