Дэниел ячейка

Ячейка Даниэля — тип электрохимической ячейки, изобретенной в 1836 году Джоном Фредериком Дэниелом , британским химиком и метеорологом , и состоит из медного горшка, наполненного раствором сульфата меди (II) , в который погружен неглазурованный глиняный сосуд, наполненный серной кислотой. кислота и цинковый электрод. Он искал способ устранить проблему с пузырьками водорода, обнаруженную в гальванической батарее , и его решение заключалось в использовании второго электролита для потребления водорода, вырабатываемого первым. сульфатом цинка Серную кислоту можно заменить . Элемент Даниэля представлял собой значительное улучшение по сравнению с существующей технологией, использовавшейся на заре разработки аккумуляторов . Более поздний вариант ячейки Даниэля, названный гравитационной ячейкой или ячейкой «гусиной лапки», был изобретен в 1860-х годах французом по имени Калло и стал популярным выбором для электрической телеграфии .
Ячейка Даниэля также является исторической основой современного определения вольта , который является единицей электродвижущей силы в Международной системе единиц . Определения электрических единиц, предложенные на Международной конференции электриков 1881 года , были разработаны таким образом, что электродвижущая сила элемента Даниэля составляла около 1,0 вольт. [1] [2] Согласно современным определениям, стандартный потенциал ячейки Даниэля при 25 °C (77 °F) на самом деле составляет 1,10 В. [3]
Химия
[ редактировать ]В ячейке Даниэля медный и цинковый электроды погружены в раствор сульфата меди (II) и сульфата цинка соответственно.

На аноде (отрицательном электроде) цинк окисляется по следующей полуреакции:
- Зн
(s) → Zn 2+
(вод) + 2е − . . ( Стандартный потенциал восстановления электрода -0,7618 В) [4] [5]
На катоде (положительном электроде) медь восстанавливается по следующей реакции:
- С 2+
(вод) + 2е − → С
(с) . . ( Стандартный восстановительный потенциал электрода +0,340 В)
Обратите внимание, что положительно заряженные ионы меди движутся к положительному электроду за счет уменьшения химической энергии.
Суммарная реакция:
- Зн
(ы) + Cu 2+
(вод) → Zn 2+
(aq) + Cu
(с) . . ( Напряжение холостого хода 1,1018 В)
Эти процессы приводят к накоплению твердой меди на катоде и коррозии цинкового электрода в раствор в виде катионов цинка.

В демонстрациях в классе часто используется форма ячейки Даниэля, известная как две полуячейки, из-за ее простоты. Каждая из двух полуэлементов поддерживает половину реакций, описанных выше. проводом . и лампочкой Два электрода можно соединить Избыточные электроны, образующиеся при окислении металлического цинка, «выталкиваются» из анода, который, следовательно, является отрицательным электродом, проходят через провод и «втягиваются» в медный катод, где они поглощаются за счет восстановления ионов меди. Это обеспечивает электрический ток, который освещает лампочку.
Поскольку ни одна полуреакция не происходит независимо от другой, две полуячейки должны быть соединены таким образом, чтобы ионы могли свободно перемещаться между ними. барьер Для разделения двух растворов можно использовать пористый или керамический диск, обеспечивая при этом поток сульфат-ионов. Когда полуячейки помещаются в два совершенно разных и отдельных контейнера, солевой мостик для соединения двух ячеек часто используется . Солевой мостик обычно содержит высокую концентрацию нитрата калия (соли, которая не оказывает химического влияния на реакцию ни в одной из полуэлементов). В вышеупомянутой влажной камере во время разрядки нитрат-анионы в солевом мостике перемещаются в цинковую полуячейку, чтобы сбалансировать увеличение Zn. 2+
ионы. В то же время ионы калия из солевого мостика переходят в медную полуячейку, чтобы заменить Cu 2+
ионы осаждаются на медный электрод.
Если элемент подключен к источнику потенциала (например, зарядному устройству), так что разность потенциалов источника немного выше, чем ЭДС элемента (1,1 В), тогда ток может быть изменен на противоположное, и реакция будет такой:
- Зн 2+
(вод) + 2е − → Цинк
(с) - С
(ы) → Cu 2+
(вод) + 2е −
или,
- Зн 2+
(aq) + Cu
(s) → Zn
(ы) + Cu 2+
(вода)
Следовательно, ячейка Даниэля является обратимой, если ток, потребляемый из нее (или подаваемый в нее), мал. Ячейку Даниэля можно использовать для «генерации» электроэнергии путем потребления электрода или для хранения электроэнергии.
Разработка
[ редактировать ]Оригинальная конструкция Дэниела
[ редактировать ]
Дэниел впервые построил свою камеру в 1836 году. [6] Его первоначальная конструкция представляла собой медный цилиндр диаметром 3,5 дюйма. Поперёк утопленного сверху цилиндра располагался медный диск, продырявленный многочисленными отверстиями. Трубка из бычьего пищевода свисала с большого отверстия в центре перфорированного медного диска. Внутри этой трубки из бычьего пищевода, подвешенной на деревянных опорах, висел цинковый стержень диаметром 0,5 дюйма. Медный сосуд заполняли раствором серной кислоты , насыщенным сульфатом меди, до уровня выше уровня перфорированного диска. Бычье пищеводную трубку заполняли раствором серной кислоты. Кристаллы медного купороса складывались на перфорированный медный диск, чтобы раствор оставался насыщенным. Бычий пищевод действует как пористая мембрана, позволяющая проходить ионам. Дэниел утверждает, что для удобства вместо бычьего пищевода можно использовать пористую глиняную трубку, но такое устройство будет производить меньшую мощность. Еще одно предложение Дэниела по улучшению элемента заключалось в замене меди платиной, а сульфата меди - хлоридом платины. , но он отмечает, что «такое устройство было бы идеальным, но слишком дорогостоящим для обычных приложений». [7] Именно пористая форма ячейки стала широко использоваться в телеграфии.
Пористая ячейка горшка
[ редактировать ]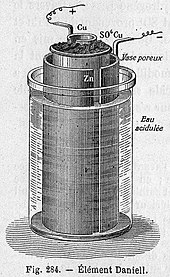
Пористая ячейка горшка состоит из центрального цинкового анода, погруженного в пористый глиняный горшок, содержащий раствор сульфата цинка. Пористый горшок, в свою очередь, погружается в раствор медного купороса, находящийся в медной банке. [ нужны разъяснения ] который действует как катод ячейки. Использование пористого барьера позволяет ионам проходить сквозь него, но предотвращает смешивание растворов. Без этого барьера, когда ток не подается, ионы меди будут дрейфовать к цинковому аноду и восстанавливаться без образования тока, что сократит срок службы батареи. [8] Замена серной кислоты сульфатом цинка была изобретением Дж. Ф. Фуллера в 1853 г. Оно продлевает жизнь клетки. [9]
Со временем накопление меди закупорит поры глиняного барьера и сократит срок службы батареи. Тем не менее, элемент Даниэля обеспечивает более длительный и более надежный ток, чем Вольтов столб, потому что электролит откладывает на медь, которая является проводником , а не водород, который является изолятором катоде . Это также более безопасно и менее коррозионно. При рабочем напряжении примерно 1,1 вольт он широко использовался в телеграфных сетях, пока его не вытеснил элемент Лекланше . в конце 1860-х годов [10]
Гравитационная ячейка
[ редактировать ]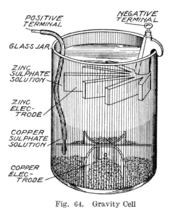
Где-то в 1860-х годах француз по имени Калло изобрел вариант ячейки Даниэля, в котором не использовался пористый барьер. [10] Вместо этого слой сульфата цинка находится поверх слоя сульфата меди. Две жидкости разделяются из-за их разной плотности, часто сверху добавляется слой масла для предотвращения испарения. Это уменьшает внутреннее сопротивление системы и, таким образом, батарея выдает более сильный ток.
Этот вариант, называемый гравитационной ячейкой, состоит из стеклянной банки, в которой на дне находится медный катод, а под краем в слое сульфата цинка подвешен цинковый анод. Кристаллы медного купороса рассыпаются вокруг катода, а затем сосуд наполняется дистиллированной водой. При подаче тока вверху вокруг анода образуется слой раствора сульфата цинка. Этот верхний слой отделен от нижнего слоя сульфата меди из-за его более низкой плотности и полярности ячейки. Недостатком гравитационной ячейки является то, что необходимо постоянно создавать ток, чтобы предотвратить смешивание двух растворов путем диффузии, поэтому она непригодна для периодического использования. Кроме того, он был уязвим для потери целостности, если слишком большой электрический ток подается , что также приводит к перемешиванию слоев.
Эта конструкция, которую иногда называют элементом «гусиная лапка» из-за отличительной формы электродов, является менее дорогостоящей для больших многоэлементных батарей и быстро стала предпочтительной батареей для американских и британских телеграфных сетей. Даже после того, как большинство телеграфных линий начали питаться от мотор-генераторов, гравитационная батарея продолжала использоваться на промежуточных станциях для питания местной сети, по крайней мере, до 1950-х годов. [11] В телеграфной промышленности эту батарею часто собирали на месте сами телеграфисты, а когда она разряжалась, ее можно было обновить путем замены израсходованных комплектующих. [12] Слой сульфата цинка бесцветен, в отличие от темно-синего слоя сульфата меди, что позволяет технику с первого взгляда определить срок службы батареи. С другой стороны, такая установка означает, что батарею можно использовать только в стационарном приборе, иначе растворы смешаются или прольются.
Использование в электрометаллургии
[ редактировать ]Птичья клетка
[ редактировать ]Вариант клетки Даниэля был изобретен в 1837 году больницы Гая врачом Голдингом Бердом , который использовал гипсовый барьер, чтобы разделить растворы. Эксперименты Берда с этой ячейкой имели определенное значение для новой дисциплины электрометаллургии , но сам Берд не занимался этой областью; его интересом была электротерапия . Неожиданным результатом экспериментов Берда стало осаждение меди на пористом гипсе и в проходящих через него венах без какого-либо контакта с металлическими электродами. Настолько удивительно, что поначалу в это не поверили исследователи-электрохимики, включая Майкла Фарадея . Самому Бёрду пришлось тщательно осмотреть свой аппарат на предмет случайного контакта, возможно, из-за роста медных «усов», прежде чем он убедился в результате. Отложение меди и других металлов отмечалось и раньше, но раньше всегда это было металл на металлическом электроде. [13] [14]
электротипирование
[ редактировать ]Джон Дэнсер , ливерпульский производитель инструментов, в 1838 году первым воспользовался коммерческими преимуществами уникальных особенностей ячейки Даниэля для меднения. С помощью процесса, который теперь известен как электротипирование, он обнаружил, что может придавать объектам любую желаемую форму, используя пористый барьер в качестве формы. Однако многие другие сделали то же открытие, и в патентном споре с Томасом Спенсером было указано, что Берд имеет приоритет в отношении этого принципа. Заслугу изобретения электротипирования обычно приписывают русскому Морицу фон Якоби . [13]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Борвон, Жерар (10 сентября 2012 г.). «История электрических агрегатов» . Ассоциация С-ЕАУ-С.
- ^ Хамер, Уолтер Дж. (15 января 1965 г.). Стандартные элементы: их конструкция, обслуживание и характеристики (PDF) . Монография Национального бюро стандартов № 84. Национальное бюро стандартов США.
- ^ Спенсер, Джеймс Н.; Боднер, Джордж М.; Рикард, Лайман Х. (2010). Химия: структура и динамика (Пятое изд.). Джон Уайли и сыновья. п. 564. ИСБН 9780470587119 .
- ^ Майкл Клагстон, Розалинд Флемминг, Продвинутая химия , стр. 224, Издательство Оксфордского университета, 2000 г. ISBN 0199146330 .
- ^ Национальное бюро стандартов, цинк и его сплавы , стр. 40 , Типография правительства США, 1931 г. OCLC 954241601 .
- ^ Элизабет Х. Оукс, от А до Я ученых STS , с. 72, Издательство «Информационная база», 2009 г. ISBN 1438109253 .
- ^ Джон Фредерик Дэниел, Введение в изучение химической философии , стр. 504–505, Джон В. Паркер, 1843 г. OCLC 315534231 (стр. 438–439 в издании 1839 г.) OCLC 7841489 , в котором нет комментариев о платине).
- ^ Джорджио Карбони, Эксперименты по электрохимии ; Последний доступ: 30 июля 2010 г.
- ^ Томас Кингстон Дерри, Тревор Илтид Уильямс, Краткая история технологий с древнейших времен до 1900 года нашей эры , стр. 611, Курьерская корпорация, 1960 г. ISBN 9780486274720 .
- ^ Jump up to: а б Джеймс Б. Калверт. «Электромагнитный телеграф» . Архивировано из оригинала 4 августа 2007 г. Проверено 30 июля 2010 г.
- ^ Инструменты телеграфии. Архивировано 23 июля 2011 г. в Wayback Machine , Telegraph Lore; Последний доступ: 30 июля 2010 г.
- ^ Грегори С. Рэйвен, Воспоминания об узкоколейном пращнике для молний. Архивировано 23 июля 2011 г. в Wayback Machine ; Последний доступ: 30 июля 2010 г.
- ^ Jump up to: а б Ватт, Александр; Филип, Арнольд (2005). Гальваника и электрорафинирование металлов . Издательство часовщика. стр. 90–92. ISBN 1929148453 . Перепечатка тома 1889 года.
- ^ Голдинг Берд, Отчет седьмого собрания Британского общества содействия развитию науки , том 6 (1837), стр. 45, Лондон: Дж. Мюррей, 1838.
Дальнейшее чтение
[ редактировать ]- Саслоу, Уэйн М. (1999), «Гальванические элементы для физиков: два поверхностных насоса и внутреннее сопротивление», American Journal of Physics , 67 (7): 574–583, Bibcode : 1999AmJPh..67..574S , doi : 10.1119/1.19327
- Лестер, Джеймс С.; Викари, Роза Мария; Парагуасу, Фабио (2004), Лестер, Джеймс С.; Викари, Роза Мария; Парагуасу, Фабио (ред.), Качественная модель ячейки Даниэля для химического образования , Конспекты лекций по информатике, том. 3220, doi : 10.1007/b100137 , hdl : 10092/340 , ISBN 978-3-540-22948-3 , S2CID 24433795
