Палладий на углероде

| |
| Имена | |
|---|---|
| Другие имена
Palladium on Carbon, PD/C, PD-C
| |
| Идентификаторы | |
| Характеристики | |
| Появление | Черный порошок |
| Растворимость | Аква направление |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
Палладий на углероде , часто называемый PD/C , является формой палладия , используемой в качестве катализатора . [ 1 ] Металл поддерживается на активированном углероде, чтобы максимизировать площадь и активность поверхности .
Использование
[ редактировать ]Гидрирование
[ редактировать ]Палладий на углероде используется для каталитических гидрирований при органическом синтезе . Примеры включают восстановительное амирование , [ 2 ] сокращение карбонила , нитро -составное сокращение , [ 3 ] [ 4 ] сокращение баз иминов и Шиффа [ 1 ] и реакции деформации.
Гидрогенолиз
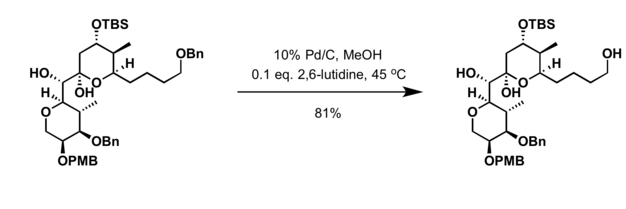
[ редактировать ]Палладий на углероде является распространенным катализатором для гидрогенолиза . Такие реакции полезны в стратегиях снятия защиты. Особенно распространенными субстратами для гидрогенолиза являются бензиловые эфиры : [ 5 ]
Другие лабильные заместители также подвержены расщеплению этим реагентом. [ 6 ]
Реакции связи
[ редактировать ]Палладий на углероде также используется для реакций связи . Примеры включают реакцию Suzuki и реакцию Stille . [ 7 ]
Подготовка
[ редактировать ]Раствор хлорида палладия и соляной кислоты объединяется с водной суспензией активированного углерода . Палладий (II) затем уменьшается за счет добавления формальдегида. [ 8 ] Нагрузка на палладие обычно составляет от 5% до 10%. Часто смесь катализатора хранится влажной.
Смотрите также
[ редактировать ]- Палладий черный
- Платина на углероде
- Платиновый диоксид
- Родий-платиновый оксид
- Линдлрар Катализатор
- Рэни Никель
- Хикель никель
Ссылки
[ редактировать ]- ^ Подпрыгнуть до: а беременный Nishimura, Shigeo (2001). Справочник по гетерогенному каталитическому гидрированию для органического синтеза (1 -е изд.). Нью-Йорк: Wiley-Interscience. С. 34–38. ISBN 9780471396987 .
- ^ Романелли, Майкл Г.; Беккер, Эрнест И. (1967). «Этилп-диметиламинофенилацетат». Органические синтезы . 47 : 69. doi : 10.15227/orgsyn.047.0069 .
- ^ Смит, Майкл Б.; Март, Джерри (2007). Продвинутая органическая химия марта (6 -е изд.). Джон Уайли и сыновья. п. 1816. ISBN 978-0-471-72091-1 .
- ^ Рам, Сия; Ehrenkaufer, Richard E. (1984). «Общая процедура легкого и быстрого восстановления алифатических и ароматических нитро -соединений с использованием формиата аммония в качестве агента каталитического переноса водорода». Тетраэдр буквы . 25 (32): 3415–3418. doi : 10.1016/s0040-4039 (01) 91034-2 . HDL : 2027.42/25034 .
- ^ Смит, Амос Б.; Чжу, Вениу; Шираками, Шохей; Сфугатакис, Крис; Даути, Виктория А.; Беннетт, Клэй С.; Сакамото, Ясухару (2003-03-01). «Полный синтез (+)-губчататин 1. Эффективная конструкция второго поколения усовершенствованной соли EF Wittig, фрагментного союза и окончательной разработки». Органические буквы . 5 (5): 761–764. doi : 10.1021/ol034037a . ISSN 1523-7060 . PMID 12605509 .
- ^ Муслин, Уолтер Дж.; Гейтс, младший, Джон В. (1971). «Дегидроксилирование фенолов; гидрогенолиз фенольных эфиров: бифенил». Органические синтезы . 51 : 82. doi : 10.15227/orgsyn.051.0082 .
- ^ Liebeskind, Lanny S.; Peña-Cabrera, Eduardo (2000). «Стильные муфты, катализируемые палладием на углероде с CUI в качестве коатализатора: синтез 2- (4'-ацетилхенил) тиофена». Органические синтезы . 77 : 138. doi : 10.15227/orgsyn.077.0135 .
- ^ Мозинго, Ральф (1946). «Палладийские катализаторы». Органические синтезы . 26 : 77–82. doi : 10.15227/orgsyn.026.0077 . PMID 20280763 .