Летальный аллель
Летальные аллели (также называемые летальными или летальными ) — это аллели , которые вызывают смерть организма, который их несет. Обычно они являются результатом мутаций в генах, которые необходимы для роста и развития. [1] Летальные аллели могут быть рецессивными, доминантными или условными в зависимости от задействованного гена или генов.
Летальные аллели могут быть летальными на эмбриональном этапе, при которых плод никогда не доживет до срока, или могут быть летальными перинатально или постнатально после длительного периода очевидно нормального развития. Эмбрионально летальные аллели являются причиной неменделевских закономерностей наследования, например, наблюдения признаков в соотношении 2:1.
История
[ редактировать ]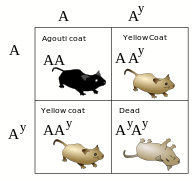
Летальные аллели были впервые обнаружены Люсьеном Куэно в 1905 году при изучении наследования окраски шерсти у мышей. Ген агути у мышей в значительной степени отвечает за определение цвета шерсти. Аллель дикого типа вызывает смесь желтой и черной пигментации в каждом волоске мыши. Эту смесь желтого и черного цветов можно назвать «агути». [3] Один из мутантных аллелей гена агути приводит к появлению мышей с гораздо более светлой желтоватой окраской. Когда этих желтых мышей скрещивали с гомозиготными мышами дикого типа , получали желтое и темно-серое потомство в соотношении 1:1. Это указывало на то, что мутация желтого цвета является доминантной, и все родительские мыши желтого цвета были гетерозиготными по мутантному аллелю.
Спаривая двух желтых мышей, Куэно ожидал наблюдать обычное менделевское соотношение 1:2:1 между гомозиготными агути, гетерозиготными желтыми и гомозиготными желтыми. Вместо этого он всегда наблюдал соотношение агути и желтых мышей 1:2. Ему не удалось получить мышей, гомозиготных по аллелю желтого агути.
Лишь в 1910 году У. Э. Касл и Си Си Литтл подтвердили работу Куэно, дополнительно продемонстрировав, что четверть потомства умирала во время эмбрионального развития. Это был первый документально подтвержденный пример рецессивного летального аллеля.
Типы летального аллеля
[ редактировать ]Рецессивные летальные исходы
[ редактировать ]Пара идентичных аллелей, которые оба присутствуют в организме и в конечном итоге приводят к гибели этого организма, называются рецессивными летальными аллелями. Хотя рецессивные летальные признаки могут кодировать доминантные или рецессивные признаки, они смертельны только в гомозиготном состоянии.
Гетерозиготы иногда демонстрируют форму болезненного фенотипа, как в случае ахондроплазии . [4] Можно допустить один мутантный летальный аллель, но два варианта приводят к смерти. При гомозиготной ахондроплазии смерть почти всегда наступает до рождения или в перинатальном периоде. Не все гетерозиготы по рецессивным летальным аллелям будут демонстрировать мутантный фенотип , как в случае с носителями муковисцидоза . Если у двух носителей муковисцидоза есть дети, у них есть 25-процентная вероятность произвести на свет потомство с двумя копиями летального аллеля, что в конечном итоге приведет к смерти ребенка. [5] Другим примером являются мутации BRCA; наследование одного дефектного аллеля BRCA приводит к значительному увеличению риска рака молочной железы и рака яичников , тогда как наследование обоих дефектных аллелей приводит к тяжелой форме анемии Фанкони (FA-S для BRCA1, FA-D1 для BRCA2), которая является эмбрионально летальной для большинстве случаев. Выжившие после гомозиготных или биаллельных мутаций BRCA почти никогда не доживают до взрослого возраста. [6] В живых случаях наследование обеих мутаций приводит к серьезному прогнозу, при котором выживание почти никогда не выходит за рамки детства. [7]
Другой пример рецессивного летального аллеля встречается у мэнской кошки . Мэнские кошки обладают гетерозиготной мутацией, приводящей к укорочению или отсутствию хвоста. Скрещивание двух гетерозиготных мэнских кошек приводит к тому, что две трети выживших потомков демонстрируют гетерозиготный фенотип укороченного хвоста, а одна треть выживших потомков имеет нормальную длину хвоста, гомозиготную по нормальному аллелю. Гомозиготное потомство по мутантному аллелю не может пережить рождение и поэтому не встречается при таких скрещиваниях. [8]
Доминирующие летальные исходы
[ редактировать ]Аллели, которые должны присутствовать в организме только в одной копии, чтобы быть фатальными, называются доминантными летальными аллелями. Эти аллели обычно не встречаются в популяциях, поскольку они обычно приводят к гибели организма до того, как он сможет передать свой летальный аллель своему потомству. [4] Примером доминантного летального аллеля у людей является болезнь Хантингтона, редкое нейродегенеративное заболевание, которое в конечном итоге приводит к смерти. Однако из-за позднего начала (т.е. часто после того, как уже произошло размножение) он способен сохраняться в популяциях. У человека проявляется болезнь Хантингтона, когда он несет единственную копию повторяющегося расширенного аллеля Хантингтона на хромосоме 4. [9]
Условные летальные исходы
[ редактировать ]Аллели, которые будут фатальными только в ответ на какой-либо фактор окружающей среды, называются условными летальными. Одним из примеров условно летального исхода является фавизм , наследственное заболевание, сцепленное с полом, которое приводит к развитию гемолитической анемии у носителя при употреблении в пищу бобов фава . [4]
Инфекция клетки-хозяина E. coli бактериофага (фага) Т4, чувствительного к температуре (ts), условно- летальным мутантом при высокой ограничительной температуре приводит к отсутствию продукции жизнеспособного фага. Однако рост таких мутантов все же может происходить при более низкой температуре. Такие условно летальные ts-мутанты использовались для идентификации и характеристики функций многих генов фага. [10] Таким образом, гены, участвующие в репарации повреждений ДНК, были идентифицированы с использованием ts-мутантов. [11] [12] а также гены, влияющие на генетическую рекомбинацию . [13] [14] Например, выращивание мутанта репарации ДНК ts при промежуточной температуре позволит получить некоторое количество фага-потомка. Однако если этот ts-мутант облучить УФ-светом, его выживаемость будет снижена сильнее по сравнению со снижением выживаемости облученного фага Т4 дикого типа. Кроме того, в фаге Т4 были выделены холодочувствительные условно-летальные мутанты, способные расти при высоких температурах, но не способные расти при низких. [15] Эти чувствительные к холоду условно-летальные мутанты также определили набор фаговых генов. Другой класс условно летальных мутантов фага Т4, называемый янтарными мутантами , способен расти на одних штаммах E. coli , но не на других. [10] [16] [17] Эти мутанты были также использованы для первоначальной идентификации и характеристики многих генов фага Т4 , включая гены, кодируемые белки которых участвуют в репарации ДНК , генетической рекомбинации , репликации ДНК и молекулярном морфогенезе . Кроме того, было обнаружено, что янтарная мутация приводит к образованию «нонсенс-кодона» внутри гена, который вызывает обрыв полипептидной цепи во время трансляции . Это открытие дало понимание важного аспекта генетического кода .
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Глюксон-Вельш, Саломея (1963). «Летальные гены и анализ дифференциации». Наука . 142 (3597): 1269–76. Бибкод : 1963Sci...142.1269G . дои : 10.1126/science.142.3597.1269 . ПМИД 14074837 . S2CID 46113268 .
- ^ Информатика о геномах мышей
- ^ Хартвелл, Лиланд; Худ, Лерой; Гольдберг, Майкл; Рейнольдс, Энн; Сильвер, Ли; Карагианнис, Джим; Папаконстантину, Мария (2014). Генетика: от генов к геномам . Канада: МакГроу-Хилл Райерсон. стр. 39–42. ISBN 978-0-07-094669-9 .
- ^ Jump up to: а б с Лобо, Я (2008). «Менделевские соотношения и летальные гены» . Природное образование . 1 (1): 138.
- ^ Ратьен, Феликс; Дёринг, Герд (февраль 2003 г.). "Муковисцидоз". Ланцет . 361 (9358): 681–689. дои : 10.1016/S0140-6736(03)12567-6 . ПМИД 12606185 . S2CID 24879334 .
- ^ Сойер С.Л., Тиан Л., Кахконен М., Шварцентрубер Дж., Кирхер М., Маевски Дж., Даймент Д.А., Иннес А.М., Бойкот К.М., Моро Л.А., Мойланен Дж.С., Гринберг Р.А. (2014). «Биаллельные мутации в BRCA1 вызывают новый подтип анемии Фанкони» . Рак Дисков . 5 (2): 135–42. дои : 10.1158/2159-8290.CD-14-1156 . ПМК 4320660 . ПМИД 25472942 .
- ^ Максвелл, К.Н., Патель, В., Нид, К.Т. и др. (2013). «Анемия Фанкони, вызванная биаллельной инактивацией BRCA2, может проявляться атипичным раковым фенотипом во взрослом возрасте» . Клиническая генетика . 103 (1): 119–124. дои : 10.1111/cge.14231 . ПМЦ 9742260 . ПМИД 36089892 . S2CID 252198281 .
- ^ Робинсон, Р. (1993). «Экспрессивность мэнского гена у кошек». Дж. Херед . 84 (3): 170–2. doi : 10.1093/oxfordjournals.jhered.a111311 . ПМИД 8228170 .
- ^ Роос, Раймунд AC (2010). «Болезнь Хантингтона: клинический обзор» . Сиротский журнал редких заболеваний . 5 (1): 40. дои : 10.1186/1750-1172-5-40 . ПМК 3022767 . ПМИД 21171977 .
- ^ Jump up to: а б Эдгар Р.С., Эпштейн Р.Х. (февраль 1965 г.). «Генетика бактериального вируса». Sci Am . 212 : 70–8. doi : 10.1038/scientificamerican0265-70 . ПМИД 14272117 .
- ^ Болди М.В. (февраль 1970 г.). «Чувствительность к УФ-излучению некоторых чувствительных к температуре мутантов фага Т4 с ранней функцией». Вирусология . 40 (2): 272–87. дои : 10.1016/0042-6822(70)90403-4 . ПМИД 4909413 .
- ^ Болди М.В., Стром Б., Бернштейн Х. (март 1971 г.). «Репарация дезоксирибонуклеиновой кислоты алкилированного бактериофага Т4 по механизму с участием полинуклеотидлигазы» . Дж Вирол . 7 (3): 407–8. doi : 10.1128/JVI.7.3.407-408.1971 . ПМК 356131 . ПМИД 4927528 .
- ^ Бернштейн Х. (август 1967 г.). «Влияние на рекомбинацию мутационных дефектов ДНК-полимеразы и дезоксицитидилатгидроксиметилазы фага Т4Д» . Генетика . 56 (4): 755–69. дои : 10.1093/генетика/56.4.755 . ПМЦ 1211652 . ПМИД 6061665 .
- ^ Бернштейн Х (1968). «Репарация и рекомбинация в фаге Т4. I. Гены, влияющие на рекомбинацию». Холодный источник Harb Symp Quant Biol . 33 : 325–31. дои : 10.1101/sqb.1968.033.01.037 . ПМИД 4891972 .
- ^ Скотти П.Д. (1968). «Новый класс температурных условно-летальных мутантов бактериофага Т4Д». Мутат Рес . 6 (1): 1–14. дои : 10.1016/0027-5107(68)90098-5 . ПМИД 4885498 .
- ^ Эпштейн Р.Х., Болле А., Стейнберг К.М., Шталь Ф.В. (март 2012 г.). «Янтарные мутанты бактериофага T4D: их выделение и генетическая характеристика» . Генетика . 190 (3): 831–40. дои : 10.1534/genetics.112.138438 . ПМК 3296251 . ПМИД 22518878 .
- ^ Эпштейн Р.Х., Болле А., Стейнберг К.М. (март 2012 г.). «Янтарные мутанты бактериофага T4D: их выделение и генетическая характеристика» . Генетика . 190 (3): 833–40. дои : 10.1534/genetics.112.138438 . ПМК 3296251 . ПМИД 22419076 .