Вирус эшерихии Т4

| Вирус эшерихии Т4 | |
|---|---|

| |
| Вирус эшерихии ( ЭМ вириона Т4 ) | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область : | Дуплоднавирия |
| Королевство: | Хынггунвирэ |
| Тип: | Уровироката |
| Сорт: | Каудовирицеты |
| Семья: | Страбовирусиды |
| Род: | Текватровирус |
| Разновидность: | Вирус эшерихии Т4
|
| Штаммы [2] | |
| Синонимы [3] | |
|
Фаг энтеробактерий Т4 | |
Вирус Escherichia T4 представляет собой разновидность бактериофагов , инфицирующих Escherichia coli бактерии . Это вирус с двухцепочечной ДНК подсемейства Tevenvirinae семейства Straboviridae . Т4 способен проходить только литический жизненный цикл , а не лизогенный жизненный цикл . Этот вид ранее назывался Т-четным бактериофагом , это название также включает, среди других штаммов (или изолятов), фаг энтеробактерий Т2 , фаг энтеробактерий Т4 и фаг энтеробактерий Т6 .
Использование в исследованиях
[ редактировать ]Начиная с 1940-х годов и по сей день, Т-четные фаги считаются наиболее изученными модельными организмами. Модельные организмы обычно должны быть простыми и содержать всего пять генов . Тем не менее, Т-четные фаги на самом деле являются одними из самых крупных и сложных вирусов этих фагов , в которых генетическая информация состоит примерно из 300 генов . В соответствии с их сложностью было обнаружено, что Т-четные вирусы имеют необычное основание гидроксиметилцитозин (HMC) вместо основания цитозина нуклеиновой кислоты . [4]
Геном и структура
[ редактировать ]двухцепочечной ДНК Геном около 169 т.п.н. вируса Т4 имеет длину [5] и кодирует 289 белков . Геном Т4 окончательно избыточен . При репликации ДНК образуются конкатемеры длинной мультигеномной длины, возможно, по механизму репликации по катящемуся кругу. [6] При упаковке конкатемер разрезается в неспецифических положениях одинаковой длины, что приводит к образованию нескольких геномов, которые представляют собой круговые перестановки оригинала. [7] Геном Т4 несет эукариоподобные последовательности интронов .
Перевод
[ редактировать ]Последовательность Шайна-Дальгарно GAGG доминирует в ранних генах вируса Т4, тогда как последовательность GGAG является мишенью для эндонуклеазы Т4 RegB, которая инициирует раннюю деградацию мРНК. [8]
Структура вирусных частиц
[ редактировать ]
Т4 — относительно крупный вирус, шириной примерно 90 нм и длиной 200 нм (длина большинства вирусов варьируется от 25 до 200 нм). Геном ДНК содержится в икосаэдрической головке, также известной как капсид . [9] Хвост Т4 полый, поэтому после прикрепления он может передавать свою нуклеиновую кислоту в клетку, которую заражает. Фаги Myoviridae, такие как T4, имеют сложные сократительные структуры хвоста с большим количеством белков, участвующих в сборке и функционировании хвоста. [10] Волокна хвоста также важны для распознавания поверхностных рецепторов клетки-хозяина, поэтому они определяют, находится ли бактерия в пределах диапазона хозяина вируса. [11]
Недавно была описана структура базовой пластинки Т4 массой 6 мегадальтон, которая включает 127 полипептидных цепей 13 различных белков (генные продукты 5, 5.4, 6, 7, 8, 9, 10, 11, 12, 25, 27, 48 и 53). в атомарных деталях. Также создана атомная модель проксимальной области хвостовой трубки, образованной gp54 и белком основной трубки gp19. Белок рулетки gp29 присутствует в комплексах опорная пластинка-хвостовая трубка, но его невозможно смоделировать. [12]
бактериофага (фага) Т4 При сборке вириона морфогенетические белки, кодируемые фаговыми генами, взаимодействуют друг с другом в характерной последовательности. Поддержание соответствующего баланса в количествах каждого из этих белков, вырабатываемых во время вирусной инфекции, по-видимому, имеет решающее значение для нормального морфогенеза фага Т4. [13] Белки, кодируемые фагом Т4, которые определяют структуру вириона, включают основные структурные компоненты, второстепенные структурные компоненты и неструктурные белки, которые катализируют определенные этапы последовательности морфогенеза. [14] Морфогенез фага Т4 разделен на три независимых пути: головной, хвостовой и длинные хвостовые волокна, как подробно описано Япом и Россманом. [15]
Процесс заражения
[ редактировать ]Вирус Т4 инициирует Escherichia coli инфекцию , связывая порины OmpC и липополисахарид ( ЛПС) на поверхности клеток E. coli своими длинными хвостовыми волокнами (LTF). [16] [17] Сигнал распознавания передается через LTF на базовую плату. Это распутывает короткие хвостовые волокна (STF), которые необратимо связываются с поверхностью клеток E. coli . Опорная пластинка меняет конформацию, а хвостовая оболочка сжимается, в результате чего GP5 на конце хвостовой трубки прокалывает внешнюю мембрану клетки. [18] Лизоцимный слой домен GP5 активируется и разрушает периплазматический пептидогликана . Оставшаяся часть мембраны разрушается, и тогда ДНК из головки вируса может пройти через хвостовую трубку и попасть в клетку E. coli . [ нужна ссылка ]
В 1952 году Херши и Чейз [19] предоставили ключевые доказательства того, что ДНК фага, в отличие от белка, проникает в бактериальную клетку-хозяина при инфекции и, таким образом, является генетическим материалом фага. Это открытие позволило предположить, что ДНК в целом является генетическим материалом различных организмов. [ нужна ссылка ]
Воспроизведение
[ редактировать ]Литический жизненный цикл (от попадания в бактерию до ее разрушения) занимает около 30 минут (при 37 °С). Вирулентные бактериофаги размножаются в бактериальном хозяине сразу после проникновения. После того, как количество дочерних фагов достигает определенного количества, они заставляют хозяина лизировать или разрушаться, поэтому они высвобождаются и заражают новые клетки-хозяева. [20] Процесс лизиса и высвобождения хозяина называется литическим циклом . Литический цикл — это цикл размножения вируса, который включает разрушение инфицированной клетки и ее мембраны. В этом цикле участвует вирус, который захватывает клетку-хозяина и ее механизм размножения. Следовательно, вирус должен пройти 5 стадий, чтобы размножиться и заразить клетку-хозяина: [ нужна ссылка ]
- Адсорбция и проникновение (начинается немедленно)
- Остановка экспрессии генов хозяина (начинается немедленно)
- Синтез ферментов (начинается через 5 минут)
- Репликация ДНК (начинается через 10 минут)
- Образование новых вирусных частиц (начинается через 12 минут)
После завершения жизненного цикла клетка-хозяин разрывается и выбрасывает вновь созданные вирусы в окружающую среду, разрушая клетку-хозяина. T4 имеет размер вспышки примерно 100-150 вирусных частиц на инфицированного хозяина. [ нужна ссылка ]
Бензер (1955 – 1959) разработал систему изучения тонкой структуры гена с использованием мутантов бактериофага Т4, дефектных по генам rIIA и rIIB . [21] [22] [23] Используемые методы включали тесты комплементации и скрещивания для обнаружения рекомбинации , особенно между делеционными мутациями. Эти генетические эксперименты привели к обнаружению уникального линейного порядка мест мутаций внутри генов. Этот результат предоставил убедительное доказательство ключевой идеи о том, что ген имеет линейную структуру, эквивалентную длине ДНК, со многими сайтами, которые могут независимо мутировать. [ нужна ссылка ]
Адсорбция и проникновение
[ редактировать ]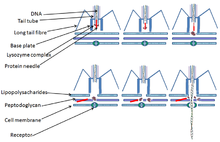
Как и все другие вирусы, Т-четные фаги не прикрепляются к поверхности хозяина случайным образом; вместо этого они «ищут» и связываются с рецепторами , специфическими белковыми структурами, обнаруженными на поверхности хозяина. Эти рецепторы различаются в зависимости от фага; тейхоевая кислота , белки клеточной стенки и липополисахариды , жгутики и пили — все они могут служить рецепторами для связывания фага. Чтобы Т-четный фаг заразил своего хозяина и начал свой жизненный цикл, он должен начать первый процесс заражения — адсорбцию фага бактериальной клеткой. Адсорбция является величиной, характеризующей пару фаг-хозяин, и адсорбция фага на поверхности клетки-хозяина представлена как двухстадийный процесс: обратимый и необратимый. Он включает в себя структуру хвоста фага, которая начинается, когда волокна хвоста фага помогают связывать фаг с соответствующим рецептором его хозяина. Этот процесс обратим. Один или несколько компонентов базовой пластинки опосредуют необратимый процесс связывания фага с бактерией. [ нужна ссылка ]
Проникновение также является ценной характеристикой заражения фагом-хозяином , которая включает инъекцию генетического материала фага внутрь бактерии . Проникновение нуклеиновой кислоты происходит после фазы необратимой адсорбции. Механизмы проникновения нуклеиновой кислоты фага специфичны для каждого фага. Этот механизм проникновения может включать электрохимический мембранный потенциал , молекулы АТФ , ферментативное расщепление слоя пептидогликана , или все три фактора могут иметь жизненно важное значение для проникновения нуклеиновой кислоты внутрь бактериальной клетки. Были проведены исследования механизма проникновения бактериофага Т2 (Т4-подобного фага), и они показали, что хвост фага не проникает внутрь клеточной стенки бактерии, а проникновение этого фага связано с электрохимическим мембранным потенциалом на внутренней мембране. [24] [25]
Тиражирование и упаковка
[ редактировать ]Геном вируса Т4 синтезируется внутри клетки-хозяина с использованием репликации по катящемуся кругу. [6] Время, необходимое для репликации ДНК в живой клетке, измерялось как скорость удлинения ДНК вируса Т4 в инфицированной вирусом E. coli. [26] В период экспоненциального роста ДНК при 37°С скорость составляла 749 нуклеотидов в секунду. Частота мутаций на пару оснований за репликацию во время синтеза ДНК вируса Т4 составляет 1,7 на 10. −8 , [27] высокоточный механизм копирования ДНК, допускающий всего 1 ошибку на 300 копий. Вирус также кодирует уникальные механизмы восстановления ДНК . [28] Головка фага Т4 собирается пустой вокруг каркасного белка, который позже разрушается. Следовательно, ДНК должна войти в проголовку через крошечную пору, что достигается за счет того, что сначала с ДНК взаимодействует гексамер gp17, который также служит мотором и нуклеазой. Было обнаружено, что двигатель упаковки ДНК T4 загружает ДНК в капсиды вируса со скоростью до 2000 пар оснований в секунду. Задействованная мощность, если ее увеличить, будет эквивалентна мощности среднего автомобильного двигателя. [29]
Выпускать
[ редактировать ]Заключительный этап репродукции и размножения вируса определяется высвобождением вирионов из клетки-хозяина. Высвобождение вирионов происходит после разрыва бактериальной плазматической мембраны. Вирусы без оболочки лизуют клетку-хозяина, для которой характерны вирусные белки, атакующие пептидогликан или мембрану. Лизис бактерий происходит, когда капсиды внутри клетки выделяют фермент лизоцим, который разрушает клеточную стенку. Высвободившиеся бактериофаги заражают другие клетки, и цикл размножения вируса повторяется внутри этих клеток. [ нужна ссылка ]
Реактивация множественности
[ редактировать ]
Реактивация множественности (MR) — это процесс, посредством которого два или более вирусных генома, каждый из которых содержит инактивирующие повреждения генома, могут взаимодействовать внутри инфицированной клетки с образованием жизнеспособного вирусного генома. Сальвадор Лурия , изучая УФ-облученный вирус Т4 в 1946 году, обнаружил MR и предположил, что наблюдаемая реактивация поврежденного вируса происходит по механизму рекомбинации (см. ссылки. [30] [31] [32] Это предшествовало подтверждению ДНК в качестве генетического материала в 1952 году в родственном вирусе Т2 экспериментом Херши-Чейза . [19]
Как вспоминает Лурия (1984, [33] стр. 97) открытие реактивации облученного вируса (называемой « реактивацией множественности ») немедленно положило начало бурной активности в изучении восстановления радиационных повреждений в группе ранних фагов (обзор Бернштейна [28] в 1981 году). Позже выяснилось, что обнаруженное Лурией восстановление поврежденного вируса путем взаимопомощи было лишь одним частным случаем восстановления ДНК. Теперь известно, что клетки всех типов, не только бактерии и их вирусы, но и все изученные организмы, включая человека, имеют сложные биохимические процессы восстановления повреждений ДНК (см. Репарация ДНК ). В настоящее время признано, что процессы восстановления ДНК играют решающую роль в защите от старения , рака и бесплодия . [ нужна ссылка ]
MR обычно представляют в виде «кривых выживания», где выживаемость бляшкообразующей способности многократно инфицированных клеток (мультикомплексов) отображается в зависимости от дозы агента, повреждающего геном. Для сравнения также построен график выживаемости вирусной бляшкообразующей способности одиночно инфицированных клеток (монокомплексов) в зависимости от дозы повреждающего геном агента. На верхнем рисунке показаны кривые выживаемости мультикомплексов и монокомплексов вируса Т4 при увеличении дозы УФ-света. Поскольку выживаемость представлена в логарифмическом масштабе, ясно, что выживаемость мультикомплексов превышает выживаемость монокомплексов в очень больших количествах (в зависимости от дозы). Кривая УФ-инактивации мультикомплексов имеет начальное плечо. Другими агентами, повреждающими ДНК вируса Т4, имеющими плечи на мультикомплексных кривых выживания, являются рентгеновские лучи. [34] [35] и этилметансульфонат (EMS). [28] Наличие плеча было интерпретировано как означающее, что используются два рекомбинационных процесса. [36] Первый восстанавливает ДНК с высокой эффективностью (в «плечо»), но насыщается по своей способности по мере увеличения повреждений; второй путь функционирует на всех уровнях повреждения. Выживший вирус Т4, выпущенный из мультикомплексов, не демонстрирует увеличения мутаций , что указывает на то, что MR вируса, облученного УФ-излучением, является точным процессом. [36]
На нижнем рисунке показаны кривые выживаемости при инактивации вируса Т4 агентом, повреждающим ДНК, митомицином С (ММС). В этом случае кривая выживаемости мультикомплексов не имеет начального плеча, что позволяет предположить, что активен только второй описанный выше процесс рекомбинационной репарации. Об эффективности репарации с помощью этого процесса свидетельствует то наблюдение, что доза ММС, обеспечивающая выживание только 1 из 1000 монокомплексов, обеспечивает выживание около 70% мультикомплексов. Аналогичные мультикомплексные кривые выживаемости (без плеч) были также получены для повреждающих ДНК агентов распада P32 , псоралена плюс ближнего УФ-облучения (ПУВА), N-метил-N'-нитро-N-нитрозогуанидина (МННГ), метилметансульфоната (ММС). ) и азотистая кислота . [28]
Некоторые из генов, которые оказались необходимыми для MR в вирусе Т4, оказались ортологами генов, необходимых для рекомбинации у прокариот , эукариот и архей . Сюда входит, например, ген Т4 uvsX. [37] который определяет белок, который имеет трехмерную структурную гомологию с RecA из Escherichia coli и гомологичным белком RAD51 у эукариот и RadA у архей . Было высказано предположение, что эффективная и точная рекомбинационная репарация повреждений ДНК при МР может быть аналогична процессу рекомбинационной репарации, происходящему во время мейоза у эукариот . [38]
История
[ редактировать ]Бактериофаги были впервые обнаружены английским ученым Фредериком Твортом в 1915 году и Феликсом д'Эрелем либо смесь неочищенных сточных вод, либо лизат кишечной палочки, в 1917 году. В конце 1930-х годов Т. Л. Ракиетен предложил двум исследователям Милиславу зараженной неочищенными сточными водами. Демерец и Уго Фано . Эти два исследователя выделили Т3, Т4, Т5 и Т6 из E.coli . Также в 1932 г. исследователь Дж. Бронфенбреннер изучал и работал над фагом Т2, при котором фаг Т2 был выделен из вируса. [39] Эта изоляция была сделана из фекального материала, а не из канализации. Во всяком случае, Макс Дельбрюк участвовал в открытии Т-фагов. Его роль заключалась в том, чтобы разделить бактериофаги на Тип 1 (Т1), Тип 2 (Т2), Тип 3 (Т3) и т. д. [ нужна ссылка ]
Точное время и место выделения вируса Т4 остается неясным, хотя, вероятно, они были обнаружены в сточных водах или фекалиях. Т4 и подобные вирусы были описаны в статье Томаса Ф. Андерсона , Макса Дельбрюка и Милислава Демерца в ноябре 1944 года. [40] В 1943 году Сальвадор Лурия и Дельбрюк показали, что бактериальные мутации устойчивости к фагам возникают в отсутствие отбора , а не являются ответом на отбор. [33] До 1943 года среди бактериологов традиционно считалось, что у бактерий нет ни хромосом, ни генов. Эксперимент Лурии-Дельбрюка показал, что бактерии, как и другие известные модельные генетические организмы, имеют гены и что они могут спонтанно мутировать, создавая мутантов, которые затем могут размножаться, образуя клональные линии. В том же году они также начали работать с Альфредом Херши , еще одним экспериментатором с фагами. [41] (Эти трое разделят Нобелевскую премию по физиологии и медицине 1969 года «за работу над механизмом репликации и генетикой вирусов».)
Группа фагов представляла собой неформальную сеть биологов во главе с Максом Дельбрюком, которая проводила фундаментальные исследования в основном бактериофага Т4 и внесла большой плодотворный вклад в генетику микробов и истоки молекулярной биологии в середине 20 века. В 1961 году Сидней Бреннер , один из первых членов группы фагов, сотрудничал с Фрэнсисом Криком , Лесли Барнеттом и Ричардом Уоттс-Тобином в Кавендишской лаборатории в Кембридже для проведения генетических экспериментов, которые продемонстрировали основную природу генетического кода белков. [42] Эти эксперименты, проведенные с мутантами гена rIIB фага Т4, показали, что для гена, кодирующего белок, три последовательных основания ДНК гена определяют каждую последующую аминокислоту белка. Таким образом, генетический код представляет собой триплетный код, где каждый триплет (называемый кодоном) определяет определенную аминокислоту. Они также получили доказательства того, что кодоны не перекрываются друг с другом в последовательности ДНК, кодирующей белок, и что такая последовательность считывается с фиксированной начальной точки. [ нужна ссылка ]
В 1962–1964 годах исследователи фага Т4 предоставили возможность изучить функцию практически всех генов, необходимых для роста фага в лабораторных условиях. [43] [44] Этим исследованиям способствовало открытие двух классов условно летальных мутантов . Один класс таких мутантов известен как янтарные мутанты . [45] Другой класс условно-летальных мутантов называется термочувствительными мутантами. [46] Исследования этих двух классов мутантов привели к значительному пониманию многочисленных фундаментальных биологических проблем. Таким образом, было получено понимание функций и взаимодействий белков, участвующих в механизме репликации , репарации и рекомбинации ДНК , а также того, как вирусы собираются из белковых компонентов и компонентов нуклеиновых кислот (молекулярный морфогенез ). Кроме того, была выяснена роль терминирующих кодонов цепи . В одном примечательном исследовании использовались янтарные мутанты, дефектные по гену, кодирующему основной головной белок фага Т4. [47] Этот эксперимент предоставил убедительные доказательства широко распространенной, но до 1964 года все еще недоказанной «гипотезы последовательности», согласно которой аминокислотная последовательность белка определяется нуклеотидной последовательностью гена, определяющего белок. Таким образом, это исследование продемонстрировало коллинеарность гена с кодируемым им белком.
Ряд лауреатов Нобелевской премии работали с вирусом Т4 или Т4-подобными вирусами, в том числе Макс Дельбрюк , Сальвадор Лурия , Альфред Херши , Джеймс Д. Уотсон и Фрэнсис Крик . Среди других важных учёных, работавших с вирусом Т4, — Майкл Россманн , Сеймур Бензер , Брюс Альбертс , Гизела Мозиг , [48] Ричард Ленски и Джеймс Булл .
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Падилья-Санчес V (2021). «Структурная модель бактериофага Т4» . Викижурнал науки 4 (1):5.doi : 10.15347 /WJS/2021.005 .
- ^ «9-й отчет ICTV (2011) Myoviridae » . Международный комитет по таксономии вирусов (ICTV) . Архивировано из оригинала 26 декабря 2018 года . Проверено 26 декабря 2018 г.
- ^ «История таксономии ICTV: вирус эшерихии Т4 » . Международный комитет по таксономии вирусов (ICTV) . Проверено 26 декабря 2018 г.
Caudovirales > Myoviridae > Tevenvirinae > T4virus > Escherichia Virus T4
- ^ Вятт Г.Р., Коэн С.С. (декабрь 1952 г.). «Новое пиримидиновое основание из нуклеиновых кислот бактериофага» . Природа . 170 (4338): 1072–1073. Бибкод : 1952Natur.170.1072W . дои : 10.1038/1701072a0 . ISSN 1476-4687 . ПМИД 13013321 . S2CID 4277592 .
- ^ Миллер Э.С., Каттер Э., Мосиг Г., Арисака Ф., Кунисава Т., Рюгер В. (март 2003 г.). «Геном бактериофага Т4» . Обзоры микробиологии и молекулярной биологии . 67 (1): 86–156, оглавление. дои : 10.1128/ммбр.67.1.86-156.2003 . ПМК 150520 . ПМИД 12626685 .
- ^ Jump up to: а б Бернштейн Х, Бернштейн С (июль 1973 г.). «Кольцевые и разветвленные кольцевые конкатенаты как возможные промежуточные соединения в репликации ДНК бактериофага Т4». Журнал молекулярной биологии . 77 (3): 355–61. дои : 10.1016/0022-2836(73)90443-9 . ПМИД 4580243 .
- ^ Мэдиган М., Мартинко Дж., ред. (2006). Брок Биология микроорганизмов (11-е изд.). Прентис Холл. ISBN 978-0-13-144329-7 .
- ^ Малис Н. (январь 2012 г.). «Последовательность Шайна-Дальгарно бактериофага Т4: GAGG преобладает в ранних генах». Отчеты по молекулярной биологии . 39 (1): 33–9. дои : 10.1007/s11033-011-0707-4 . ПМИД 21533668 . S2CID 17854788 .
- ^ Прескотт Л.М., Харли Дж.П., Кляйн Д.А. (2008). Микробиология (седьмое изд.). МакГроу-Хилл. ISBN 978-0-07-126727-4 .
- ^ Лейман П.Г., Арисака Ф., ван Раай М.Дж., Костюченко В.А., Аксюк А.А., Канамару С., Россманн М.Г. (декабрь 2010 г.). «Морфогенез хвоста Т4 и хвостовых волокон» . Вирусологический журнал . 7 : 355. дои : 10.1186/1743-422X-7-355 . ПМК 3004832 . ПМИД 21129200 .
- ^ Акерманн Х.В., Криш Х.М. (1997). «Каталог бактериофагов типа Т4». Архив вирусологии . 142 (12): 2329–45. дои : 10.1007/s007050050246 . ПМИД 9672598 . S2CID 39369249 .
- ^ Тейлор Н.М., Прохоров Н.С., Герреро-Феррейра Р.К., Шнайдер М.М., Браунинг С., Голди К.Н., Штальберг Х., Лейман П.Г. (май 2016 г.). «Структура опорной пластины Т4 и ее функция в запуске сокращения оболочки». Природа . 533 (7603): 346–52. Бибкод : 2016Natur.533..346T . дои : 10.1038/nature17971 . ПМИД 27193680 . S2CID 4399265 .
- ^ Этаж Е (февраль 1970 г.). «Взаимодействие морфогенетических генов бактериофага Т4». Журнал молекулярной биологии . 47 (3): 293–306. дои : 10.1016/0022-2836(70)90303-7 . ПМИД 4907266 .
- ^ Снустад Д.П. (август 1968 г.). «Взаимодействия доминирования в клетках Escherichia coli, смешанно инфицированных бактериофагом T4D дикого типа и янтарными мутантами, и их возможные последствия в отношении типа функции гена-продукта: каталитическая или стехиометрическая». Вирусология . 35 (4): 550–63. дои : 10.1016/0042-6822(68)90285-7 . ПМИД 4878023 .
- ^ Яп М.Л., Россманн М.Г. (2014). «Структура и функции бактериофага Т4» . Будущая микробиология . 9 (12): 1319–27. дои : 10.2217/fmb.14.91 . ПМЦ 4275845 . ПМИД 25517898 .
- ^ Ю Ф, Мизушима С (август 1982 г.). «Роль липополисахарида и белка внешней мембраны OmpC Escherichia coli K-12 в функции рецептора бактериофага Т4» . Журнал бактериологии . 151 (2): 718–22. дои : 10.1128/JB.151.2.718-722.1982 . ПМК 220313 . ПМИД 7047495 .
- ^ Фурукава Х., Мизушима С. (май 1982 г.). «Роль компонентов клеточной поверхности Escherichia coli K-12 при инфекции бактериофага Т4: взаимодействие хвостового ядра с фосфолипидами» . Журнал бактериологии . 150 (2): 916–24. дои : 10.1128/JB.150.2.916-924.1982 . ПМК 216445 . ПМИД 7040345 .
- ^ Магсуди А., Чаттерджи А., Андрисиоаи I, Перкинс, Северная Каролина (декабрь 2019 г.). «Как работает механизм инъекции фага Т4, включая энергетику, силы и динамический путь» . Труды Национальной академии наук Соединенных Штатов Америки . 116 (50): 25097–25105. Бибкод : 2019PNAS..11625097M . дои : 10.1073/pnas.1909298116 . ПМК 6911207 . ПМИД 31767752 .
- ^ Jump up to: а б ХЕРШИ Э.Д., ЧЕЙЗ М. (май 1952 г.). «Независимые функции вирусного белка и нуклеиновой кислоты в росте бактериофага» . Журнал общей физиологии . 36 (1): 39–56. дои : 10.1085/jgp.36.1.39 . ПМК 2147348 . ПМИД 12981234 .
- ^ Шервуд Л. (2011). Микробиология Прескотта (восьмое изд.). МакГроу-Хилл.
- ^ Бензер С. «Приключения в регионе rII» в книге «Фаг и истоки молекулярной биологии» (2007) под редакцией Джона Кэрнса, Гюнтера С. Стента и Джеймса Д. Уотсона, Лаборатория количественной биологии Колд-Спринг-Харбор, Колд-Спринг-Харбор, Лонг-Айленд, Нью-Йорк ISBN 978-0879698003
- ^ Бензер С. (июнь 1955 г.). «Тонкая структура генетической области бактериофага» . Труды Национальной академии наук Соединенных Штатов Америки . 41 (6): 344–54. Бибкод : 1955ПНАС...41..344Б . дои : 10.1073/pnas.41.6.344 . ПМК 528093 . ПМИД 16589677 .
- ^ Бензер С. (ноябрь 1959 г.). «К топологии тонкой генетической структуры» . Труды Национальной академии наук Соединенных Штатов Америки . 45 (11): 1607–20. Бибкод : 1959PNAS...45.1607B . дои : 10.1073/pnas.45.11.1607 . ПМК 222769 . ПМИД 16590553 .
- ^ Норкин Л.С. (2010). Вирусология, молекулярная биология и патогенез . Вашингтон: Американское общество микробиологии. п. 31. ISBN 978-1-55581-453-3 .
- ^ Прескотт Л.М., Харли Дж.П., Кляйн Д.А. (2008). Микробиология (седьмое изд.). МакГроу Хилл. п. 427. ИСБН 978-0-07-126727-4 .
- ^ Маккарти Д., Миннер С., Бернштейн Х., Бернштейн С. (1976). «Скорость элонгации ДНК и распределение точек роста фага Т4 дикого типа и янтарного мутанта с задержкой ДНК». Дж Мол Биол . 106 (4): 963–81. дои : 10.1016/0022-2836(76)90346-6 . ПМИД 789903 .
- ^ Дрейк JW (1970) Молекулярная основа мутации. Холден-Дэй, Сан-Франциско ISBN 0816224501 ISBN 978-0816224500
- ^ Jump up to: а б с д Бернштейн К. «Репарация дезоксирибонуклеиновой кислоты в бактериофаге». Microbiol Rev., март 1981 г.;45(1):72-98. Обзор. ПМИД 6261109
- ^ Рао В.Б., Черный LW (декабрь 2010 г.). «Строение и сборка головки бактериофага Т4» . Вирусологический журнал . 7 : 356. дои : 10.1186/1743-422X-7-356 . ПМК 3012670 . ПМИД 21129201 .
- ^ Лурия С.Е. (1947). «Реактивация облученного бактериофага путем переноса самовоспроизводящихся единиц» . Учеб. Натл. акад. наук. США . 33 (9): 253–64. Бибкод : 1947ПНАС...33..253Л . дои : 10.1073/pnas.33.9.253 . ПМК 1079044 . ПМИД 16588748 .
- ^ ЛУРИА С.Е., ДАЛЬБЕККО Р. (1948). «Летальные мутации и инактивация отдельных генетических детерминант бактериофага». Генетика . 33 (6): 618. PMID 18100306 .
- ^ Лурия С.Е., Дульбекко Р. (1949). «Генетические рекомбинации, ведущие к производству активного бактериофага из инактивированных ультрафиолетом частиц бактериофага» . Генетика . 34 (2): 93–125. дои : 10.1093/генетика/34.2.93 . ПМК 1209443 . ПМИД 17247312 .
- ^ Jump up to: а б Сальвадор Э. Лурия. Игровой автомат, сломанная пробирка: автобиография. Harper & Row, Нью-Йорк: 1984. Стр. 228. ISBN 0-06-015260-5 (США и Канада)
- ^ УОТСОН Джей Ди (1952). «Свойства рентгеноинактивированного бактериофага» . Дж. Бактериол . 63 (4): 473–85. дои : 10.1128/JB.63.4.473-485.1952 . ПМК 169298 . ПМИД 14938320 .
- ^ ВРЕД Ж (1958). «Множественная реактивация, спасение маркеров и генетическая рекомбинация в фаге Т4 после инактивации рентгеновскими лучами». Вирусология . 5 (2): 337–61. дои : 10.1016/0042-6822(58)90027-8 . ПМИД 13544109 .
- ^ Jump up to: а б Ярош Д.Б. (1978). «УФ-индуцированная мутация бактериофага Т4» . Дж. Вирол . 26 (2): 265–71. doi : 10.1128/JVI.26.2.265-271.1978 . ПМК 354064 . ПМИД 660716 .
- ^ История РМ, Бишоп Д.К., Клекнер Н., Стейц Т.А. (1993). «Структурная связь бактериальных белков RecA с рекомбинационными белками бактериофага Т4 и дрожжей». Наука . 259 (5103): 1892–6. Бибкод : 1993Sci...259.1892S . дои : 10.1126/science.8456313 . ПМИД 8456313 .
- ^ Бернштейн С (1979). «Почему дети такие маленькие? Мейоз может предотвратить старение зародышевой линии». Перспектива. Биол. Мед . 22 (4): 539–44. дои : 10.1353/pbm.1979.0041 . ПМИД 573881 . S2CID 38550472 .
- ^ Микробиология Уилли Дж. Прескотта (седьмое изд.). МакГроу-Хилл.
- ^ Абедон С.Т. (июнь 2000 г.). «Темное происхождение Белоснежки и ее Т-четных гномов» . Генетика . 155 (2): 481–6. дои : 10.1093/генетика/155.2.481 . ПМЦ 1461100 . ПМИД 10835374 .
- ^ Моранж, История молекулярной биологии , стр. 43-44.
- ^ КРИК Ф.Х., БАРНЕТТ Л., БРЕННЕР С., УОТТС-ТОБИН Р.Дж. (декабрь 1961 г.). «Общая природа генетического кода белков». Природа . 192 (4809): 1227–32. Бибкод : 1961Natur.192.1227C . дои : 10.1038/1921227a0 . ПМИД 13882203 . S2CID 4276146 .
- ^ Эдгар Р.С. Условные летальные исходы: в книге «Фаг и истоки молекулярной биологии» (2007) под редакцией Джона Кэрнса, Гюнтера С. Стента и Джеймса Д. Уотсона, Лаборатория количественной биологии Колд-Спринг-Харбор, Колд-Спринг-Харбор, Лонг-Айленд, Нью-Йорк ISBN 978-0879698003
- ^ Эдгар Б. (октябрь 2004 г.). «Геном бактериофага Т4: археологические раскопки» . Генетика . 168 (2): 575–82. дои : 10.1093/генетика/168.2.575 . ПМЦ 1448817 . ПМИД 15514035 .
- ^ Эпштейн Р.Х., Болле А., Стейнберг С.М., Келленбергер Э., Бой де ла Тур Э., Шевалле Р., Эдгар Р.С., Сусман М., Денхардт Г.Х., Лиелаусис А. (1963). «Физиологические исследования условно-летальных мутантов бактериофага T4D». Симпозиумы Колд-Спринг-Харбор по количественной биологии . 28 : 375–394. дои : 10.1101/SQB.1963.028.01.053 . ISSN 0091-7451 .
- ^ Эдгар Р.С., Лиелаусис I (апрель 1964 г.). «Температурно-чувствительные мутанты бактериофага T4D: их выделение и характеристика» . Генетика . 49 (4): 649–62. дои : 10.1093/генетика/49.4.649 . ПМК 1210603 . ПМИД 14156925 .
- ^ Сарабхай А.С., Стреттон А.О., Бреннер С., Болле А. (январь 1964 г.). «Колинеарность гена с полипептидной цепью». Природа . 201 (4914): 13–7. Бибкод : 1964Natur.201...13S . дои : 10.1038/201013a0 . ПМИД 14085558 . S2CID 10179456 .
- ^ Носсал Н.Г., Франклин Дж.Л., Каттер Э., Дрейк Дж.В. (ноябрь 2004 г.). «Анекдотические, исторические и критические комментарии по генетике. Гизела Мозиг» . Генетика . 168 (3): 1097–104. дои : 10.1093/генетика/168.3.1097 . ПМЦ 1448779 . ПМИД 15579671 .
Дальнейшее чтение
[ редактировать ]- Лейман П.Г., Канамару С., Месянжинов В.В., Арисака Ф., Россманн М.Г. (2003). «Структура и морфогенез бактериофага Т4» . Клеточные и молекулярные науки о жизни . 60 (11): 2356–2370. дои : 10.1007/s00018-003-3072-1 . ПМЦ 11138918 . ПМИД 14625682 . S2CID 2228357 .
- Карам Дж., Петров В., Нолан Дж., Чин Д., Шэтли К., Криш Х. и Летаров А. Проект генома Т4-подобных фагов. https://web.archive.org/web/20070523215704/http://phage.bioc.tulane.edu/ . (Хранилище полных геномных последовательностей Т4-подобного фага)
- Мозиг Г. и Ф. Эйзерлинг. 2006. Т4 и родственные фаги: структура и развитие, Р. Календарь и С.Т. Абедон (ред.), Бактериофаги. Издательство Оксфордского университета, Оксфорд. (Обзор биологии фага Т4) ISBN 0-19-514850-9
- Файли Дж. Тетарт Ф., Саттл, Калифорния, Криш Х.М. (2005). «Морские бактериофаги типа Т4, вездесущий компонент темной материи биосферы» . Учеб. Натл. акад. наук. США . 102 (35): 12471–6. Бибкод : 2005PNAS..10212471F . дои : 10.1073/pnas.0503404102 . ПМЦ 1194919 . ПМИД 16116082 . (Указание на распространенность Т4-подобных фагов в дикой природе)
- Чибани-Ченнуфи С., Канчая К., Бруттин А., Брюссов Х. (2004). «Сравнительная геномика Т4-подобного фага Escherichia coli JS98: значение для эволюции фагов Т4» . Дж. Бактериол . 186 (24): 8276–86. дои : 10.1128/JB.186.24.8276-8286.2004 . ПМК 532421 . ПМИД 15576776 . (Характеристика Т4-подобного фага)
- Деспла С., Криш Х. М. (май 2003 г.). «Разнообразие и эволюция бактериофагов типа Т4» . Рез. Микробиол . 154 (4): 259–67. дои : 10.1016/S0923-2508(03)00069-X . ПМИД 12798230 .
- Миллер, Э.С., Каттер Э., Мосиг Г., Арисака Ф., Кунисава Т., Ругер В. (2003). «Геном бактериофага Т4» . Микробиол. Мол. Биол. Преподобный . 67 (1): 86–156. дои : 10.1128/ММБР.67.1.86-156.2003 . ПМК 150520 . ПМИД 12626685 . (Обзор фага Т4 с точки зрения его генома)
- Деспла К., Дез К., Тетарт Ф., Элом Х., Криш Х.М. (2002). «Снимок генома псевдо-Т-четного бактериофага RB49» . Дж. Бактериол . 184 (10): 2789–2804. дои : 10.1128/JB.184.10.2789-2804.2002 . ПМК 135041 . ПМИД 11976309 . (Обзор генома RB49, T4-подобного фага)
- Малис Н., Чанг Д.Ю., Бауманн Р.Г., Се Д., Блэк Л.В. (2002). «Двудольная библиотека рандомизированного отображения пептидов бактериофага T4 SOC и HOC: обнаружение и анализ взаимодействия терминазы фага T4 (gp17) и позднего сигма-фактора (gp55)». Дж Мол Биол . 319 (2): 289–304. дои : 10.1016/S0022-2836(02)00298-X . ПМИД 12051907 . (Применение фага Т4 в биотехнологии для изучения взаимодействия белков)
- Тетар Ф., Деспла К., Кутателадзе М., Моно К., Акерманн Х.-В., Криш Х.М. (2001). «Филогения основных генов головы и хвоста широкомасштабных бактериофагов типа Т4» . Дж. Бактериол . 183 (1): 358–366. дои : 10.1128/JB.183.1.358-366.2001 . ПМК 94885 . ПМИД 11114936 . (Указание на распространенность последовательностей типа Т4 в дикой природе)
- Абедон СТ (2000). «Темное происхождение Белоснежки и ее Т-четных гномов» . Генетика . 155 (2): 481–6. дои : 10.1093/генетика/155.2.481 . ПМЦ 1461100 . ПМИД 10835374 . (Историческое описание выделения Т4-подобных фагов Т2, Т4 и Т6)
- Акерманн Х.В., Криш Х.М. (1997). «Каталог бактериофагов типа Т4» . Арх. Вирол . 142 (12): 2329–45. дои : 10.1007/s007050050246 . ПМИД 9672598 . S2CID 39369249 . Архивировано из оригинала 1 ноября 2001 г. (Почти полный список известных на тот момент Т4-подобных фагов).
- Моно С., Репоила Ф., Кутателадзе М., Тетар Ф., Криш Х.М. (март 1997 г.). «Геном псевдоТ-четных бактериофагов, разнообразной группы, напоминающей Т4». Дж. Мол. Биол . 267 (2): 237–49. дои : 10.1006/jmbi.1996.0867 . ПМИД 9096222 . (Обзор различных Т4-подобных фагов с точки зрения их геномов)
- Каттер Э., Гачечиладзе К., Поглазов А., Марусич Э., Шнайдер М., Аронссон П., Напули А., Портер Д., Месянжинов В. (1995). «Эволюция фагов, родственных Т4». Гены вирусов . 11 (2–3): 285–297. дои : 10.1007/BF01728666 . ПМИД 8828153 . S2CID 20529415 . (Сравнение геномов различных Т4-подобных фагов)
- Карам, JD и др. 1994. Молекулярная биология бактериофага Т4. ASM Press, Вашингтон, округ Колумбия. (Вторую Библию о Т4 можно найти здесь, а также Mosig and Eiserling, 2006, чтобы начать изучать биологию фага Т4.) ISBN 1-55581-064-0
- Эдди, С.Р. 1992. Интроны в Т-четных бактериофагах. Кандидатская диссертация. Университет Колорадо в Боулдере. (В главе 3 представлен обзор различных Т4-подобных фагов, а также выделение новых на тот момент Т4-подобных фагов.)
- Сурдис, Т. Дж. «и др.», Калифорнийский университет в Санта-Крус, ноябрь 1978 г., «Методы прикрепления бактериофагов, специфичные для Т4», анализ, обзор.
- Мэтьюз, К.К., Э.М. Каттер, Г. Мосиг и П.Б. Бергет. 1983. Бактериофаг Т4. Американское общество микробиологии, Вашингтон, округ Колумбия. (Первая Библия Т4; не вся информация здесь дублируется у Карама и др. , 1994; см., в частности, вводную главу Дормана для исторического обзора Т4-подобных фагов) ISBN 0-914826-56-5
- Рассел, Р.Л. 1967. Видообразование среди Т-четных бактериофагов. Кандидатская диссертация. Калифорнийский технологический институт. (Выделение серии RB Т4-подобных фагов)
- Малис Н., Нивинскас Р. (2009). «Неканоническое расположение РНК в Т4-четных фагах: сайт связывания рибосомы размещен в межцистронном соединении гена 26-25». Мол Микробиол . 73 (6): 1115–1127. дои : 10.1111/j.1365-2958.2009.06840.x . ПМИД 19708923 . S2CID 8187771 . (редкий тип трансляционной регуляции, характерный для Т4)
- Кей Д., Филдс П. (1962). «Гидроксиметилцитозинсодержащие и триптофанзависимые бактериофаги, выделенные из городских сточных вод» . Дж. Генерал Микробиол . 27 : 143–6. дои : 10.1099/00221287-27-1-143 . ПМИД 14454648 . (Выделение Т4-подобных фагов, включая фаг Ох2)