Вирусология

Вирусология – это научное исследование биологических вирусов . Это раздел микробиологии , который фокусируется на их обнаружении, структуре, классификации и эволюции, методах заражения и использовании - хозяев клеток для размножения, их взаимодействии с физиологией и иммунитетом организма-хозяина, заболеваниях, которые они вызывают, методах выделения и культивирования. их и их использование в исследованиях и терапии.
(1898) возбудителя болезни табачной мозаики (ТМВ) как нового патогена Идентификация Мартинусом Бейеринком в настоящее время признана официальным началом развития вирусологии как дисциплины, отличной от бактериологии . Он понял, что источником была не бактериальная и не грибковая инфекция , а нечто совершенно иное. Бейеринк использовал слово «вирус» для описания загадочного агента в своей книге « contagium vivum fluidum » («заразная живая жидкость»). Розалинда Франклин предложила полную структуру вируса табачной мозаики в 1955 году.
Одной из основных причин изучения вирусов является то, что они вызывают многие инфекционные заболевания растений и животных. [1] Изучение того, каким образом вирусы вызывают заболевания, называется вирусным патогенезом . Степень, в которой вирус вызывает заболевание, является его вирулентностью . [2] Эти области исследований называются вирусологией растений , вирусологией животных и человеческой или медицинской вирусологией . [3]
Вирусология возникла, когда не было методов распространения или визуализации вирусов или специальных лабораторных тестов на вирусные инфекции. Методов разделения вирусных нуклеиновых кислот ( РНК и ДНК ) и белков , которые сейчас являются основой вирусологии, не существовало. Сейчас существует множество методов наблюдения за строением и функциями вирусов и их составных частей. Сейчас известны тысячи различных вирусов, и вирусологи часто специализируются либо на вирусах, поражающих растения, либо на бактериях и других микроорганизмах , либо на животных. Вирусы, поражающие человека, сейчас изучают медицинские вирусологи. Вирусология – это широкий предмет, охватывающий биологию, здравоохранение, защиту животных, сельское хозяйство и экологию.
История [ править ]

Луи Пастер не смог найти возбудителя бешенства и предположил, что возбудитель слишком мал, чтобы его можно было обнаружить с помощью микроскопа. [4] В 1884 году французский микробиолог Шарль Чемберлан изобрел фильтр Чемберланда (или фильтр Пастера-Чемберленда) с порами, достаточно маленькими, чтобы удалить все бактерии из прошедшего через него раствора. [5] В 1892 году русский биолог Дмитрий Ивановский использовал этот фильтр для изучения того, что сейчас известно как вирус табачной мозаики : измельченные экстракты листьев зараженных растений табака оставались заразными даже после фильтрации для удаления бактерий. Ивановский предположил, что инфекция может быть вызвана токсином, вырабатываемым бактериями, но не стал развивать эту идею. [6] В то время считалось, что все инфекционные агенты могут быть задержаны фильтрами и выращены на питательной среде — это было частью микробной теории болезней . [7]
В 1898 году голландский микробиолог Мартинус Бейеринк повторил эксперименты и убедился, что отфильтрованный раствор содержит новую форму инфекционного агента. [8] Он заметил, что агент размножается только в делящихся клетках, но, поскольку его эксперименты не показали, что он состоит из частиц, он назвал его contagium vivum Liquidum (растворимый живой микроб) и вновь ввел слово вирус . Бейеринк утверждал, что вирусы по своей природе являются жидкими — теория, позже дискредитированная Уэнделлом Стэнли , доказавшим, что они состоят из частиц. [6] В том же году Фридрих Леффлер первый вирус животных, афтовирус (возбудитель ящура ). и Пауль Фрош пропустили через аналогичный фильтр [9]
В начале 20 века английский бактериолог Фредерик Творт открыл группу вирусов, поражающих бактерии, которые сейчас называются бактериофагами. [10] (или обычно «фаги»), а франко-канадский микробиолог Феликс д'Эрель описал вирусы, которые при добавлении к бактериям на чашке с агаром производят участки мертвых бактерий. Он аккуратно разбавил суспензию этих вирусов и обнаружил, что самые высокие разведения (самые низкие концентрации вируса) не убивают все бактерии, а образуют отдельные участки мертвых организмов. Подсчет этих площадей и умножение на коэффициент разведения позволили ему подсчитать количество вирусов в исходной суспензии. [11] Фаги были провозглашены потенциальным средством лечения таких заболеваний, как брюшной тиф и холера , но их обещания были забыты с разработкой пенициллина . Развитие устойчивости бактерий к антибиотикам возобновило интерес к терапевтическому использованию бактериофагов. [12]
К концу 19-го века вирусы были определены с точки зрения их инфекционности , способности проходить через фильтры и их потребности в живых хозяевах. Вирусы выращивали только на растениях и животных. В 1906 году Росс Грэнвилл Харрисон изобрел метод выращивания ткани в лимфе , а в 1913 году Э. Стейнхардт, К. Израэл и Р. А. Ламберт использовали этот метод для выращивания вируса коровьей оспы во фрагментах ткани роговицы морской свинки. [13] В 1928 году Х.Б. Мейтленд и М.С. Мейтленд вырастили вирус коровьей оспы в суспензиях измельченных куриных почек. Их метод не получил широкого распространения до 1950-х годов, когда полиовирус стал выращиваться в больших масштабах для производства вакцин. [14]
Еще один прорыв произошел в 1931 году, когда американские патологи Эрнест Уильям Гудпасчер и Элис Майлз Вудрафф вырастили грипп и несколько других вирусов в оплодотворенных куриных яйцах. [15] В 1949 году Джон Франклин Эндерс , Томас Веллер и Фредерик Роббинс вырастили полиовирус в культивируемых клетках из ткани абортированного эмбриона человека. [16] первый вирус, выращенный без использования твердых тканей животных или яиц. Эта работа позволила Хилари Копровски , а затем и Джонасу Солку создать эффективную вакцину против полиомиелита . [17]
Первые изображения вирусов были получены после изобретения электронной микроскопии в 1931 году немецкими инженерами Эрнстом Руской и Максом Кноллем . [18] В 1935 году американский биохимик и вирусолог Уэнделл Мередит Стэнли исследовал вирус табачной мозаики и обнаружил, что он в основном состоит из белка. [19] Спустя некоторое время этот вирус был разделен на белковую и РНК-части. [20] первым Вирус табачной мозаики был кристаллизован , и поэтому его структуру удалось выяснить подробно. Первые рентгеновские дифракционные изображения кристаллизованного вируса были получены Берналом и Фанкюхеном в 1941 году. На основе своих рентгеновских кристаллографических изображений Розалинда Франклин открыла полную структуру вируса в 1955 году. [21] В том же году Хайнц Френкель-Конрат и Робли Уильямс показали, что очищенная РНК вируса табачной мозаики и его белковая оболочка могут собираться сами по себе с образованием функциональных вирусов, предполагая, что этот простой механизм, вероятно, был средством, с помощью которого вирусы создавались внутри клеток-хозяев. . [22]
Вторая половина 20-го века была золотым веком открытия вирусов, и в эти годы было открыто большинство задокументированных видов вирусов животных, растений и бактерий. [23] В 1957 году был открыт артеривирус лошадей и возбудитель вирусной диареи крупного рогатого скота ( пестивирус ). В 1963 году вирус гепатита В был открыт Барухом Блюмбергом . [24] а в 1965 году Говард Темин описал первый ретровирус . Обратная транскриптаза , фермент , который ретровирусы используют для создания ДНК-копий своей РНК, была впервые описана в 1970 году независимо друг от друга Темином и Дэвидом Балтимором . [25] В 1983 году Люка Монтанье группа из Института Пастера во Франции впервые выделила ретровирус, который теперь называется ВИЧ. [26] В 1989 году Майкла Хоутона команда из корпорации Chiron обнаружила гепатит С. [27] [28]
Обнаружение вирусов [ править ]

Существует несколько подходов к обнаружению вирусов, в том числе обнаружение вирусных частиц (вирионов) или их антигенов или нуклеиновых кислот, а также анализы на инфекционность.
Электронная микроскопия [ править ]

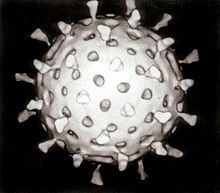
Впервые вирусы были обнаружены в 1930-х годах, когда были изобретены электронные микроскопы. используются пучки электронов В этих микроскопах вместо света , которые имеют гораздо более короткую длину волны и могут обнаруживать объекты, которые невозможно увидеть с помощью световых микроскопов. Максимальное увеличение, которое можно получить с помощью электронного микроскопа, составляет до 10 000 000 раз. [29] тогда как для световых микроскопов это около 1500 раз. [30]
Вирусологи часто используют негативное окрашивание , чтобы визуализировать вирусы. В этой процедуре вирусы суспендируют в растворе солей металлов, таких как ацетат урана. Атомы металла непрозрачны для электронов, и вирусы кажутся взвешенными на темном фоне атомов металла. [29] Этот метод используется с 1950-х годов. [31] Многие вирусы были обнаружены с помощью этого метода, и электронная микроскопия с отрицательным окрашиванием до сих пор остается ценным оружием в арсенале вирусолога. [32]
Традиционная электронная микроскопия имеет недостатки, заключающиеся в том, что вирусы повреждаются при сушке в высоком вакууме внутри электронного микроскопа, а сам электронный луч является разрушительным. [29] В криогенной электронной микроскопии структура вирусов сохраняется за счет помещения их в среду стекловидной воды . [33] Это позволяет определять биомолекулярные структуры с разрешением, близким к атомному. [34] и привлек широкое внимание к этому подходу как альтернативе рентгеновской кристаллографии или ЯМР-спектроскопии для определения структуры вирусов. [35]
Рост культур [ править ]
Вирусы являются обязательными внутриклеточными паразитами, и поскольку они размножаются только внутри живых клеток хозяина, эти клетки необходимы для их выращивания в лаборатории. Для вирусов, поражающих животных (обычно называемых «вирусами животных»), клетки, выращенные в лабораторных культурах клеток используются . Раньше использовались оплодотворенные куриные яйца, и вирусы выращивались на оболочках, окружающих эмбрион. Этот метод до сих пор используется при производстве некоторых вакцин. Для вирусов, поражающих бактерии, можно напрямую использовать бактериофаги , бактерии, растущие в пробирках. Для вирусов растений можно использовать естественные растения-хозяева или, особенно, когда инфекция не очевидна, так называемые растения-индикаторы, которые более четко проявляют признаки инфекции. [36] [37]
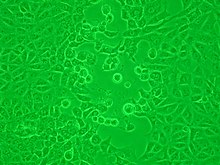
Вирусы, выросшие в клеточных культурах, можно обнаружить косвенно по вредному воздействию, которое они оказывают на клетку-хозяина. Эти цитопатические эффекты часто характерны для данного типа вируса. Например, вирусы простого герпеса вызывают характерное «раздувание» клеток, обычно фибробластов человека . Некоторые вирусы, такие как вирус эпидемического паротита, вызывают прочное прикрепление эритроцитов кур к инфицированным клеткам. Это называется «гемадсорбция» или «гемадсорбция». Некоторые вирусы производят локализованные «повреждения» в клеточных слоях, называемые бляшками , которые полезны при количественном анализе и идентификации вида вируса с помощью анализов уменьшения бляшек . [38] [39]
Вирусы, растущие в клеточных культурах, используются для измерения их чувствительности к проверенным и новым противовирусным препаратам . [40]
Серология [ править ]
Вирусы — это антигены , которые индуцируют выработку антител , и эти антитела можно использовать в лабораториях для изучения вирусов. Родственные вирусы часто реагируют с антителами друг друга, и некоторые вирусы можно назвать по антителам, с которыми они реагируют. Использование антител, которые когда-то получали исключительно из сыворотки (кровяной жидкости) животных, называется серологией . [41] Если в тесте произошла реакция антител, для подтверждения этого необходимы другие методы. Старые методы включали тесты на фиксацию комплемента . [42] торможение гемагглютинации и нейтрализация вируса . [43] В новых методах используются иммуноферментные анализы (ИФА). [44]
За годы до ПЦР изобретения иммунофлуоресценция использовалась для быстрого подтверждения вирусных инфекций. Это анализ инфекционности, специфичный для вида вируса, поскольку используются антитела. Антитела помечаются люминесцентным красителем, и при использовании оптического микроскопа с модифицированным источником света инфицированные клетки светятся в темноте. [45]
обнаружения нуклеиновых кислот другие методы и Полимеразная цепная реакция (ПЦР )
ПЦР — основной метод обнаружения вирусов у всех видов, включая растения и животных. Он работает путем обнаружения следов специфичной для вируса РНК или ДНК. Он очень чувствителен и специфичен, но может быть легко нарушен в результате загрязнения. Большинство тестов, используемых в ветеринарной вирусологии и медицинской вирусологии, основаны на ПЦР или аналогичных методах, таких как амплификация, опосредованная транскрипцией . Когда появляется новый вирус, такой как коронавирус Covid, можно быстро разработать специальный тест, если секвенировать вирусный геном и идентифицировать уникальные области вирусной ДНК или РНК. [46] Изобретение микрофлюидных тестов позволило автоматизировать большинство этих тестов. [47] Несмотря на свою специфичность и чувствительность, ПЦР имеет недостаток, заключающийся в том, что она не различает инфекционные и неинфекционные вирусы, и «тесты на излечение» приходится откладывать на срок до 21 дня, чтобы дать возможность остаточной вирусной нуклеиновой кислоте удалиться из места заражения. инфекция. [48]
Диагностические тесты [ править ]
В лабораториях многие диагностические тесты для обнаружения вирусов представляют собой методы амплификации нуклеиновых кислот, такие как ПЦР. Некоторые тесты выявляют вирусы или их компоненты, например, электронная микроскопия и иммуноферментный анализ . Так называемые «домашние» или «самостоятельные» устройства для тестирования обычно представляют собой тесты с боковым потоком , которые обнаруживают вирус с помощью меченых моноклональных антител . [49] Они также используются в сельском хозяйстве, пищевой промышленности и науках об окружающей среде. [50]
и вирусная определение Количественное нагрузка
Подсчет вирусов (количественное определение) всегда играл важную роль в вирусологии и стал центральным элементом борьбы с некоторыми инфекциями человека, при которых вирусная нагрузка . измеряется [51] Существует два основных метода: тот, который подсчитывает полностью инфекционные вирусные частицы, которые называются анализами инфекционности, и тот, который подсчитывает все частицы, включая дефектные. [29]
Анализы инфекционность на
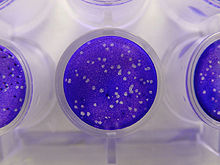
Анализы инфекционности измеряют количество (концентрацию) инфекционных вирусов в образце известного объема. [52] В качестве клеток-хозяев используют растения или культуры бактериальных или животных клеток. Лабораторные животные, такие как мыши, также использовались, в частности, в ветеринарной вирусологии. [53] Это анализы либо количественные, когда результаты имеют непрерывный масштаб, либо количественные, когда событие либо происходит, либо нет. Количественные анализы дают абсолютные значения , а количественные анализы дают статистическую вероятность, например, объем тестируемого образца, необходимый для обеспечения инфицирования 50% клеток-хозяев, растений или животных. Это называется средней инфекционной дозой или ID 50 . [54] Инфекционные бактериофаги можно подсчитать, посеяв их на «лужайки» бактерий в культуральных чашках. В низких концентрациях вирусы образуют дыры в газоне, которые можно сосчитать. Затем количество вирусов выражают в единицах образования бляшек . Для бактериофагов, которые размножаются в бактериях, которые невозможно выращивать в культурах, используются анализы вирусной нагрузки. [55]
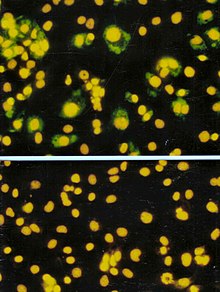
Анализ формирования фокуса (FFA) представляет собой вариант анализа бляшек, но вместо того, чтобы полагаться на лизис клеток для обнаружения образования бляшек, FFA использует иммуноокрашивания методы с использованием флуоресцентно-меченых антител, специфичных для вирусного антигена, для обнаружения инфицированных клеток-хозяев и инфекционных клеток. вирусные частицы до того, как образуется настоящий зубной налет. FFA особенно полезен для количественного определения классов вирусов, которые не лизируют клеточные мембраны, поскольку эти вирусы не поддаются анализу бляшек. Как и при анализе бляшек, монослои клеток-хозяев инфицируются различными разведениями образца вируса и инкубируются в течение относительно короткого периода инкубации (например, 24–72 часа) в полутвердой среде, которая ограничивает распространение инфекционного вируса, создавая локализованные скопления (очаги) инфицированных клеток. Затем планшеты исследуют флуоресцентно меченными антителами против вирусного антигена и используют флуоресцентную микроскопию для подсчета и количественного определения количества очагов. Метод FFA обычно дает результаты за меньшее время, чем метод бляшек или пятипроцентная инфекционная доза в тканевой культуре (TCID). 50 ) анализы, но они могут быть более дорогими с точки зрения необходимых реагентов и оборудования. Время завершения анализа также зависит от размера площади, которую считает пользователь. Большая площадь потребует больше времени, но может обеспечить более точное представление образца. Результаты FFA выражаются в единицах фокусообразования на миллилитр, или FFU/ [56]
нагрузки вирусной Анализы
Когда проводится анализ для измерения количества инфекционных вирусных частиц (анализ бляшек, анализ фокуса), титр вируса часто относится к концентрации инфекционных вирусных частиц, которая отличается от общего количества вирусных частиц. Анализы вирусной нагрузки обычно подсчитывают количество присутствующих вирусных геномов, а не количество частиц, и используют методы, аналогичные ПЦР . [57] Тесты на вирусную нагрузку играют важную роль в борьбе с ВИЧ-инфекцией. [58] Этот универсальный метод можно использовать для вирусов растений. [59] [60]
биология Молекулярная
Молекулярная вирусология — это изучение вирусов на уровне нуклеиновых кислот и белков. Все методы, изобретенные молекулярными биологами, оказались полезными в вирусологии. Их небольшие размеры и относительно простая структура делают вирусы идеальными кандидатами для изучения этими методами.
Очистка вирусов и их компонентов [ править ]

Для дальнейшего изучения вирусы, выращенные в лаборатории, необходимо очистить от примесей из клеток-хозяев. Преимущество используемых методов часто заключается в концентрации вирусов, что облегчает их исследование.
Центрифугирование [ править ]
Центрифуги часто используются для очистки вирусов. Низкоскоростные центрифуги, то есть центрифуги с максимальной скоростью 10 000 оборотов в минуту (об/мин), недостаточно мощны для концентрации вирусов, а ультрацентрифуги с максимальной скоростью около 100 000 об/мин — достаточно мощные, и эта разница используется в методе, называемом дифференциальным центрифугированием . В этом методе более крупные и тяжелые примеси удаляются из вирусной смеси центрифугированием на низкой скорости. Маленькие и легкие вирусы, оставленные во взвешенном состоянии, затем концентрируются с помощью высокоскоростного центрифугирования. [62]
После дифференциального центрифугирования суспензии вирусов часто остаются загрязненными остатками, имеющими тот же коэффициент седиментации , и не удаляются в ходе процедуры. модификация центрифугирования, называемая центрифугированием с плавучей плотностью В этих случаях используется . В этом методе вирусы, выделенные в результате дифференциального центрифугирования, снова центрифугируются на очень высокой скорости в течение нескольких часов в плотных растворах сахаров или солей, которые образуют градиент плотности от низкой к высокой в пробирке во время центрифугирования. В некоторых случаях используются заранее сформированные градиенты, в которых решения постепенно уменьшающейся плотности тщательно накладываются друг на друга. Как и объект в Мертвом море , несмотря на центробежную силу, частицы вируса не могут погрузиться в более плотные растворы, чем они есть на самом деле, и образуют в пробирке отдельные слои, часто видимые, концентрированные вирусы. Для этих растворов часто используется хлорид цезия, поскольку он относительно инертен, но легко образует градиент при центрифугировании на высокой скорости в ультрацентрифуге. [61] Центрифугирование с плавучей плотностью также можно использовать для очистки компонентов вирусов, таких как их нуклеиновые кислоты или белки. [63]
Электрофорез [ править ]
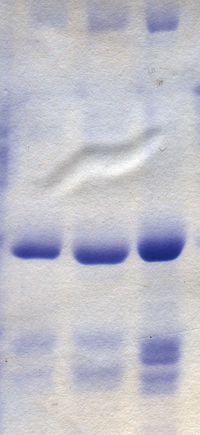
Разделение молекул на основе их электрического заряда называется электрофорезом . С помощью этого метода можно отделить и очистить вирусы и все их компоненты. Обычно это делается в поддерживающей среде, такой как агарозный и полиакриламидный гели . Отделенные молекулы выявляют с помощью красителей, таких как кумази синий для белков или бромистый этидий для нуклеиновых кислот. В некоторых случаях вирусные компоненты становятся радиоактивными перед электрофорезом и обнаруживаются с помощью фотопленки в процессе, известном как авторадиография . [64]
Секвенирование вирусных геномов [ править ]
Поскольку большинство вирусов слишком малы, чтобы их можно было увидеть в световой микроскоп, секвенирование является одним из основных инструментов в вирусологии для идентификации и изучения вируса. Традиционное секвенирование по Сэнгеру и секвенирование нового поколения (NGS) используются для секвенирования вирусов в фундаментальных и клинических исследованиях, а также для диагностики новых вирусных инфекций, молекулярной эпидемиологии вирусных патогенов и тестирования на лекарственную устойчивость. В GenBank хранится более 2,3 миллиона уникальных вирусных последовательностей. [65] NGS превзошел традиционный метод Сэнгера как самый популярный подход к созданию вирусных геномов. [65] Секвенирование вирусного генома стало центральным методом вирусной эпидемиологии и классификации вирусов .
Филогенетический анализ [ править ]
Данные секвенирования вирусных геномов могут быть использованы для определения эволюционных связей, и это называется филогенетическим анализом . [66] Программное обеспечение, такое как PHYLIP , используется для построения филогенетических деревьев . Этот анализ также используется при изучении распространения вирусных инфекций в сообществах ( эпидемиология ). [67]
Клонирование [ править ]
Когда для диагностических тестов или вакцин необходимы очищенные вирусы или вирусные компоненты, вместо выращивания вирусов можно использовать клонирование. [68] В начале пандемии COVID-19 наличие последовательности РНК коронавируса 2 тяжелого острого респираторного синдрома позволило быстро изготовить тесты. [69] Существует несколько проверенных методов клонирования вирусов и их компонентов. небольшие фрагменты ДНК, называемые векторами клонирования Часто используются , и наиболее распространенными из них являются лабораторно модифицированные плазмиды (небольшие кольцевые молекулы ДНК, вырабатываемые бактериями). Вирусная нуклеиновая кислота или ее часть встраивается в плазмиду, которая многократно копируется бактериями. Эту рекомбинантную ДНК затем можно использовать для производства вирусных компонентов без необходимости использования нативных вирусов. [70]
вирусология Фаговая
Вирусы, размножающиеся в бактериях, археях и грибах, неофициально называются «фагами». [71] а те, которые заражают бактерии – бактериофаги – особенно полезны в вирусологии и биологии в целом. [72] Бактериофаги были одними из первых вирусов, открытых в начале двадцатого века. [73] и поскольку их относительно легко быстро вырастить в лабораториях, большая часть нашего понимания вирусов возникла в результате их изучения. [73] Бактериофаги, давно известные своим положительным воздействием на окружающую среду, используются в методах фагового дисплея для скрининга последовательностей ДНК белков. Они являются мощным инструментом в молекулярной биологии. [74]
Генетика [ править ]
Все вирусы имеют гены , которые изучаются с помощью генетики . [75] Все методы, используемые в молекулярной биологии, такие как клонирование, создание мутаций, подавление РНК, используются в вирусной генетике. [76]
Реассортимент [ править ]
Реассортация — это переключение генов от разных родителей, и она особенно полезна при изучении генетики вирусов, которые имеют сегментированные геномы (фрагментированные на две или более молекулы нуклеиновой кислоты), таких как вирусы гриппа и ротавирусы . гены, которые кодируют такие свойства, как серотип . Таким образом можно идентифицировать [77]
Рекомбинация [ править ]
Рекомбинацию, которую часто путают с реассортацией, также называют смешиванием генов, но механизм отличается тем, что участки молекул ДНК или РНК, а не полные молекулы, соединяются во время цикла репликации РНК или ДНК. Рекомбинация не так распространена в природе, как рекомбинация, но является мощным лабораторным инструментом изучения структуры и функций вирусных генов. [78]
Обратная генетика [ править ]
Обратная генетика — мощный исследовательский метод в вирусологии. [79] В этой процедуре комплементарные копии ДНК (кДНК) вирусных геномов, называемые «инфекционными клонами», используются для производства генетически модифицированных вирусов, которые затем можно проверить на предмет изменений, скажем, вирулентности или трансмиссивности. [80]
Классификация вирусов [ править ]
Важнейшим разделом вирусологии является классификация вирусов . Он искусственен в том смысле, что основан не на эволюционной филогенетике , а на общих или отличительных свойствах вирусов. [81] [82] Он стремится описать разнообразие вирусов, называя и группируя их на основе сходства. [83] В 1962 году Андре Львофф , Роберт Хорн и Поль Турнье первыми разработали способ классификации вирусов, основанный на иерархической системе Линнея . [84] Эта система основана на классификации по типу , классу , отряду , семейству , роду и виду . Вирусы были сгруппированы в соответствии с их общими свойствами (а не свойствами их хозяев) и типом нуклеиновой кислоты, образующей их геномы. [85] В 1966 году был создан Международный комитет по таксономии вирусов (ICTV). Система, предложенная Львоффом, Хорном и Турнье, изначально не была принята ICTV, поскольку небольшой размер генома вирусов и высокая скорость их мутаций затрудняли определение их происхождения за пределами порядка. Таким образом, система классификации Балтимора стала использоваться в качестве дополнения к более традиционной иерархии. [86] Начиная с 2018 года ICTV начал признавать более глубокие эволюционные связи между вирусами, которые были обнаружены с течением времени, и принял 15-ранговую систему классификации, варьирующуюся от области до вида. [87] Кроме того, некоторые виды одного рода объединены в геногруппу . [88] [89]
Классификация ICTV [ править ]
ICTV разработала действующую систему классификации и написала рекомендации, которые придают больший вес определенным свойствам вируса для поддержания единообразия семейства. Установлена единая таксономия (универсальная система классификации вирусов). Изучена лишь небольшая часть от общего разнообразия вирусов. [90] 6 сфер, 10 царств, 17 типов, 2 подтипа, 39 классов, 65 отрядов, 8 подотрядов, 233 семейства, 168 подсемейств , 2606 родов, 84 подрода и 10 434 вида вирусов. По состоянию на 2021 год ICTV определило [91]
Ниже представлена общая таксономическая структура ареалов таксонов и суффиксы, используемые в таксономических названиях. По состоянию на 2021 год ранги подцарства, подцарства и подкласса не используются, тогда как все остальные ранги используются. [91]
- Царство ( -вирия )
- Подцарство ( -вира )
- Королевство ( -virae )
- Подцарство ( -вира )
Балтиморская классификация

Лауреат Нобелевской премии по биологии Дэвид Балтимор разработал систему классификации Балтимора . [92]
Балтиморская классификация вирусов основана на механизме продукции мРНК . Вирусы должны генерировать мРНК из своих геномов, чтобы производить белки и воспроизводить себя, но для достижения этой цели в каждом семействе вирусов используются разные механизмы. Вирусные геномы могут быть одноцепочечными (ss) или двухцепочечными (ds), РНК или ДНК и могут использовать или не использовать обратную транскриптазу (RT). Кроме того, вирусы оцРНК могут быть смысловыми (+) или антисмысловыми (-). Эта классификация делит вирусы на семь групп:
- I: вирусы с дцДНК (например, аденовирусы , герпесвирусы , поксвирусы )
- II: ДНК вирусов оцДНК (+ цепь или «смысловая») ДНК (например, парвовирусов )
- III: вирусы дсРНК (например, реовирусы )
- IV: (+)оцРНК вирусов (+ цепь или смысловая) РНК (например , коронавирусы , пикорнавирусы , тогавирусы )
- В: (-)оцРНК вирусов (-цепь или антисмысловая РНК) (например, ортомиксовирусы , рабдовирусы )
- VI: вирусы оцРНК-RT (+ цепь или смысловая РНК) с промежуточной ДНК в жизненном цикле (например, ретровирусы )
- VII: дцДНК-RT ДНК вирусов с промежуточной РНК в жизненном цикле (например, гепаднавирусы )
Ссылки [ править ]
- ^ Доля В.В., Кунин Е.В. (ноябрь 2011 г.). «Общее происхождение и зависящее от хозяина разнообразие виромов растений и животных» . Современное мнение в вирусологии . 1 (5): 322–31. дои : 10.1016/j.coviro.2011.09.007 . ПМК 3293486 . ПМИД 22408703 .
- ^ Novella IS, Presloid JB, Taylor RT (декабрь 2014 г.). «Ошибки репликации РНК и эволюция патогенности и вирулентности вируса». Современное мнение в вирусологии . 9 : 143–7. дои : 10.1016/j.coviro.2014.09.017 . ПМИД 25462446 .
- ^ Продажи Р.К., Ораньо Х., Эстанислао Р.Д., Бальестерос А.Дж., Гомес М.И. (29 апреля 2021 г.). «Определение приоритетов исследований в области вирусологии человека, растений и животных: онлайн-опыт для Института вирусологии Филиппин» . Политика и системы медицинских исследований . 19 (1): 70. дои : 10.1186/s12961-021-00723-z . ISSN 1478-4505 . ПМК 8082216 . ПМИД 33926472 .
- ^ Борденейв Дж. (май 2003 г.). «Луи Пастер (1822-1895)». Микробы и инфекции . 5 (6): 553–60. дои : 10.1016/S1286-4579(03)00075-3 . ПМИД 12758285 .
- ↑ Шорс стр. 74, 827.
- ↑ Перейти обратно: Перейти обратно: а б Коллиер п. 3
- ^ Диммок с. 4
- ^ Диммок, стр. 4–5.
- ^ Феннер Ф (2009). Махи Б.В., Ван Регенмортал М.Х. (ред.). Настольная энциклопедия общей вирусологии (1-е изд.). Оксфорд: Академическая пресса. п. 15. ISBN 978-0-12-375146-1 .
- ^ Шорс с. 827
- ^ Д'Эрель Ф (сентябрь 2007 г.). «О невидимом микробе, антагонисте дизентерийных бацилл: краткая заметка г-на Ф. Д'Эреля, представленная г-ном Ру. 1917» . Исследования в области микробиологии . 158 (7): 553–54. дои : 10.1016/j.resmic.2007.07.005 . ПМИД 17855060 .
- ^ Доминго-Калап П., Джорджель П., Бахрам С. (март 2016 г.). «Назад в будущее: бактериофаги как перспективные терапевтические инструменты». ХЛА . 87 (3): 133–40. дои : 10.1111/tan.12742 . ПМИД 26891965 . S2CID 29223662 .
- ^ Стейнхардт Э., Израильтянин С., Ламберт Р.А. (1913). «Исследования по культивированию вируса коровьей оспы» . Журнал инфекционных болезней . 13 (2): 294–300. дои : 10.1093/infdis/13.2.294 .
- ^ Кольер с. 4
- ^ Гудпасчер Э.В., Вудрафф А.М., Баддинг Г.Дж. (октябрь 1931 г.). «Культивирование вакцинных и других вирусов в хориоаллантоисной оболочке куриных эмбрионов». Наука . 74 (1919): 371–72. Бибкод : 1931Sci....74..371G . дои : 10.1126/science.74.1919.371 . ПМИД 17810781 .
- ^ Томас Хакл Веллер (2004). Выращивание патогенов в тканевых культурах: пятьдесят лет академической тропической медицины, педиатрии и вирусологии . Бостонская медицинская библиотека. п. 57. ИСБН 978-0-88135-380-8 .
- ^ Розен Ф.С. (октябрь 2004 г.). «Выделение полиовируса - Джон Эндерс и Нобелевская премия». Медицинский журнал Новой Англии . 351 (15): 1481–83. дои : 10.1056/NEJMp048202 . ПМИД 15470207 .
- ^ Френгсмир Т., Экспонг Г., ред. (1993). Нобелевские лекции по физике 1981–1990 гг . World Scientific Publishing Co Сингапур: Бибкод .: 1993nlp..book.....F .
- В 1887 году Бюист визуализировал один из крупнейших вирусов осповакцины с помощью оптической микроскопии после его окрашивания. В то время еще не было известно, что вакцина является вирусом. (Бюист Дж. Б. Вакциния и Вариола: исследование истории их жизни, Черчилль, Лондон)
- ^ Стэнли В.М., Лоринг Х.С. (январь 1936 г.). «Выделение кристаллического белка вируса мозаики табака из больных растений томата». Наука . 83 (2143): 85. Бибкод : 1936Sci....83...85S . дои : 10.1126/science.83.2143.85 . ПМИД 17756690 .
- ^ Стэнли В.М., Лауффер М.А. (апрель 1939 г.). «Распад вируса табачной мозаики в растворах мочевины». Наука . 89 (2311): 345–47. Бибкод : 1939Sci....89..345S . дои : 10.1126/science.89.2311.345 . ПМИД 17788438 .
- ^ Крегер А.Н., Морган Г.Дж. (июнь 2008 г.). «После двойной спирали: исследование Розалинды Франклин вируса табачной мозаики». Исида . 99 (2): 239–72. дои : 10.1086/588626 . ПМИД 18702397 . S2CID 25741967 .
- ^ Диммок с. 12
- ^ Норрби Э (2008). «Нобелевские премии и новая концепция вируса». Архив вирусологии . 153 (6): 1109–23. дои : 10.1007/s00705-008-0088-8 . ПМИД 18446425 . S2CID 10595263 .
- ^ Кольер с. 745
- ^ Темин Х.М., Балтимор Д. (1972). «РНК-направленный синтез ДНК и РНК-опухолевые вирусы». Достижения в области исследования вирусов . 17 : 129–86. дои : 10.1016/S0065-3527(08)60749-6 . ISBN 9780120398171 . ПМИД 4348509 .
- ^ Барре-Синусси Ф., Черманн Дж.К., Рей Ф., Нугейр М.Т., Шамаре С., Грюст Дж. и др. (май 1983 г.). «Выделение Т-лимфотропного ретровируса от пациента с риском развития синдрома приобретенного иммунодефицита (СПИД)». Наука . 220 (4599): 868–71. Бибкод : 1983Sci...220..868B . дои : 10.1126/science.6189183 . ПМИД 6189183 .
- ^ Чу К.Л., Куо Дж., Вайнер А.Дж., Оверби Л.Р., Брэдли Д.В., Хоутон М. (апрель 1989 г.). «Выделение клона кДНК, полученного из генома вирусного гепатита ни А, ни В, передающегося с кровью». Наука . 244 (4902): 359–62. Бибкод : 1989Sci...244..359C . CiteSeerX 10.1.1.469.3592 . дои : 10.1126/science.2523562 . ПМИД 2523562 .
- ^ Хоутон М. (ноябрь 2009 г.). «Долгий и извилистый путь, ведущий к идентификации вируса гепатита С» . Журнал гепатологии . 51 (5): 939–48. дои : 10.1016/j.jhep.2009.08.004 . ПМИД 19781804 .
- ↑ Перейти обратно: Перейти обратно: а б с д Пейн С. Методы изучения вирусов. Вирусы. 2017;37-52. doi:10.1016/B978-0-12-803109-4.00004-0
- ^ «Увеличение — микроскопия, размер и увеличение (CCEA) — GCSE Biology (Single Science) Revision — CCEA» . BBC Bitesize . Проверено 2 января 2023 г.
- ^ Бреннер С., Хорн Р.В. (июль 1959 г.). «Метод негативного окрашивания для электронной микроскопии вирусов с высоким разрешением». Биохимика и биофизика Acta . 34 : 103–10. дои : 10.1016/0006-3002(59)90237-9 . ПМИД 13804200 .
- ^ Голдсмит К.С., Миллер С.Е. (октябрь 2009 г.). «Современное использование электронной микроскопии для обнаружения вирусов» . Обзоры клинической микробиологии . 22 (4): 552–63. дои : 10.1128/CMR.00027-09 . ПМЦ 2772359 . ПМИД 19822888 .
- ^ Тивол В.Ф., Бригель А., Дженсен Г.Дж. (октябрь 2008 г.). «Улучшенный криоген для погружной заморозки» . Микроскопия и микроанализ . 14 (5): 375–379. Бибкод : 2008MiMic..14..375T . дои : 10.1017/S1431927608080781 . ISSN 1431-9276 . ПМК 3058946 . ПМИД 18793481 .
- ^ Ченг Ю., Григорьев Н., Пенчек П.А., Уолц Т. (апрель 2015 г.). «Букварь к одночастичной криоэлектронной микроскопии» . Клетка . 161 (3): 438–449. дои : 10.1016/j.cell.2015.03.050 . ПМЦ 4409659 . ПМИД 25910204 .
- ^ Стоддарт С. (1 марта 2022 г.). «Структурная биология: как белки оказались крупным планом» . Знающий журнал . doi : 10.1146/knowable-022822-1 . Проверено 25 марта 2022 г.
- ^ Лю Дж. З., Ричерсон К., Нельсон Р. С. (август 2009 г.). «Условия роста для исследований растений-вирусов-хозяев». Современные протоколы в микробиологии . Глава 16: Раздел 16A.1. дои : 10.1002/9780471729259.mc16a01s14 . ПМИД 19653216 . S2CID 41236532 .
- ^ Вальмонте-Кортес Г.Р., Лилли С.Т., Пирсон М.Н., Хиггинс С.М., МакДиармид Р.М. (январь 2022 г.). «Потенциал молекулярных индикаторов заражения вирусом растений: могут ли растения сообщить нам, что они заражены?» . Растения . 11 (2): 188. doi : 10.3390/plants11020188 . ПМЦ 8777591 . ПМИД 35050076 .
- ^ Gauger PC, Винсент А.Л. (2014). «Анализ нейтрализации сывороточного вируса для обнаружения и количественного определения сывороточно-нейтрализующих антител к вирусу гриппа у свиней». Вирус гриппа животных . Методы молекулярной биологии. Том. 1161. стр. 313–24. дои : 10.1007/978-1-4939-0758-8_26 . ISBN 978-1-4939-0757-1 . ПМИД 24899440 .
- ^ Димитрова К., Мендоса Э.Дж., Мюллер Н., Вуд Х. (2020). «Тест нейтрализации уменьшения бляшек для обнаружения ZIKV-специфичных антител». Вирус Зика . Методы молекулярной биологии. Том. 2142. стр. 59–71. дои : 10.1007/978-1-0716-0581-3_5 . ISBN 978-1-0716-0580-6 . ПМИД 32367358 . S2CID 218504421 .
- ^ Лампехо Т. (июль 2020 г.). «Грипп и противовирусная резистентность: обзор» . Европейский журнал клинической микробиологии и инфекционных заболеваний . 39 (7): 1201–1208. дои : 10.1007/s10096-020-03840-9 . ПМЦ 7223162 . ПМИД 32056049 .
- ^ Зайнол Рашид З., Отман С.Н., Абдул Самат М.Н., Али Великобритания, Вонг К.К. (апрель 2020 г.). «Диагностическая эффективность серологических анализов COVID-19». Малазийский журнал патологии . 42 (1): 13–21. ПМИД 32342927 .
- ^ Свак Н.С., Гаан Т.Ф., Хауслер В.Дж. (август 1992 г.). «Современное состояние теста фиксации комплемента в вирусной серодиагностике». Инфекционные агенты и болезни . 1 (4): 219–24. ПМИД 1365549 .
- ^ Смит Т.Дж. (август 2011 г.). «Структурные исследования по распознаванию и нейтрализации вирусов антителами» . Современное мнение в вирусологии . 1 (2): 150–6. дои : 10.1016/j.coviro.2011.05.020 . ПМЦ 3163491 . ПМИД 21887208 .
- ^ Махони Дж.Б., Петрич А., Смьея М. (2011). «Молекулярная диагностика респираторных вирусных инфекций». Критические обзоры клинических лабораторных наук . 48 (5–6): 217–49. дои : 10.3109/10408363.2011.640976 . ПМИД 22185616 . S2CID 24960083 .
- ^ АбуСалах М.А., Ган Ш., Аль-Хатамле М.А., Ирекеола А.А., Шуеб Р.Х., Йен Йан С. (март 2020 г.). «Последние достижения в диагностических подходах к вирусу Эпштейна-Барр» . Патогены . 9 (3): 226. doi : 10.3390/pathogens9030226 . ПМЦ 7157745 . ПМИД 32197545 .
- ^ Чжу Х, Чжан Х, Сюй Ю, Лашшакова С, Коравечна М, Нойжил П (октябрь 2020 г.). «ПЦР прошлое, настоящее и будущее» . БиоТехники . 69 (4): 317–325. дои : 10.2144/btn-2020-0057 . ПМЦ 7439763 . ПМИД 32815744 .
- ^ Ван X, Хун XZ, Ли YW, Ли Y, Ван Дж, Чен П, Лю БФ (март 2022 г.). «Стратегии молекулярной диагностики инфекционных заболеваний на основе микрофлюидики» . Военно-медицинские исследования . 9 (1): 11. дои : 10.1186/s40779-022-00374-3 . ПМК 8930194 . ПМИД 35300739 .
- ^ Бензигар М.Р., Бхаттачарджи Р., Бахарфар М., Лю Г. (апрель 2021 г.). «Современные методы диагностики коронавирусов человека: плюсы и минусы» . Аналитическая и биоаналитическая химия . 413 (9): 2311–2330. дои : 10.1007/s00216-020-03046-0 . ПМЦ 7679240 . ПМИД 33219449 .
- ^ Баррелл С.Дж., Ховард С.Р., Мерфи Ф.А. (01.01.2017), Баррелл С.Дж., Ховард С.Р., Мерфи Ф.А. (ред.), «Глава 10. Лабораторная диагностика вирусных заболеваний», Медицинская вирусология Феннера и Уайта (пятое издание) , Лондон: Academic Press, стр. 135–154, doi : 10.1016/b978-0-12-375156-0.00010-2 , ISBN. 978-0-12-375156-0 , ПМЦ 7149825
- ^ Кочула К.М., Галлотта А. (июнь 2016 г.). «Анализ латерального потока» . Очерки по биохимии . 60 (1): 111–20. дои : 10.1042/EBC20150012 . ПМЦ 4986465 . ПМИД 27365041 .
- ^ Ли MJ (октябрь 2021 г.). «Количественная оценка вирусной нагрузки SARS-CoV-2: текущее состояние и перспективы» . Экспертный обзор молекулярной диагностики . 21 (10): 1017–1023. дои : 10.1080/14737159.2021.1962709 . ПМЦ 8425446 . ПМИД 34369836 .
- ^ Мистри Б.А., Д'Орсонья М.Р., Чоу Т (июнь 2018 г.). «Влияние статистической множественности инфекции на количественное определение вируса и анализы инфекционности» . Биофизический журнал . 114 (12): 2974–2985. arXiv : 1805.02810 . Бибкод : 2018BpJ...114.2974M . дои : 10.1016/j.bpj.2018.05.005 . ПМК 6026352 . ПМИД 29925033 .
- ^ Кашуба С, Сюй С, Крогстад А, Франклин С (январь 2005 г.). «Вирусология мелких млекопитающих» . Ветеринарные клиники Северной Америки. Практика с экзотическими животными . 8 (1): 107–22. дои : 10.1016/j.cvex.2004.09.004 . ПМК 7110861 . ПМИД 15585191 .
- ^ Катлер Т.Д., Ван С., Хофф С.Дж., Киттаворнрат А., Циммерман Дж.Дж. (август 2011 г.). «Средняя инфекционная доза (ID 50 ) изолята вируса репродуктивного и респираторного синдрома свиней MN-184 при воздействии аэрозоля». Ветеринарная микробиология . 151 (3–4): 229–37. дои : 10.1016/j.vetmic.2011.03.003 . ПМИД 21474258 .
- ^ Мун К., Чо Дж.К. (март 2021 г.). «Метавиромика в сочетании с идентификацией фага-хозяина открывает вирусный «черный ящик» ». Журнал микробиологии (Сеул, Корея) . 59 (3): 311–323. дои : 10.1007/s12275-021-1016-9 . ПМИД 33624268 . S2CID 232023531 .
- ^ Сальгадо Э.Н., Упадьяюла С., Харрисон С.С. (сентябрь 2017 г.). «Одночастичное обнаружение транскрипции после проникновения ротавируса» . Журнал вирусологии . 91 (18). дои : 10.1128/JVI.00651-17 . ПМЦ 5571246 . ПМИД 28701394 .
- ^ Ёкота И., Хаттори Т., Шейн П.Ю., Конно С., Нагасака А., Такэябу К., Фудзисава С., Нисида М., Тешима Т. (февраль 2021 г.). «Эквивалентная вирусная нагрузка SARS-CoV-2 по данным ПЦР между мазками из носоглотки и слюной у пациентов с симптомами» . Научные отчеты . 11 (1): 4500. Бибкод : 2021NatSR..11.4500Y . дои : 10.1038/s41598-021-84059-2 . ПМК 7904914 . ПМИД 33627730 .
- ^ Николс Б.Е., Гирдвуд С.Дж., Кромптон Т., Стюарт-Ишервуд Л., Берри Л., Чимхамхива Д., Мойо С., Кюнле Дж., Стивенс В., Розен С. (сентябрь 2019 г.). «Мониторинг вирусной нагрузки на последней миле: сколько это будет стоить?» . Журнал Международного общества по СПИДу . 22 (9): e25337. дои : 10.1002/jia2.25337 . ПМК 6742838 . ПМИД 31515967 .
- ^ Ширима Р.Р., Маэда Д.Г., Кандзю Э., Сезар Дж., Тибазарва Ф.И., Легг Дж.П. (июль 2017 г.). «Абсолютное количественное определение мРНК вируса коричневой полоски маниоки с помощью кПЦР в реальном времени» . Журнал вирусологических методов . 245 : 5–13. дои : 10.1016/j.jviromet.2017.03.003 . ПМЦ 5429390 . ПМИД 28315718 .
- ^ Рубио Л., Галипиенсо Л., Ферриоль И. (2020). «Обнаружение вирусов растений и борьба с болезнями: актуальность генетического разнообразия и эволюции» . Границы в науке о растениях . 11 : 1092. дои : 10.3389/fpls.2020.01092 . ПМК 7380168 . ПМИД 32765569 .
- ↑ Перейти обратно: Перейти обратно: а б Beards GM (август 1982 г.). «Способ очистки ротавирусов и аденовирусов из фекалий». Журнал вирусологических методов . 4 (6): 343–52. дои : 10.1016/0166-0934(82)90059-3 . ПМИД 6290520 .
- ^ Чжоу Ю, Макнамара Р.П., Диттмер Д.П. (август 2020 г.). «Методы очистки и наличие РНК в вирусных частицах и внеклеточных везикулах» . Вирусы . 12 (9): 917. дои : 10.3390/v12090917 . ПМЦ 7552034 . ПМИД 32825599 .
- ^ Су Ц, Сена-Эстевес М, Гао Дж (май 2019 г.). «Очистка рекомбинантного аденовируса градиентным центрифугированием хлорида цезия». Протоколы Колд-Спринг-Харбора . 2019 (5): pdb.prot095547. дои : 10.1101/pdb.prot095547 . ПМИД 31043560 . S2CID 143423942 .
- ^ Клепарник К., Бочек П. (март 2010 г.). «Электрофорез сегодня и завтра: помогаем мечтам биологов сбыться». Биоэссе . 32 (3): 218–226. doi : 10.1002/bies.200900152 . ПМИД 20127703 . S2CID 41587013 .
- ↑ Перейти обратно: Перейти обратно: а б Кастро К., Марине Р., Рамос Э., Нг ТФ (22 июня 2020 г.). «Влияние вариантной интерференции на сборку de novo для глубокого секвенирования вирусов» . БМК Геномика . 21 (1): 421. doi : 10.1186/s12864-020-06801-w . ПМЦ 7306937 . ПМИД 32571214 .
- ^ Цуй Дж., Ли Ф., Ши З.Л. (март 2019 г.). «Происхождение и эволюция патогенных коронавирусов» . Обзоры природы. Микробиология . 17 (3): 181–192. дои : 10.1038/s41579-018-0118-9 . ПМК 7097006 . ПМИД 30531947 .
- ^ Горбаленя А.Е., Лаубер К. Филогения вирусов. Справочный модуль по биомедицинским наукам. 2017;Б978-0-12-801238-3.95723-4. doi:10.1016/B978-0-12-801238-3.95723-4
- ^ Кох Л. (июль 2020 г.). «Платформа для клонирования РНК-вирусов» . Обзоры природы. Генетика . 21 (7): 388. doi : 10.1038/s41576-020-0246-8 . ПМК 7220607 . ПМИД 32404960 .
- ^ Тхи Нху Тао Т, Лабруса Ф, Эберт Н, В'ковски П, Сталдер Х, Портманн Дж, Келли Дж, Штайнер С, Холверда М, Крацель А, Гултом М, Шмид К, Лалоли Л, Хюссер Л, Уайдер М, Пфаендер С., Хирт Д., Сиппа В., Креспо-Помар С., Шредер С., Мут Д., Нимейер Д., Корман В.М., Мюллер М.А., Дростен С., Дейкман Р., Хорес Дж., Тиль В. (июнь 2020 г.). «Быстрая реконструкция SARS-CoV-2 с использованием платформы синтетической геномики» . Природа . 582 (7813): 561–565. Бибкод : 2020Natur.582..561T . дои : 10.1038/s41586-020-2294-9 . ПМИД 32365353 . S2CID 213516085 .
- ^ Розано Г.Л., Моралес Э.С., Чеккарелли Э.А. (август 2019 г.). «Новые инструменты для производства рекомбинантного белка в Escherichia coli: обновление за 5 лет» . Белковая наука . 28 (8): 1412–1422. дои : 10.1002/pro.3668 . ПМК 6635841 . ПМИД 31219641 .
- ^ Пеннацио С (2006). «Происхождение фаговой вирусологии». Ривиста ди Биология . 99 (1): 103–29. ПМИД 16791793 .
- ^ Харада Л.К., Силва Э.К., Кампос В.Ф., Дель Фиол Ф.С., Вила М., Домбровска К., Крылов В.Н., Балкан В.М. (2018). «Биотехнологическое применение бактериофагов: современное состояние» . Микробиологические исследования . 212–213: 38–58. дои : 10.1016/j.micres.2018.04.007 . hdl : 1822/54758 . ПМИД 29853167 . S2CID 46921731 .
- ↑ Перейти обратно: Перейти обратно: а б Стоун Э., Кэмпбелл К., Грант И., Маколифф О. (июнь 2019 г.). «Понимание и использование взаимодействий фаг-хозяин» . Вирусы . 11 (6): 567. дои : 10.3390/v11060567 . ПМК 6630733 . ПМИД 31216787 .
- ^ Нагано К., Цуцуми Ю (январь 2021 г.). «Технология фагового дисплея как мощная платформа для открытия лекарств на основе антител» . Вирусы . 13 (2): 178. дои : 10.3390/v13020178 . ПМЦ 7912188 . ПМИД 33504115 .
- ^ Ибрагим Б., МакМахон Д.П., Хуфски Ф., Бир М., Денг Л., Мерсье П.Л., Пальмарини М., Тиль В., Марц М. (июнь 2018 г.). «Новая эра вирусной биоинформатики» . Вирусные исследования . 251 : 86–90. doi : 10.1016/j.virusres.2018.05.009 . ПМИД 29751021 . S2CID 21736957 .
- ^ Бэмфорд Д., Цукерман Массачусетс (2021). Энциклопедия вирусологии . Амстердам. ISBN 978-0-12-814516-6 . OCLC 1240584737 .
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) - ^ Макдональд С.М., Нельсон М.И., Тернер П.Е., Паттон Дж.Т. (июль 2016 г.). «Реассортация сегментированных РНК-вирусов: механизмы и результаты» . Обзоры природы. Микробиология . 14 (7): 448–60. дои : 10.1038/nrmicro.2016.46 . ПМК 5119462 . ПМИД 27211789 .
- ^ Ли Дж., Аревало М.Т., Цзэн М. (2013). «Инженерные векторы вируса гриппа» . Биоинженерия . 4 (1): 9–14. дои : 10.4161/bioe.21950 . ПМК 3566024 . ПМИД 22922205 .
- ^ Ли CW (2014). «Обратная генетика вируса гриппа». Вирус гриппа животных . Методы молекулярной биологии. Том. 1161. стр. 37–50. дои : 10.1007/978-1-4939-0758-8_4 . ISBN 978-1-4939-0757-1 . ПМИД 24899418 .
- ^ Ли З, Чжун Л, Хэ Дж, Хуан Ю, Чжао Ю (апрель 2021 г.). «Разработка и применение обратной генетической технологии вируса гриппа» . Гены вирусов . 57 (2): 151–163. дои : 10.1007/s11262-020-01822-9 . ПМЦ 7851324 . ПМИД 33528730 .
- ^ Халл Р., Рима Б (ноябрь 2020 г.). «Таксономия и классификация вирусов: наименование видов вирусов» . Архив вирусологии . 165 (11): 2733–2736. дои : 10.1007/s00705-020-04748-7 . ПМИД 32740831 . S2CID 220907379 .
- ^ Пеллетт П.Е., Митра С., Голландия Т.К. (2014). «Основы вирусологии». Нейровирусология . Справочник по клинической неврологии. Том. 123. стр. 45–66. дои : 10.1016/B978-0-444-53488-0.00002-X . ISBN 9780444534880 . ПМЦ 7152233 . ПМИД 25015480 .
- ^ Симмондс П., Айевсакун П. (август 2018 г.). «Классификация вирусов – где провести черту?» . Архив вирусологии . 163 (8): 2037–2046. дои : 10.1007/s00705-018-3938-z . ПМК 6096723 . ПМИД 30039318 .
- ^ Львофф А., Хорн Р.В., Турнье П. (июнь 1962 г.). «[Вирусная система]». Еженедельные отчеты сессий Академии наук (на французском языке). 254 :4225–27. ПМИД 14467544 .
- ^ Львофф А., Хорн Р., Турнье П. (1962). «Система вирусов». Симпозиумы Колд-Спринг-Харбор по количественной биологии . 27 : 51–55. дои : 10.1101/sqb.1962.027.001.008 . ПМИД 13931895 .
- ^ Фоке СМ, Фаржетт Д (август 2005 г.). «Международный комитет по таксономии вирусов и 3142 неустановленных видов» . Вирусологический журнал . 2:64 . дои : 10.1186/1743-422X-2-64 . ПМК 1208960 . ПМИД 16105179 .
- ^ Исполнительный комитет Международного комитета по таксономии вирусов (май 2020 г.). «Новая сфера таксономии вирусов: разделение виросферы на 15 иерархических рангов» . Нат Микробиол . 5 (5): 668–674. дои : 10.1038/s41564-020-0709-x . ПМК 7186216 . ПМИД 32341570 .
- ^ Хан МК, Алам ММ (июль 2021 г.). «Вспышки норовирусного гастроэнтерита, геномное разнообразие и эволюция: обзор». Медицинский журнал Майменсингха . 30 (3): 863–873. ПМИД 34226482 .
- ^ Эберле Дж., Гюртлер Л. (2012). «Типы, группы, подтипы и рекомбинантные формы ВИЧ: ошибки репликации, давление отбора и квазивиды» . Интервирусология . 55 (2): 79–83. дои : 10.1159/000331993 . ПМИД 22286874 . S2CID 5642060 .
- ^ Делварт Э.Л. (2007). «Вирусная метагеномика» . Обзоры по медицинской вирусологии . 17 (2): 115–31. дои : 10.1002/rmv.532 . ПМК 7169062 . ПМИД 17295196 .
- ↑ Перейти обратно: Перейти обратно: а б «Таксономия вирусов: выпуск 2021 г.» . talk.ictvonline.org . Международный комитет по таксономии вирусов . Проверено 4 апреля 2022 г.
- ^ Кунин Е.В., Крупович М., Агол В.И. (август 2021 г.). «Балтиморская классификация вирусов 50 лет спустя: как она выглядит в свете эволюции вирусов?» (PDF) . Обзоры микробиологии и молекулярной биологии . 85 (3): e0005321. дои : 10.1128/MMBR.00053-21 . ПМЦ 8483701 . ПМИД 34259570 . S2CID 235821748 .
Библиография [ править ]
- Коллиер Л., Балоуз А., Сассман М. (1998). Мэхи Б., Коллиер Л.А. (ред.). Микробиология и микробные инфекции Топли и Уилсона . Вирусология. Том. 1 (Девятое изд.). ISBN 0-340-66316-2 .
- Диммок, Нью-Джерси, Истон А.Дж., Леппард К. (2007). Введение в современную вирусологию (Шестое изд.). Издательство Блэквелл. ISBN 978-1-4051-3645-7 .
- Шорс Т (2017). Понимание вирусов . Издательство Джонс и Бартлетт. ISBN 978-1-284-02592-7 .
Внешние ссылки [ править ]
 СМИ, связанные с вирусологией, на Викискладе?
СМИ, связанные с вирусологией, на Викискладе? - Официальный сайт Международного комитета по таксономии вирусов
