Остаточный индекс карбоната натрия
этой статьи Фактическая точность оспаривается . ( Октябрь 2019 г. ) |
Индекс остаточного карбоната натрия (RSC) оросительной воды или почвенной воды используется для обозначения опасности щелочности почвы. Индекс RSC используется для определения пригодности воды для орошения глинистых . почв с высокой катионообменной способностью Когда растворенного натрия в воде больше, чем растворенного кальция и магния, глинистая почва набухает или подвергается диспергированию , что резко снижает ее инфильтрационную способность . [1]
В рассеянном [ нужны разъяснения ] структура почвы , корни растений не могут проникнуть глубже в почву из-за недостатка влаги. Однако вода с высоким индексом RSC не увеличивает осмотическое давление и не препятствует захвату воды корнями растений, в отличие от воды с высокой соленостью . Орошение глинистых почв водой с высоким индексом RSC приводит к образованию залежных солончаков . [2] [3] [4]

Формула индекса RSC
[ редактировать ]RSC выражается в единицах мэкв/л . RSC не должен быть выше 1 и предпочтительно меньше +0,5 для учета использования воды для орошения. [5] Формула расчета индекса RSC:
- Индекс RSC = [HCO 3 + CO 3 ] − [Ca + Mg]
- Индекс RSC = HCO 3/61 + CO 3/30 – Ca/20 – Mg/12 (в случае, если концентрации ионов измеряются в мг/л или ppm в виде солей)
При расчете индекса RSC следует учитывать качество воды, присутствующей в корневой зоне культуры, с учетом фактора выщелачивания в поле. [6] На кальций, присутствующий в растворенной форме, также влияет парциальное давление растворенного CO 2 в корневой зоне растений в полевой воде. [7]
Природное загрязнение воды
[ редактировать ]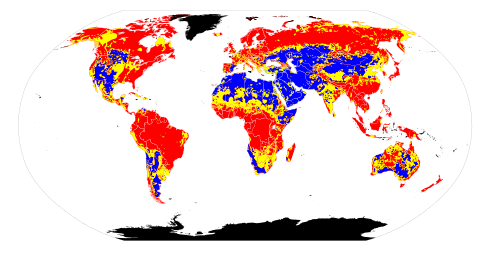
Кальцинированная сода [Na 2 CO 3 ] может присутствовать в природной воде в результате выветривания базальта , который является магматической породой. Известь [Ca(OH) 2 ] может присутствовать в природной воде, когда дождевая вода вступает в контакт с обожженными минералами, такими как зола, образующаяся при сжигании известкового угля или бурого угля в котлах. Антропогенное использование кальцинированной соды также приводит к окончательному увеличению РСК речной воды.
Там, где речные и подземные воды неоднократно используются в интенсивно орошаемых речных бассейнах, речная вода, доступная в низовьях, часто оказывается непригодной для сельского хозяйства из-за высокого индекса RSC или щелочности. [8] Соленость воды не обязательно должна быть высокой.
Смягченная вода
[ редактировать ]В терминологии промышленной очистки воды качество воды с высоким индексом RSC является синонимом мягкой воды , но химически сильно отличается от естественно мягкой воды, которая имеет очень низкую концентрацию ионов. [9] Когда соли кальция и магния присутствуют в воде в растворенной форме, эти соли осаждаются на поверхностях теплопередачи, образуя изолирующие твердые накипи/покрытия, которые снижают эффективность теплопередачи теплообменников. Чтобы избежать образования накипи в теплообменниках с водяным охлаждением, воду обрабатывают известью или кальцинированной содой для устранения жесткости воды .
происходят следующие химические реакции, В процессе умягчения известковой содой в результате которых осаждаются соли кальция и магния в виде карбоната кальция и гидроксида магния, которые имеют очень низкую растворимость в воде.
- CaSO 4 + Na 2 CO 3 ---> CaCO 3 ↓ + Na 2 SO 4
- CaCl 2 + Na 2 CO 3 ---> CaCO 3 ↓ + 2NaCl
- MgSO 4 + Ca(OH) 2 + Na 2 CO 3 ---> Mg(OH) 2 ↓ + CaCO 3 ↓ + Na 2 SO 4
- MgCl 2 + Ca(OH) 2 + Na 2 CO 3 ---> Mg(OH) 2 ↓ + CaCO 3 ↓ + 2NaCl
- 2NaHCO 3 + Ca(OH) 2 ---> CaCO 3 ↓ + Na 2 CO 3 + 2H 2 O
- Na 2 CO 3 + Ca(OH) 2 ---> CaCO 3 ↓ + 2NaOH
- Ca(HCO 3 ) 2 + Ca(OH) 2 ---> 2CaCO 3 ↓ + 2H 2 O
- Mg(HCO 3 ) 2 + 2Ca(OH) 2 ---> Mg(OH) 2 ↓ + 2CaCO 3 ↓ + 2H 2 O
- MgCO 3 + Ca(OH) 2 ---> Mg(OH) 2 ↓ + CaCO 3 ↓
Избыток кальцинированной соды после осаждения солей кальция и магния находится в виде карбонатов и бикарбонатов натрия, что придает высокий pH или щелочность почвенной воде .
Содовые озера
[ редактировать ]Озера бессточной котловины называются содовыми или щелочными, если притоки воды содержат высокие концентрации Na 2 CO 3 . pH воды содового озера обычно превышает 9, а иногда соленость близка к солоноватой воде из-за истощения чистой воды из-за солнечного испарения.
Содовые озера богаты водорослями из-за повышенного содержания растворенного CO 2 в озерной воде по сравнению с озерами с пресной или соленой водой. Карбонат натрия и гидроксид натрия находятся в равновесии с наличием растворенного диоксида углерода, как показано ниже в химической реакции.
- Na 2 CO 3 + H 2 O <=> 2NaOH + CO 2
- NaHCO 3 <=> NaOH + CO 2
В дневное время, когда доступен солнечный свет, водоросли подвергаются фотосинтеза процессу , который поглощает CO 2 , смещая реакцию в сторону образования NaOH, и наоборот, в ночное время происходит высвобождение CO 2 в процессе дыхания водорослей в сторону Na 2 CO 3 и NaHCO3 Образование . В водах содовых озер карбонаты натрия действуют как катализатор роста водорослей, обеспечивая благоприятную более высокую концентрацию растворенного CO 2 в дневное время. Из-за колебаний содержания растворенного CO 2 pH и щелочность воды также продолжают меняться. [10]
.
См. также
[ редактировать ]- pH почвы
- Воздействие орошения на окружающую среду
- Указатель статей о почве
- Агрети зеленый овощ
- Водорослевое топливо
- Альгакультура
- Гравитропизм
Ссылки
[ редактировать ]- ^ Управление качеством оросительной воды, Университет штата Орегон, США , Проверено 4 октября 2012 г.
- ^ «Оценка риска засоления для региона Квинсленд Мюррей-Дарлинг (см. Приложение 2), Департамент окружающей среды и управления ресурсами Квинсленда» (PDF) . Архивировано из оригинала (PDF) 10 апреля 2013 года . Проверено 29 октября 2012 г.
- ^ И.П. Аброл, Ж.С.П. Ядав и Ф.И. Массуд. «Засоленные почвы и обращение с ними, см. пункт 4.7» . Проверено 23 декабря 2012 г.
- ^ Фарук Ахмад. «Выращивание травы Карнал / Каллар на солонно-щелочных почвах в Пакистане» (PDF) . Проверено 22 января 2013 г.
- ^ Справочник лаборатории солености США 60
- ^ «Справочник по управлению соленостью, Качество воды, стр. 85» (PDF) . Проверено 5 октября 2012 г. [ постоянная мертвая ссылка ]
- ^ «Фиторемедиация натриевых и солончаково-натриевых почв» (PDF) . Проверено 23 июля 2013 г.
- ^ Дж. Келлер, А. Келлер и Г. Дэвидс. «Этапы развития речного бассейна и последствия закрытия» (PDF) . Проверено 25 августа 2012 г.
- ^ «Умягчение осадков, GE Power & Water» . Проверено 11 октября 2012 г.
- ^ Электроэнергия и вода GE. «Водахимия. Справочник по промышленной водоподготовке» . Проверено 4 января 2014 г.