Виртуальный показ
Виртуальный скрининг ( VS ) – это вычислительный метод, используемый при открытии лекарств для поиска библиотек малых молекул с целью идентификации тех структур, которые с наибольшей вероятностью связываются с мишенью лекарства , обычно с белковым рецептором или ферментом . [2] [3]
Виртуальный скрининг определяется как «автоматическая оценка очень больших библиотек соединений» с использованием компьютерных программ. [4] Как следует из этого определения, VS в основном представляла собой игру с числами, в которой основное внимание уделялось тому, как огромное химическое пространство , насчитывающее более 10 60 мыслимые соединения [5] могут быть отфильтрованы до управляемого числа, которое можно синтезировать, приобрести и протестировать. Хотя поиск во всей химической вселенной может быть теоретически интересной проблемой, более практичные сценарии VS сосредоточены на разработке и оптимизации целевых комбинаторных библиотек и пополнении библиотек доступных соединений из собственных хранилищ соединений или предложений поставщиков. Поскольку точность метода возросла, виртуальный скрининг стал неотъемлемой частью процесса открытия лекарств . [6] [1] Виртуальный скрининг можно использовать для выбора соединений из собственной базы данных для скрининга, выбора соединений, которые можно приобрести на стороне, и выбора соединения, которое следует синтезировать следующим.
Методы
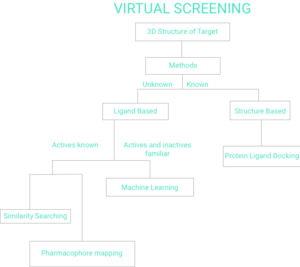
[ редактировать ]Существует две широкие категории методов скрининга: на основе лигандов и на основе структуры. [7] Оставшаяся часть этой страницы будет отражать рисунок 1. Блок-схема виртуального скрининга.
Лигандные методы
[ редактировать ]Учитывая набор структурно разнообразных лигандов , которые связываются с рецептором , модель рецептора может быть построена путем использования коллективной информации, содержащейся в таком наборе лигандов. Различные вычислительные методы исследуют структурные, электронные, молекулярные формы и физико-химические сходства различных лигандов, что может указывать на их способ действия на определенный молекулярный рецептор или клеточные линии. [8] Затем кандидатный лиганд можно сравнить с моделью фармакофора, чтобы определить, совместим ли он с ней и, следовательно, может ли он связываться. [9] Различные методы двумерного анализа химического сходства [10] были использованы для сканирования баз данных для поиска активных лигандов. Другой популярный подход, используемый в виртуальном скрининге на основе лигандов, заключается в поиске молекул, форма которых аналогична форме известных активных веществ, поскольку такие молекулы подходят к сайту связывания мишени и, следовательно, с большой вероятностью связывают мишень. В литературе имеется ряд перспективных применений этого класса методов. [11] [12] [13] Фармакофорные расширения этих 3D-методов также свободно доступны в виде веб-серверов. [14] [15] Также значительную популярность приобрел виртуальный скрининг на основе формы. [16]
Структурные методы
[ редактировать ]Подход виртуального скрининга на основе структуры включает в себя различные вычислительные методы, которые учитывают структуру рецептора, который является молекулярной мишенью исследуемых активных лигандов. Некоторые из этих методов включают молекулярную стыковку , предсказание фармакофора на основе структуры и моделирование молекулярной динамики. [17] [18] [8] Молекулярный докинг — это наиболее часто используемый метод, основанный на структурировании, и он применяет оценочную функцию для оценки приспособленности каждого лиганда к участку связывания макромолекулярного рецептора, помогая выбрать лиганды с наиболее высоким сродством. [19] [20] [21] В настоящее время существует несколько веб-серверов, ориентированных на перспективный виртуальный скрининг. [22] [23]
Гибридные методы
[ редактировать ]Гибридные методы, основанные на структурном сходстве и сходстве лигандов, также были разработаны для преодоления ограничений традиционных подходов VLS. Эта методология использует основанную на эволюции информацию о связывании лигандов для прогнозирования низкомолекулярных связующих веществ. [24] [25] и может использовать как глобальное структурное сходство, так и карманное сходство. [24] Подход, основанный на глобальном структурном сходстве, использует как экспериментальную структуру, так и предсказанную модель белка для обнаружения структурного сходства с белками в библиотеке голо-шаблонов PDB. При обнаружении значительного структурного сходства метрика коэффициента Танимото на основе двумерного отпечатка пальца применяется для скрининга малых молекул, которые похожи на лиганды, извлеченные из выбранных шаблонов голографической PDB. [26] [27] Прогнозы этого метода были экспериментально оценены и показывают хорошие результаты в идентификации активных малых молекул.
Указанный выше метод зависит от глобального структурного сходства и не позволяет априори выбрать конкретный сайт связывания лиганда в интересующем белке. Кроме того, поскольку методы основаны на двумерной оценке сходства лигандов, они не способны распознавать стереохимическое сходство малых молекул, которые существенно различаются, но демонстрируют сходство геометрической формы. Чтобы решить эти проблемы, был разработан и экспериментально оценен новый подход, ориентированный на карманы, PoLi, способный нацеливаться на специфические карманы связывания в матрицах голо-белков.
Вычислительная инфраструктура
[ редактировать ]Вычисление парных взаимодействий между атомами, которое является необходимым условием для работы многих программ виртуального скрининга, масштабируется за счет , N — число атомов в системе. Из-за квадратичного масштабирования вычислительные затраты быстро возрастают.
Лигандный подход
[ редактировать ]Методы на основе лигандов обычно требуют доли секунды для одной операции сравнения структур. Иногда одного процессора достаточно, чтобы выполнить большой скрининг за несколько часов. Однако несколько сравнений можно проводить параллельно, чтобы ускорить обработку большой базы данных соединений.
Структурный подход
[ редактировать ]Размер задачи требует параллельных вычислений инфраструктуры , такой как кластер систем Linux , на котором работает процессор пакетной очереди для обработки работы, например Sun Grid Engine или Torque PBS.
Необходимы средства обработки входных данных из больших библиотек соединений. Для этого требуется некая составная база данных, к которой может обращаться параллельный кластер, доставляя соединения параллельно различным вычислительным узлам. Коммерческие базы данных могут быть слишком громоздкими, и лучшим выбором может быть высокоскоростная система индексирования, такая как Berkeley DB . Кроме того, может быть неэффективно выполнять одно сравнение для каждого задания, поскольку время разгона узлов кластера может легко превысить объем полезной работы. Чтобы обойти эту проблему, необходимо обрабатывать пакеты соединений в каждом задании кластера, объединяя результаты в некий файл журнала. Вторичный процесс для анализа файлов журналов и извлечения кандидатов с высокими оценками может быть запущен после завершения всего эксперимента.
Точность
[ редактировать ]Целью виртуального скрининга является идентификация молекул новой химической структуры, которые связываются с интересующей макромолекулярной мишенью . Таким образом, успех виртуального экрана определяется поиском новых интересных каркасов, а не общим количеством просмотров. Поэтому к интерпретации точности виртуального скрининга следует относиться с осторожностью. Низкая результативность интересных каркасов явно предпочтительнее высокой результативности уже известных каркасов.
Большинство тестов виртуальных скрининговых исследований в литературе являются ретроспективными. В этих исследованиях эффективность метода VS измеряется его способностью извлекать небольшой набор ранее известных молекул, обладающих сродством к интересующей мишени (активные молекулы или просто активные вещества) из библиотеки, содержащей гораздо более высокую долю предполагаемых неактивных или просто активных веществ. приманки. Существует несколько различных способов выбора ловушек путем сопоставления свойств соответствующей активной молекулы. [28] и в последнее время приманки также выбираются не имеющим себе равных способом. [29] Также обсуждалось фактическое влияние выбора приманки для целей обучения или тестирования. [29] [30]
Напротив, в перспективных приложениях виртуального скрининга полученные результаты подлежат экспериментальному подтверждению (например, измерения IC 50 ). Существует консенсус в отношении того, что ретроспективные тесты не являются хорошими предикторами предполагаемых результатов, и, следовательно, только проспективные исследования представляют собой убедительное доказательство пригодности метода для конкретной цели. [31] [32] [33] [34] [35]
Приложение к открытию лекарств
[ редактировать ]Виртуальный скрининг — очень полезное приложение, когда дело доходит до идентификации молекул, что является началом медицинской химии. Поскольку подход виртуального скрининга становится все более важным и существенным методом в медицинской химической промышленности, этот подход получил быстрое распространение. [36]
Лигандные методы
[ редактировать ]Не зная структуры, пытаются предсказать, как лиганды будут связываться с рецептором. С использованием фармакофорных свойств каждого лиганда идентифицируются донор и акцептор. Приравнивающие признаки накладываются, однако маловероятно, что существует единственное правильное решение. [1]
Фармакофорные модели
[ редактировать ]Этот метод используется при объединении результатов поиска с использованием непохожих эталонных соединений, одинаковых дескрипторов и коэффициентов, но разных активных соединений. Этот метод выгоден, поскольку он более эффективен, чем просто использование одной эталонной структуры, а также обеспечивает наиболее точную производительность, когда речь идет о различных активных объектах. [1]
Фармакофор представляет собой совокупность стерических и электронных свойств, которые необходимы для оптимального супрамолекулярного взаимодействия или взаимодействия с биологической целевой структурой, чтобы ускорить ее биологический ответ. Выберите представителя в качестве набора активов, большинство методов будут искать похожие привязки. [37] Предпочтительно иметь несколько жестких молекул, а лиганды должны быть разнообразными, другими словами, обеспечить наличие различных свойств, которые не проявляются во время фазы связывания. [1]
Виртуальный скрининг на основе формы
[ редактировать ]Подходы, основанные на молекулярном сходстве формы, признаны важными и популярными методами виртуального скрининга. В настоящее время высокооптимизированная платформа для скрининга ROCS (Rapid Overlay of Chemical Structures) считается де-факто отраслевым стандартом для виртуального скрининга на основе формы и лиганд-центризма. [38] [39] [40] Он использует функцию Гаусса для определения молекулярных объемов небольших органических молекул. Выбор конформации запроса менее важен, что делает скрининг на основе формы идеальным для моделирования на основе лигандов: поскольку наличие биоактивной конформации для запроса не является ограничивающим фактором для скрининга — это скорее выбор соединения(й) запроса. ), что имеет решающее значение для проверки эффективности. [16]
Виртуальный скрининг на местах
[ редактировать ]В качестве усовершенствования методов сходства, основанных на форме, методы на основе полей пытаются принять во внимание все поля, которые влияют на взаимодействие лиганд-рецептор, не учитывая при этом химическую структуру, используемую в качестве запроса. Примерами других полей, которые используются в этих методах, являются электростатические или гидрофобные поля.
Взаимосвязь количественной структуры и активности
[ редактировать ]Модели взаимосвязи количественной структуры и активности (QSAR) состоят из прогнозных моделей, основанных на информации, извлеченной из набора известных активных и известных неактивных соединений. [41] SAR (отношения «структура-активность»), где данные обрабатываются качественно и могут использоваться со структурными классами и более чем одним режимом привязки. Модели отдают приоритет соединениям для открытия свинца. [1]
Алгоритмы машинного обучения
[ редактировать ]Алгоритмы машинного обучения широко используются в подходах виртуального скрининга. В методах контролируемого обучения используются обучающие и тестовые наборы данных, состоящие из известных активных и известных неактивных соединений. Различные алгоритмы машинного обучения успешно применяются в стратегиях виртуального скрининга, таких как рекурсивное разделение, машины опорных векторов , случайный лес, k-ближайшие соседи и нейронные сети . [42] [43] [44] Эти модели определяют вероятность того, что соединение является активным, а затем ранжируют каждое соединение на основе его вероятности. [1]
Субструктурный анализ в машинном обучении
[ редактировать ]Первой моделью машинного обучения, используемой для больших наборов данных, является анализ подструктуры, созданный в 1973 году. Каждый фрагмент подструктуры вносит непрерывный вклад в деятельность определенного типа. [1] Субструктура — это метод, который преодолевает трудности огромной размерности, когда дело доходит до анализа структур при разработке лекарств. Эффективный анализ подконструкции используется для конструкций, похожих на многоуровневое здание или башню. Геометрия используется для нумерации граничных швов данной структуры в начале и к кульминации. При разработке метода специальной статической конденсации и процедур замены этот метод оказался более продуктивным, чем предыдущие модели анализа основания. [45]
Рекурсивное секционирование
[ редактировать ]Рекурсивное секционирование — это метод, который создает дерево решений с использованием качественных данных. Понимание того, как правила разбивают классы с низкой ошибкой неправильной классификации при повторении каждого шага до тех пор, пока не будет найдено разумное разделение. Однако рекурсивное секционирование может иметь плохую способность прогнозирования, потенциально создавая точные модели с той же скоростью. [1]
Структурно-ориентированные методы известного докинга белков-лигандов
[ редактировать ]Лиганд может связываться с активным сайтом внутри белка с помощью алгоритма поиска стыковки и функции оценки, чтобы определить наиболее вероятную причину для отдельного лиганда при назначении порядка приоритета. [1] [46]
См. также
[ редактировать ]- Грид-вычисления
- Высокопроизводительный скрининг
- Стыковка (молекулярная)
- Ретро-показ
- Функции оценки
- База данных ЦИНК
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я дж Жилле V (2013). «Виртуальный скрининг на основе лигандов и структур» (PDF) . Университет Шеффилда.
- ^ Рестер У (июль 2008 г.). «От виртуальности к реальности - Виртуальный скрининг при обнаружении и оптимизации свинцов: взгляд на медицинскую химию». Текущее мнение об открытии и разработке лекарств . 11 (4): 559–68. ПМИД 18600572 .
- ^ Роллингер Дж. М., Ступпнер Х., Лангер Т. (2008). «Виртуальный скрининг на обнаружение биологически активных натуральных продуктов». Том I. Природные соединения как лекарства . Прогресс в исследованиях лекарств. Том. 65. С. 211, 213–49. дои : 10.1007/978-3-7643-8117-2_6 . ISBN 978-3-7643-8098-4 . ПМК 7124045 . ПМИД 18084917 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Уолтерс В.П., Шталь М.Т., Мурко М.А. (1998). «Виртуальный показ – обзор». Препарат Дисков. Сегодня . 3 (4): 160–178. дои : 10.1016/S1359-6446(97)01163-X .
- ^ Бохачек Р.С., МакМартин С., Гуида В.К. (1996). «Искусство и практика разработки лекарств на основе структуры: взгляд на молекулярное моделирование». Мед. Рез. Преподобный . 16 (1): 3–50. doi : 10.1002/(SICI)1098-1128(199601)16:1<3::AID-MED1>3.0.CO;2-6 . ПМИД 8788213 .
- ^ МакГрегор MJ, Ло Цзи, Цзян Икс (11 июня 2007 г.). «Глава 3: Виртуальный скрининг при открытии лекарств». В Хуан Цзы (ред.). Исследование открытия лекарств. Новые рубежи постгеномной эры . Wiley-VCH: Вайнхайм, Германия. стр. 63–88. ISBN 978-0-471-67200-5 .
- ^ Макиннес С. (октябрь 2007 г.). «Стратегии виртуального скрининга при открытии лекарств». Современное мнение в области химической биологии . 11 (5): 494–502. дои : 10.1016/j.cbpa.2007.08.033 . ПМИД 17936059 .
- ^ Jump up to: а б Сантана К., до Насименту Л.Д., Лима и Лима А., Дамасцено В., Наум К., Брага Р.К., Ламейра Дж. (29 апреля 2021 г.). «Применение виртуального скрининга в биоразведке: факты, изменения и перспективы для изучения хемо-структурного разнообразия природных продуктов» . Границы в химии . 9 : 662688. Бибкод : 2021FrCh....9..155S . дои : 10.3389/fchem.2021.662688 . ISSN 2296-2646 . ПМК 8117418 . ПМИД 33996755 .
- ^ Сунь Х (2008). «Виртуальный скрининг на основе фармакофоров». Современная медицинская химия . 15 (10): 1018–24. дои : 10.2174/092986708784049630 . ПМИД 18393859 .
- ^ Уиллет П., Барнард Дж. М., Даунс Г. М. (1998). «Поиск химического сходства». Журнал химической информации и компьютерных наук . 38 (6): 983–996. CiteSeerX 10.1.1.453.1788 . дои : 10.1021/ci9800211 .
- ^ Раш Т.С., Грант Дж.А., Мосяк Л., Николлс А. (март 2005 г.). «Метод трехмерного прыжкового каркаса, основанный на форме, и его применение к бактериальному белок-белковому взаимодействию». Журнал медицинской химии . 48 (5): 1489–95. CiteSeerX 10.1.1.455.4728 . дои : 10.1021/jm040163o . ПМИД 15743191 .
- ^ Баллестер П.Дж., Вествуд И., Лаурьери Н., Сим Э., Ричардс В.Г. (февраль 2010 г.). «Проспективный виртуальный скрининг с помощью сверхбыстрого распознавания форм: идентификация новых ингибиторов ариламин-N-ацетилтрансфераз» . Журнал Королевского общества, Интерфейс . 7 (43): 335–42. дои : 10.1098/rsif.2009.0170 . ПМЦ 2842611 . ПМИД 19586957 .
- ^ Кумар А., Чжан К.Ю. (2018). «Достижения в разработке методов сходства формы и их применение при открытии лекарств» . Границы в химии . 6 : 315. Бибкод : 2018FrCh....6..315K . дои : 10.3389/fchem.2018.00315 . ПМК 6068280 . ПМИД 30090808 .
- ^ Ли Х, Люнг К.С., Вонг М.Х., Баллестер П.Дж. (июль 2016 г.). «USR-VS: веб-сервер для крупномасштабного проспективного виртуального скрининга с использованием сверхбыстрых методов распознавания форм» . Исследования нуклеиновых кислот . 44 (П1): И436–41. дои : 10.1093/nar/gkw320 . ПМЦ 4987897 . ПМИД 27106057 .
- ^ Сперандио О, Петижан М, Таффери П (июль 2009 г.). «wwLigCSRre: трехмерный сервер на основе лигандов для идентификации и оптимизации попаданий» . Исследования нуклеиновых кислот . 37 (проблема с веб-сервером): W504–9. дои : 10.1093/нар/gkp324 . ПМК 2703967 . ПМИД 19429687 .
- ^ Jump up to: а б Кирхмайр Дж., Дистинто С., Маркт П., Шустер Д., Спитцер Г.М., Лидл К.Р., Вольбер Г. (2009). «Как оптимизировать виртуальный скрининг на основе формы: выбор правильного запроса и включение химической информации». Журнал химической информации и моделирования . 49 (3): 678–692. дои : 10.1021/ci8004226 . ПМИД 19434901 .
- ^ Толедо Варшавиак Д., Голан Г., Боррелли К.В., Жу К., Калид О. (июль 2014 г.). «Подход к виртуальному скринингу на основе структуры для обнаружения ковалентно связанных лигандов». Журнал химической информации и моделирования . 54 (7): 1941–50. дои : 10.1021/ci500175r . ПМИД 24932913 .
- ^ Майя Э.Х., Ассис Л.К., де Оливейра Т.А., да Силва А.М., Таранто АГ (28 апреля 2020 г.). «Виртуальный скрининг на основе структур: от классического к искусственному интеллекту» . Границы в химии . 8 : 343. Бибкод : 2020FrCh....8..343M . дои : 10.3389/fchem.2020.00343 . ПМК 7200080 . ПМИД 32411671 .
- ^ Кремер RT (август 2007 г.). «Разработка лекарств на основе структуры: стыковка и оценка». Современная наука о белках и пептидах . 8 (4): 312–28. CiteSeerX 10.1.1.225.959 . дои : 10.2174/138920307781369382 . ПМИД 17696866 .
- ^ Кавасотто CN, Орри Эй Джей (2007). «Стыковка лигандов и виртуальный скрининг на основе структуры при открытии лекарств». Актуальные темы медицинской химии . 7 (10): 1006–14. дои : 10.2174/156802607780906753 . ПМИД 17508934 .
- ^ Кооистра А.Дж., Вишер Х.Ф., Макнот-Флорес Д., Леурс Р., де Эш И.Дж., де Грааф К. (июнь 2016 г.). «Функциональный виртуальный скрининг лигандов GPCR с использованием комбинированного метода оценки» . Научные отчеты . 6 : 28288. Бибкод : 2016NatSR...628288K . дои : 10.1038/srep28288 . ПМЦ 4919634 . ПМИД 27339552 .
- ^ Ирвин Дж.Дж., Шойчет Б.К., Майсингер М.М., Хуан Н., Колицци Ф., Вассам П., Цао Ю (сентябрь 2009 г.). «Автоматическая стыковка экранов: технико-экономическое обоснование» . Журнал медицинской химии . 52 (18): 5712–20. дои : 10.1021/jm9006966 . ПМЦ 2745826 . ПМИД 19719084 .
- ^ Ли Х, Люнг К.С., Баллестер П.Дж., Вонг М.Х. (24 января 2014 г.). «istar: веб-платформа для крупномасштабного стыковки белков и лигандов» . ПЛОС ОДИН . 9 (1): e85678. Бибкод : 2014PLoSO...985678L . дои : 10.1371/journal.pone.0085678 . ПМК 3901662 . ПМИД 24475049 .
- ^ Jump up to: а б Чжоу Х., Сколник Дж. (январь 2013 г.). «FINDSITE (гребень): подход скрининга виртуальных лигандов на основе нитей/структуры в протеомном масштабе» . Журнал химической информации и моделирования . 53 (1): 230–40. дои : 10.1021/ci300510n . ПМЦ 3557555 . ПМИД 23240691 .
- ^ Рой А., Сколник Дж. (февраль 2015 г.). «LIGSIFT: инструмент с открытым исходным кодом для структурного выравнивания лигандов и виртуального скрининга» . Биоинформатика . 31 (4): 539–44. doi : 10.1093/биоинформатика/btu692 . ПМЦ 4325547 . ПМИД 25336501 .
- ^ Голтон А., Беллис Л.Дж., Бенто А.П., Чемберс Дж., Дэвис М., Херси А., Лайт Ю., МакГлинчи С., Михалович Д., Аль-Лазикани Б., Оверингтон Дж.П. (январь 2012 г.). «ChEMBL: крупномасштабная база данных о биологической активности для открытия лекарств» . Исследования нуклеиновых кислот . 40 (проблема с базой данных): D1100–7. дои : 10.1093/nar/gkr777 . ПМК 3245175 . ПМИД 21948594 .
- ^ Уишарт Д.С. , Нокс С., Го А.С., Шривастава С., Хасанали М., Стотхард П., Чанг З., Вулси Дж. (январь 2006 г.). «DrugBank: комплексный ресурс для открытия и исследования лекарств in silico» . Исследования нуклеиновых кислот . 34 (Проблема с базой данных): D668–72. дои : 10.1093/nar/gkj067 . ПМЦ 1347430 . ПМИД 16381955 .
- ^ Рео М., Лангенфельд Ф., Загури Ж.Ф., Лагард Н., Монтес М. (2018). «Выбор приманок в наборах данных для сравнительного анализа: обзор и перспективы» . Границы в фармакологии . 9:11 . дои : 10.3389/fphar.2018.00011 . ПМЦ 5787549 . ПМИД 29416509 .
- ^ Jump up to: а б Баллестер Пи Джей (декабрь 2019 г.). «Выбор функций оценки машинного обучения для виртуального скрининга на основе структуры» . Открытие лекарств сегодня: технологии . 32–33: 81–87. дои : 10.1016/j.ddtec.2020.09.001 . ПМИД 33386098 . S2CID 224968364 .
- ^ Ли Х, Сзе К.Х., Лу Г, Баллестер П.Дж. (2021). «Функции оценки машинного обучения для виртуального скрининга на основе структуры». WIREs Вычислительная молекулярная наука . 11 (1): e1478. дои : 10.1002/wcms.1478 . ISSN 1759-0884 . S2CID 219089637 .
- ^ Валлах I, Хейфец А (2018). «Большинство тестов классификации на основе лигандов вознаграждают за запоминание, а не за обобщение». Журнал химической информации и моделирования . 58 (5): 916–932. arXiv : 1706.06619 . doi : 10.1021/acs.jcim.7b00403 . ПМИД 29698607 . S2CID 195345933 .
- ^ Ирвин Джей-Джей (2008). «Эталоны сообщества для виртуального скрининга». Журнал компьютерного молекулярного дизайна . 22 (3–4): 193–9. Бибкод : 2008JCAMD..22..193I . дои : 10.1007/s10822-008-9189-4 . ПМИД 18273555 . S2CID 26260725 .
- ^ Хороший AC, Oprea TI (2008). «Оптимизация методов CAMD 3. Расширенные исследования виртуального скрининга: помощь или помеха в выборе инструментов?». Журнал компьютерного молекулярного дизайна . 22 (3–4): 169–78. Бибкод : 2008JCAMD..22..169G . дои : 10.1007/s10822-007-9167-2 . ПМИД 18188508 . S2CID 7738182 .
- ^ Шнайдер Г. (апрель 2010 г.). «Виртуальный показ: бесконечная лестница?». Обзоры природы. Открытие наркотиков . 9 (4): 273–6. дои : 10.1038/nrd3139 . ПМИД 20357802 . S2CID 205477076 .
- ^ Баллестер П.Дж. (январь 2011 г.). «Сверхбыстрое распознавание формы: метод и приложения». Будущая медицинская химия . 3 (1): 65–78. дои : 10.4155/fmc.10.280 . ПМИД 21428826 .
- ^ Лавечкья А, Ди Джованни С (2013). «Стратегии виртуального скрининга при открытии лекарств: критический обзор». Современная медицинская химия . 20 (23): 2839–60. дои : 10.2174/09298673113209990001 . ПМИД 23651302 .
- ^ Спитцер Г.М., Хейсс М., Мангольд М., Маркт П., Кирхмайр Дж., Вольбер Г., Лидл К.Р. (2010). «Одна концепция, три реализации виртуального трехмерного скрининга на основе фармакофора: четкий охват пространства химического поиска». Журнал химической информации и моделирования . 50 (7): 1241–1247. дои : 10.1021/ci100136b . ПМИД 20583761 .
- ^ Грант Дж.А., Галлард М.А., Pickup BT (1996). «Быстрый метод сравнения формы молекул: простое применение гауссовского описания формы молекул». Журнал вычислительной химии . 17 (14): 1653–1666. doi : 10.1002/(SICI)1096-987X(19961115)17:14<1653::AID-JCC7>3.0.CO;2-K .
- ^ Николлс А., Грант Дж.А. (2005). «Форма молекулы и электростатика в кодировании соответствующей химической информации». Журнал компьютерного молекулярного дизайна . 19 (9–10): 661–686. дои : 10.1007/s10822-005-9019-x . ПМИД 16328855 .
- ^ Раш Т.С., Грант Дж.А., Мосяк Л., Николлс А. (2005). «Метод трехмерного прыжкового каркаса, основанный на форме, и его применение к бактериальному белок-белковому взаимодействию». Журнал медицинской химии . 48 (5): 1489–1495. дои : 10.1021/jm040163o . ПМИД 15743191 .
- ^ Невес Б.Ю., Брага Р.К., Мело-Филью СС, Морейра-Филью Ж.Т., Муратов Е.Н., Андраде СН (13.11.2018). «Виртуальный скрининг на основе QSAR: достижения и применения в поиске лекарств» . Границы в фармакологии . 9 : 1275. дои : 10.3389/fphar.2018.01275 . ПМК 6262347 . ПМИД 30524275 .
- ^ Алсенан С., Аль-Тураики И., Хафез А. (декабрь 2020 г.). «Модель рекуррентной нейронной сети для прогнозирования проницаемости гематоэнцефалического барьера» . Вычислительная биология и химия . 89 : 107377. doi : 10.1016/j.compbiolchem.2020.107377 . ПМИД 33010784 .
- ^ Дмитрий ГМ, Лио П (июнь 2017 г.). «DrugClust: подход машинного обучения для прогнозирования побочных эффектов лекарств». Вычислительная биология и химия . 68 : 204–210. doi : 10.1016/j.compbiolchem.2017.03.008 . ПМИД 28391063 .
- ^ Шумбуатонг В., Шадуанграт Н., Пративи Р., Нантасенамат К. (июнь 2019 г.). «THPep: подход на основе машинного обучения для прогнозирования пептидов, возвращающихся в опухоль». Вычислительная биология и химия . 80 : 441–451. doi : 10.1016/j.compbiolchem.2019.05.008 . ПМИД 31151025 .
- ^ Гуруджи К.С., Дешпанде В.Л. (февраль 1978 г.). «Улучшенный метод анализа оснований». Компьютеры и конструкции . 8 (1): 147–152. дои : 10.1016/0045-7949(78)90171-2 .
- ^ Прадипкиран Дж.А., Редди П.Х. (март 2019 г.). «Структурно-ориентированный дизайн и исследования молекулярного стыковки фосфорилированных ингибиторов тау при болезни Альцгеймера» . Клетки . 8 (3): 260. doi : 10.3390/cells8030260 . ПМК 6468864 . ПМИД 30893872 .
Дальнейшее чтение
[ редактировать ]- Мелаграки Г., Афантитис А., Саримвейс Х., Коутентис П.А., Маркопулос Дж., Игглесси-Маркопулу О. (май 2007 г.). «Оптимизация антагонистов рецепторов биарилпиперидина и 4-амино-2-биарилмочевины MCH1 с использованием QSAR-моделирования, методов классификации и виртуального скрининга». Журнал компьютерного молекулярного дизайна . 21 (5): 251–67. Бибкод : 2007JCAMD..21..251M . дои : 10.1007/s10822-007-9112-4 . ПМИД 17377847 . S2CID 19563229 .
- Афантитис А, Мелаграки Г, Саримвейс Х, Коутентис П.А., Маркопулос Дж, Игглесси-Маркопулу О (февраль 2006 г.). «Исследование влияния заместителя 1-(3,3-дифенилпропил)пиперидинилфенилацетамидов на аффинность связывания CCR5 с использованием методов QSAR и виртуального скрининга». Журнал компьютерного молекулярного дизайна . 20 (2): 83–95. Бибкод : 2006JCAMD..20...83A . CiteSeerX 10.1.1.716.8148 . дои : 10.1007/s10822-006-9038-2 . ПМИД 16783600 . S2CID 21523436 .
- Экерт Х., Баджорат Дж. (март 2007 г.). «Анализ молекулярного сходства при виртуальном скрининге: основы, ограничения и новые подходы». Открытие наркотиков сегодня . 12 (5–6): 225–33. дои : 10.1016/j.drudis.2007.01.011 . ПМИД 17331887 .
- Уиллетт П. (декабрь 2006 г.). «Виртуальный скрининг на основе сходства с использованием 2D-отпечатков пальцев» (PDF) . Открытие лекарств сегодня (представленная рукопись). 11 (23–24): 1046–53. дои : 10.1016/j.drudis.2006.10.005 . ПМИД 17129822 .
- Фара Д.С., Опря Т.И., Просниц Э.Р., Болога К.Г., Эдвардс Б.С., Склар Л.А. (2006). «Интеграция виртуального и физического скрининга» . Открытие лекарств сегодня: технологии . 3 (4): 377–385. дои : 10.1016/j.ddtec.2006.11.003 . ПМК 7105924 . ПМИД 38620118 .
- Мюгге I, Олоффа С (2006). «Достижения виртуального скрининга» . Открытие лекарств сегодня: технологии . 3 (4): 405–411. дои : 10.1016/j.ddtec.2006.12.002 . ПМК 7105922 . ПМИД 38620182 .
- Шнайдер Г. (апрель 2010 г.). «Виртуальный показ: бесконечная лестница?». Обзоры природы. Открытие наркотиков . 9 (4): 273–6. дои : 10.1038/nrd3139 . ПМИД 20357802 . S2CID 205477076 .
Внешние ссылки
[ редактировать ]- VLS3D — список из более чем 2000 баз данных, онлайн и автономных in silico . инструментов
