Галогенирование кетона
В органической химии α -кетогалогенирование — особый тип галогенирования . Реакцию можно проводить как в кислых, так и в основных условиях в водной среде с соответствующим элементарным галогеном . Таким образом, хлоридные , бромидные и йодидные (но особенно не ) функциональные группы могут быть избирательно вставлены в альфа-положение кетона фторидные .
Положение альфа по отношению к карбонильной группе ( C=O ) в кетонах легко галогенируется. Это связано с его способностью образовывать енолят ( С=С-О − ) в основном растворе или еноле ( C=C-OH ) в кислом растворе. Примером альфа-галогенирования монобромирование ацетона является ( (CH 3 ) 2 C=O ), проводимый в кислых или основных условиях, с получением бромацетона :
Кислые (в уксусной кислоте):
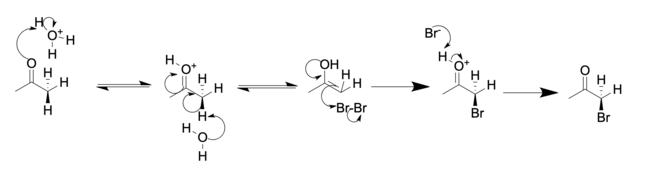
Основные (в водном растворе NaOH ):

В кислом растворе галогеном обычно заменяется только один альфа-водород, поскольку каждое последующее галогенирование протекает медленнее, чем первое. Галоген снижает основность карбонильного кислорода, что делает протонирование менее выгодным. Однако в основных растворах последовательное галогенирование происходит быстрее из-за индуктивного отвода электронов галогеном. Это делает оставшиеся атомы водорода более кислыми. В случае метилкетонов эта реакция часто происходит в третий раз с образованием тригалогенида кетона, который может подвергаться быстрому замещению водой с образованием карбоксилата ( −С(=О)О − ) в так называемой галоформной реакции . [ 1 ]
Региоселективность более замещенной также различается: галогенирование несимметричного кетона в кислоте приводит к алкильной группы галогенированию . Второй эквивалент галогена приводит к галогенированию другого алкильного заместителя (без галогена). Напротив, в основных растворах несимметричный кетон галогенируется по менее замещенной алкильной группе. Последующее галогенирование (которое обычно не может быть остановлено контролем стехиометрии) происходит в положении, уже имеющем галогенный заместитель, до тех пор, пока все атомы водорода не будут заменены атомами галогена. Для метилалкилкетонов (2-алканонов) реакция галоформа протекает с селективным образованием карбоновой кислоты. [ 2 ]
Галогенирование α,β-ненасыщенных кетонов
[ редактировать ]
В случае α,β-ненасыщенных кетонов или енонов можно галогенировать йодом избирательно по более насыщенной альфа-кетону, избирательно по ненасыщенной стороне. Йод предпочтителен, поскольку он более реакционноспособен, чем алкилбромиды, что делает эту реакцию весьма полезной. [ 3 ] Используя CuO в сочетании с I 2 , можно добиться этой реакции в относительно мягких условиях. Эта реакция протекает по очень реакционноспособному енольному механизму, чему способствует CuO, что позволяет селективно присоединить I 2 к насыщенному альфа-углероду кетона. [ 4 ] Однако эффективность этой реакции зависит от присутствия арильных функциональных групп.
Применение в зеленой химии
[ редактировать ]Альфа-галогенированные продукты являются очень полезными соединениями, поскольку они обладают высокой реакционной способностью, что делает их очень склонными к реакции. Альфа-галогенированные кетоны реагируют с нуклеофилами с образованием многих ценных соединений. Однако многие современные методы галогенирования кетонов используют опасные химические вещества, имеют сложные процедуры и/или требуют длительного времени для завершения. Кроме того, полярные растворители, которые в основном используются (ДМФ, ДМСО и CH 3 CN), являются основными загрязнителями окружающей среды.
Эксперимент, проведенный Meshram et al. в 2005 году исследовал превращение галогенирования кетонов в более зеленую реакцию в соответствии с принципами зеленой химии . [ 5 ] [ 6 ] Мешрам и др. исследовали альтернативы опасным химическим веществам, которые в основном используются при галогенировании кетонов, и обнаружили, что ионные жидкости при комнатной температуре являются многообещающим вариантом. [ 6 ] Ионные жидкости при комнатной температуре представляют собой интересную перспективу, поскольку они обладают уникальными химическими и физическими свойствами, а их свойства можно модифицировать путем изменения присоединенных катионов. Кроме того, эти ионные жидкости обладают высокой полярностью, а их способность солюбилизировать органические и неорганические молекулы приводит к увеличению скорости реакции, что делает их более желательными.
Многие эксперименты показали, что ионные жидкости с N-галосукцинимидами в качестве растворителя являются эффективной и более экологичной альтернативой обычным растворителям. [ 6 ] Этот процесс также привел к увеличению выхода, сокращению времени реакции, упрощению процедуры, использованию меньшего количества вредных химикатов (без сильных кислот) и отсутствию необходимости в катализаторах , что сделало процесс более экологичным.
Ссылки
[ редактировать ]- ^ «Органическая химия», пятое издание, Паула Юрканис Брюс. Пирсон Прентис Холл, Аппер-Сэддл-Ривер, Нью-Джерси, 2007 г.
- ^ Клейден, Джонатан. (2012). Органическая химия . Гривз, Ник., Уоррен, Стюарт Г. (2-е изд.). Оксфорд: Издательство Оксфордского университета. ISBN 9780199270293 . OCLC 761379371 .
- ^ Перейти обратно: а б Ван, Цзихуа; Инь, Годун; Цинь, Цзин; Гао, Мэн; Цао, Липин; Ву, Аньсинь (ноябрь 2008 г.). «Эффективный метод селективного йодирования α,β-ненасыщенных кетонов» . Синтез . 2008 (22): 3675–3681. дои : 10.1055/s-0028-1083200 . ISSN 0039-7881 .
- ^ «Галогенирование кетонов через енолы» . Магистр органической химии . Проверено 13 ноября 2022 г.
- ^ «12 принципов зеленой химии» . Американское химическое общество . Проверено 13 ноября 2022 г.
- ^ Перейти обратно: а б с Мешрам, HM; Редди, ПН; Вишну, П.; Садашив, К.; Ядав, Дж.С. (6 февраля 2006 г.). «Зеленый подход к эффективному α-галогенированию β-дикарбонильных соединений и циклических кетонов с использованием N-галосукцинимидов в ионных жидкостях» . Буквы тетраэдра . 47 (6): 991–995. дои : 10.1016/j.tetlet.2005.11.141 . ISSN 0040-4039 .