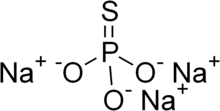
Монотиофосфат натрия
| |
| Имена | |
|---|---|
| Имя IUPAC
Монотиофосфат натрия
| |
| Идентификаторы | |
| |
3D model ( JSmol )
|
|
| Echa Infocard | 100.030.224 |
| ЕС номер |
|
PubChem CID
|
|
| НЕКОТОРЫЙ |
|
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| NA 3 PO 3 S | |
| Молярная масса | 180.00 g·mol −1 |
| Появление | Белое твердое вещество |
| Плотность | 1,58 г/см 3 (Додекагидрат) 2,40 г/см 3 (Безводная) |
| Точка плавления | От 120 до 125 ° C (от 248 до 257 ° F; от 393 до 398 K) (разложение) |
| растворимый | |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
Монотиофосфат натрия , или фосфоротиоат натрия , является неорганическим соединением с химической формулой NA 3 P O 3 S. Это натриевая соль монотиофосфорной кислоты ( H 3 PO 3 S ). Монотиофосфат натрия образует гидраты NA 3 PO 3 S X H 2 O. · Безводная форма и все гидраты - это белые твердые тела. Безводная соль ( x = 0) ( NA 3 PO 3 S ) разлагается без плавления при 120-125 ° C. Более распространенным является додекагидрат ( NA 3 PO 3 S · 12H 2 O ). Также известен негидрат ( NA 3 PO 3 S · 9H 2 O ).
Связанные соли являются ди -тиофосфатом натрия, некейгидрат NA 3 PO 2 S 2 · 11H 2 O , натрия три тиофосфат некейгидрат Na 3 Pos 3 · 11h 2 O и натрия тетра октагидрат тетра NA 3 PS 4 · 2 O. 8H [ 1 ]
Подготовка
[ редактировать ]Монотиофосфат натрия получают основополагающим гидролизом тиофосфорилхлорида с использованием водного гидроксида натрия : [ 2 ] [ 3 ]
- PSCL 3 + 6 NaOH + 9 H 2 O → Na 3 PO 3 S · 12H 2 O + 3 NaCl
Эта реакция дает додекагидрат, который легко обезвоживается .
Частичное обезвоживание более 6,5 м H 2 SO 4 дает негидрат. Под течением N 2 , безводная соль образуется. [ 4 ]
Монотиофосфат натрия разлагается при нейтральном рН . Силиконовая смазка катализирует гидролиз монотиофосфата иона По 3 с 3− , поэтому рекомендуется, чтобы он не использовался в стеклянных суставах. [ 5 ]
В безводной соли связывание PS составляет 211 вечера , а три эквивалентные связи PO короткие в 151 вечера. Эти разнородные значения предполагают, что связь PS является одинокой. [ 6 ]
Ссылки
[ редактировать ]- ^ Элиас, DP (1957). «Кристаллографические данные о некоторых фосфоротиоатах натрия» . Acta Crystallographica . 10 (9): 600. Bibcode : 1957accry..10..600e . doi : 10.1107/s0365110x57002108 .
- ^ Стэнли К. Ясуда; Джек Л. Ламберт (1957). «Монотиофосфат натрия». Неорганические синтезы . Тол. 5. С. 102–104. doi : 10.1002/9780470132364.CH28 . ISBN 978-0-470-13236-4 .
- ^ LC Washburn; Р.Л. Хейс (1977). «Важность избыточного основания в синтезе монотиофосфата натрия: (фосфоротиоат натрия)». Неорганические синтезы . Тол. 17. С. 193–4. doi : 10.1002/9780470132487.CH53 . ISBN 978-0-470-13248-7 .
- ^ Палацци, Марсель (1973). «Тризодий монотиофосфат. Радиокристаллографическое исследование». Бюллетень Франции химического общества . 12 : 3246–8.
- ^ Люсиан С. Поп и М. Сайто (2015). «Случайные реакции, связанные с силиконовой смазкой». Обзоры координационной химии . 314 : 64–70. doi : 10.1016/j.ccr.2015.07.005 .
- ^ Pompetzki, M.; Янсен М. (2002). «Монотиофосфат натрия (V): кристаллическая структура и ионная проводимость натрия» [Монотиофосфат натрия (V). Кристаллическая структура и ионная проводимость натрия]. Журнал неорганической и общей химии . 628 (3): 641–646. Doi : 10.1002/1521-3749 (200203) 628: 3 <641 :: Aid-zaac641> 3.0.co ;