Автоматический зажим патча
автоматическое крепление заплаток Начинается [1] заменить ручное зажатие пластыря как метод измерения электрической активности отдельных клеток . используются различные методы Для автоматизации записи патч-клампов клеток в клеточной культуре и in vivo . Эта работа ведется с конца 1990-х годов исследовательскими лабораториями и компаниями, пытающимися снизить сложность и стоимость ручного зажима заплаты. Закрепление патчей долгое время считалось формой искусства и до сих пор является очень трудоемким и утомительным занятием, особенно in vivo. Методы автоматизации пытаются уменьшить ошибки пользователя и вариативность при получении качественных электрофизиологических записей из отдельных клеток.
Ручной зажим патча [ править ]
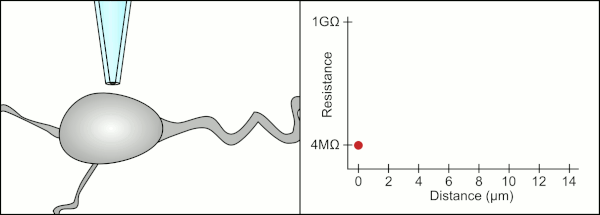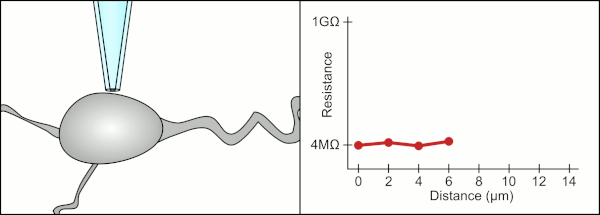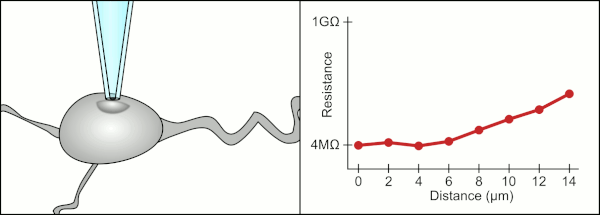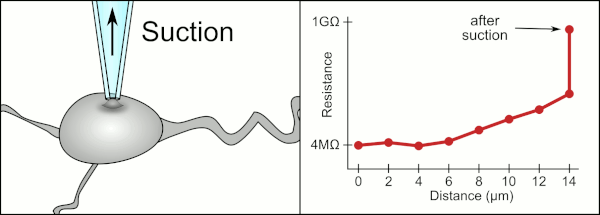
Традиционный ручной метод фиксации зажима с использованием стеклянных пипеток был разработан Эрвином Неером и Бертом Сакманном и требовал высококвалифицированного специалиста. Техник располагал стеклянную пипетку рядом с клеткой и применял соответствующее отсасывание, чтобы создать электрическое уплотнение между пипеткой и клеточной мембраной. Это уплотнение обеспечивает качественную запись, предотвращая утечку тока между кончиком пипетки и клеточной мембраной. Это уплотнение создается, когда мембрана клетки химически связывается с кончиком пипетки так, что внутренняя часть пипетки соединяется только с цитоплазмой клетки . Это соединение или уплотнение мембраны и стекла называется «gigaseal». [2]
Техник традиционно использовал свой рот, чтобы обеспечить точное давление, необходимое для присоединения его к ячейке. Помимо контроля давления, техник должен также расположить пипетку на точно правильном расстоянии от клетки, чтобы мембрана плотно прилегала к ней. С помощью микроманипулятора пипетку перемещают по направлению к клетке до тех пор, пока техник не увидит изменение электрического сопротивления между жидкостью внутри пипетки и окружающей жидкостью (см. анимацию). Обычно для этого требуется 3–12 месяцев обучения, прежде чем техник сможет надежно записывать данные с клеток. Техник, по сути, выполняет балансирующее действие, пытаясь одновременно наблюдать и манипулировать несколькими системами (движение, давление и электрические сигналы). Если каждая часть процесса не будет выполнена точно и в правильное время, уплотнение не будет сформировано должным образом, и технику придется заменить пипетку и начать все сначала.
Эти проблемы сокращают количество записей, которые может получить техник, и значительно увеличивают стоимость. Автоматизация направлена на сокращение времени, сложности и стоимости ручного зажима заплат. Повышение производительности также будет иметь ключевое значение для обеспечения высокой производительности патч-секвенирования для одновременного объединения электрофизиологических , морфологических и транскриптомных свойств нейронов в масштабе, сравнимом с другими секвенирования . методами [3]
Системы автоматизации [ править ]
Методика автоматизации варьируется в зависимости от окружающей среды клеток. Для клеток in vivo это обычно означает, что клетки находятся в мозге и окружены другими клетками. Эта среда также содержит кровеносные сосуды , дендриты , аксоны и глиальные клетки , которые затрудняют формирование гигазеала из-за закупорки кончика пипетки диаметром 1–2 мкм. Здесь точный контроль давления и положения кончика пипетки играет большую роль в предотвращении засорения и определении того, находится ли клетка рядом с кончиком пипетки, как обсуждалось выше.
Клетки in vitro могут быть суспендированы в жидкости, прикреплены к культуральной чашке или оставаться частью части ткани, удаленной от животного. Эти среды обычно не должны компенсировать движение тканей, вызванное сердцебиением или дыханием животного. В случае клеток в суспензии пипетка полностью заменяется микрочипом с отверстиями, которые могут создавать гигагерметики и измерять электрическую активность. Засорение также менее проблематично для клеток или тканей в культуральных чашках, поскольку клетки и пипетку можно увидеть в микроскоп, что помогает технику избежать всего, кроме интересующей клетки.
Каждая из этих автоматизированных систем должна выполнять несколько задач. Он должен расположить ячейку рядом с кончиком пипетки или другого устройства с отверстием диаметром 1–2 мкм, контролировать давление в отверстии и контролировать напряжение внутри клетки.
В естественных условиях [ править ]
Один пример зажима пластыря in vivo был показан Kodandaramaiah и соавт. [4] В этом случае контроль давления состоял из набора электронных клапанов и электронных регуляторов давления для обеспечения трех давлений, которые ранее обеспечивались техническим специалистом (высокое давление 800-1000 мбар, низкое давление 20-30 мбар и небольшой вакуум 15-150 мбар). Три электронных клапана переключались между тремя давлениями и атмосферным давлением. Высокое давление использовалось для предотвращения засорения пипетки, низкое давление использовалось при поиске клеток, а вакуум использовался для облегчения процесса гигагерметизации. Все они контролировались компьютером, который позволял выбирать давление по мере изменения сопротивления на кончике пипетки.
Ручное управление положением в этом случае было заменено пьезоэлектрическим микроманипулятором с компьютерным управлением , который перемещал пипетку дискретными шагами по 2-3 мкм в ткань до тех пор, пока она не вступала в контакт с клеткой. Этот прецизионный контроль гораздо более точен и воспроизводим, чем ручное позиционирование, и не требует участия оператора.
Компьютер также рассчитывает и отслеживает изменение электрического сопротивления при контакте пипетки с клеткой. Он посылает по пипетке сигнал напряжения в виде прямоугольной волны, который либо выходит из конца пипетки, либо блокируется клеточной мембраной. Когда мембрана блокирует его, компьютер останавливает движение пипетки и применяет всасывание, чтобы сформировать гигасеаль. Эта автоматизация исключает необходимость принятия решений, которые должен выполнять технический специалист, и, в отличие от технического специалиста, компьютер может выполнять эти задачи неустанно и с большей точностью.
Все эти шаги выполняются в той же логической последовательности, что и ручное закрепление заплатки, но не требуют длительной подготовки и полностью контролируются компьютером. Это снижает затраты, необходимые для получения записей патч-клампа, и увеличивает повторяемость и надежность записи в живом мозге.
В подвеске [ править ]


Было разработано множество типов систем для фиксации клеток в суспензионных культурах. В одной системе используется традиционная пипетка и клетки в капельно-суспензионной культуре для получения записей с помощью патч-клампа (см. рисунок). Это имеет дополнительное преимущество, заключающееся в использовании традиционных систем изготовления пипеток, которые нагревают стеклянный капилляр и тянут его вдоль, создавая конический кончик, используемый при патч-зажиме.
Более распространенные системы автоматизации для суспензионных культур используют микрочипы с крошечными (1-2 мкм) отверстиями в плоском субстрате вместо пипеток для создания гигазелей и записи отдельных клеток. Патч-чипы были разработаны в начале 2000-х годов в результате совершенствования технологий микропроизводства , разработанных полупроводниковой промышленностью. Чипы обычно изготавливаются из кремния , стекла , ПДМС , полимида . Системы патч-чипов обычно более сложны и дороги, но имеют дополнительное преимущество параллельной работы и работы без помощи рук. [5] [6] [7]
Обычно нейроны не растут в суспензионных культурах, но другие типы клеток могут. Некоторые из них можно трансфицировать мембранных ионных каналов генами для создания интересующих . Это означает, что клетка, которая обычно не обладает электрической активностью, может выращивать в своей мембране ионные каналы, которые будут генерировать ионные токи. Поскольку в суспензионных культурах клетки отделены друг от друга, ионные токи в отдельной клетке можно измерить с высокой точностью. Это позволяет исследователям изучать поведение ионных каналов в более контролируемых средах без вмешательства токов от других клеток, как это обычно происходит в нейронных сетях. Это особенно полезно в исследованиях по скринингу лекарств, где мишенью является конкретный белок. [8] Поскольку работать с клетками в суспензии намного проще, чем с клетками в культуре или in vivo, таким образом записи патч-клампа можно получить гораздо быстрее и надежнее, что повышает производительность и делает возможным скрининг тысяч соединений. [9]
Нейроны, полученные из стволовых клеток , культивированных адгезивно, можно перевести в суспензию и успешно использовать в устройствах с плоскими патч-зажимами. [10] Ионные каналы, такие как потенциал-управляемые натриевые каналы , потенциал-управляемые калиевые каналы и ионотропные лиганд-управляемые ионные каналы, открытые лигандом ГАМК, были записаны из этих клеток с использованием автоматического и ручного патч-клампа. [11]
В культуре [ править ]
Существует множество методов in vitro для автоматического фиксации культивируемых клеток или срезов ткани головного мозга пластырями.
Один из них использует патч-чип, подобный тем, которые обсуждались выше, а также обработку поверхности, которая заставляет культивируемые клетки мигрировать к отверстиям, где по мере их роста образуется гигазеаль. [12] Позволяя нейронам расти в культуре, они спонтанно образуют сети, подобные сетям в мозге, которые больше похожи на естественные ткани, чем на изолированные клетки в суспензии.
В другом методе клетки извлекают из животного и культивируют на чипе-пластыре в течение 2–4 часов, поскольку они спонтанно образуют гигасели с из полиимида и ПДМС. чипами [13] Эта система не требует внешнего оборудования для формирования гигасил.
Другой метод автоматизирует позиционирование клеток, зажимающих патчи, в культурах. Он использует нанопипетку на точном пьезоприводном столике для сканирования поверхности внутри культуральной чашки. Во время сканирования он поддерживает постоянную электрическую емкость между кончиком пипетки и поверхностью или клетками под ней, перемещая ее вверх и вниз. (По мере приближения к клетке емкость увеличивается, поэтому привод отодвигает пипетку, и наоборот.) Это дает точное топографическое картирование поверхности внутри культуральной чашки. После того, как клетки были картированы, компьютер перемещает пипетку к выбранной ячейке и опускает ее, образуя с ней гигасеаль. [14]
Другой метод просто автоматизирует процесс осторожного установления контакта с клетками. Оператор размещает пипетку над образцом, а затем позволяет автоматизированному программному обеспечению взять на себя работу, опуская пипетку и пытаясь обнаружить увеличение сопротивления пипетки при ее контакте с клеткой. На этом процесс заканчивается, и техник создает гигапечать вручную.
Разработка и принятие [ править ]
Приборы для автоматизации с использованием патч-зажима стали коммерчески доступными в 2003 году. Из-за первоначальной высокой стоимости эта технология, созданная почти 20 лет назад, изначально предназначалась для обслуживания биотехнологической и фармацевтической промышленности, но с тех пор она также использовалась в научных кругах и некоммерческих организациях, в связи и сосуществование с другими связанными или дополнительными технологиями и методами. [15] Принятие и признание автоматизации патч-зажимной электрофизиологии отразилось на росте количества научной литературы, издаваемой с использованием этой технологии. [16]
Ссылки [ править ]
- ^ Вуд С., Уильямс С., Уолдрон Г.Дж. (май 2004 г.). «Зажим патчей по номерам». Открытие наркотиков сегодня . 9 (10): 434–41. дои : 10.1016/S1359-6446(04)03064-8 . ПМИД 15109948 .
- ^ Хэмилл О.П., Марти А., Неер Э., Сакманн Б., Сигворт Ф.Дж. (август 1981 г.). «Улучшенные методы патч-зажима для записи тока с высоким разрешением из клеток и патчей бесклеточных мембран». Архив Пфлюгерса . 391 (2): 85–100. CiteSeerX 10.1.1.456.107 . дои : 10.1007/BF00656997 . ПМИД 6270629 . S2CID 12014433 .
- ^ Трипати, Шриджой Дж.; Токер, Лайла; Бомкамп, Клэр; Манкарчи, Б. Оган; Бельмадани, Мануэль; Павлидис, Пол (08 октября 2018 г.). «Оценка качества транскриптома в наборах данных Patch-Seq» . Границы молекулярной нейронауки . 11 : 363. doi : 10.3389/fnmol.2018.00363 . ISSN 1662-5099 . ПМК 6187980 . ПМИД 30349457 .
- ^ Кодандарамайя С.Б., Францези Г.Т., Чоу Б.И., Бойден Э.С., Форест Ч.Р. (июнь 2012 г.). «Автоматизированная цельноклеточная электрофизиология нейронов in vivo» . Природные методы . 9 (6): 585–7. doi : 10.1038/nmeth.1993 . ПМЦ 3427788 . ПМИД 22561988 .
- ^ Джонс К.А., Гарбати Н., Чжан Х.М., Большой CH (2009). «Автоматическое закрепление патчей с использованием QPatch». Высокопроизводительный скрининг . Методы молекулярной биологии. Том. 565. стр. 209–23. дои : 10.1007/978-1-60327-258-2_10 . ISBN 978-1-60327-257-5 . ПМИД 19551364 .
- ^ Чен С.И., Ту Т.Я., Чен Ч., Чон Д.С., Во А.М. (август 2009 г.). «Зажим заплатки на плоском стекле - изготовление апертуры песочных часов и высокопроизводительная запись ионных каналов». Лаборатория на чипе . 9 (16): 2370–80. дои : 10.1039/B901025D . ПМИД 19636469 .
- ^ Обергруссбергер А, Штёльцле-Фейкс С, Беккер Н, Брюггеманн А, Фертиг Н, Мёллер С (2015). «Новые методы скрининга лекарств, нацеленных на ионные каналы» . Каналы . 9 (6): 367–75. дои : 10.1080/19336950.2015.1079675 . ПМК 4850050 . ПМИД 26556400 .
- ^ Данлоп Дж., Боулби М., Пери Р., Васильев Д., Ариас Р. (апрель 2008 г.). «Высокопроизводительная электрофизиология: новая парадигма скрининга и физиологии ионных каналов». Обзоры природы. Открытие наркотиков . 7 (4): 358–68. дои : 10.1038/nrd2552 . ПМИД 18356919 . S2CID 9294213 .
- ^ Обергруссбергер А., Брюггеманн А., Гетце Т.А., Рапедиус М., Хаарманн С., Ринке И. и др. (декабрь 2016 г.). «Автоматизированный патч-кламп обеспечивает высокопроизводительный скрининг: 384 клетки, записанные параллельно на плоском модуле патч-клампа» . Журнал автоматизации лабораторий . 21 (6): 779–793. дои : 10.1177/2211068215623209 . ПМИД 26702021 .
- ^ Хейторнтуэйт А., Столцл С., Хаслер А., Кисс А., Мосбахер Дж., Джордж М. и др. (октябрь 2012 г.). «Характеристика ионных каналов человека в индуцированных нейронах, полученных из плюрипотентных стволовых клеток» . Журнал биомолекулярного скрининга . 17 (9): 1264–72. дои : 10.1177/1087057112457821 . ПМИД 22923790 .
- ^ Хейторнтуэйт А., Столцл С., Хаслер А., Кисс А., Мосбахер Дж., Джордж М. и др. (октябрь 2012 г.). «Характеристика ионных каналов человека в индуцированных нейронах, полученных из плюрипотентных стволовых клеток» . Журнал биомолекулярного скрининга . 17 (9): 1264–72. дои : 10.1177/1087057112457821 . ПМИД 22923790 .
- ^ Пи С., Мартина М., Диас-Кихада Г.А., Люк CC, Мартинес Д., Денхофф М.В. и др. (2011). «От понимания клеточных функций к открытию новых лекарств: роль технологии чипов с плоскими патч-зажимными матрицами» . Границы в фармакологии . 2 : 51. дои : 10.3389/fphar.2011.00051 . ПМК 3184600 . ПМИД 22007170 .
- ^ Мартинес Д., Пи С., Денхофф М.В., Мартина М., Монетт Р., Комас Т. и др. (декабрь 2010 г.). «Высококачественные патч-записи нейронов, культивированных на полимерном микрочипе». Биомедицинские микроустройства . 12 (6): 977–85. CiteSeerX 10.1.1.362.9850 . дои : 10.1007/s10544-010-9452-z . ПМИД 20694518 . S2CID 14441945 .
- ^ Горелик Дж., Гу Ю., Шпор Х.А., Шевчук А.И., Лаб М.Дж., Хардинг С.Е. и др. (декабрь 2002 г.). «Ионные каналы в маленьких клетках и субклеточных структурах можно изучать с помощью умной системы патч-кламп» . Биофизический журнал . 83 (6): 3296–303. Бибкод : 2002BpJ....83.3296G . дои : 10.1016/S0006-3495(02)75330-7 . ПМК 1302405 . ПМИД 12496097 .
- ^ Пиконес А., Лоса-Уэрта А., Сегура-Чама П., Лара-Фигероа СО (2016). «Вклад автоматизированных технологий в открытие лекарств с ионными каналами». Достижения в области химии белков и структурной биологии . 104 : 357–378. дои : 10.1016/bs.apcsb.2016.01.002 . ISBN 9780128048269 . ПМИД 27038379 .
- ^ Пиконес А (2015). «Ионные каналы как лекарственные мишени биологических токсинов: влияние автоматизированной электрофизиологии патч-кламп». Актуальные темы медицинской химии . 15 (7): 631–7. дои : 10.2174/1568026615666150309145928 . ПМИД 25751269 .
Внешние ссылки [ править ]
- Глава книги, посвященная зажиму плоской заплатки. Архивировано 31 марта 2010 г. в Wayback Machine.
