Стивен Альдегид Синтез
| Стивен Альдегид Синтез | |
|---|---|
| Назван в честь | Генри Стивен |
| Тип реакции | Органическая окислительно -восстановительная реакция |
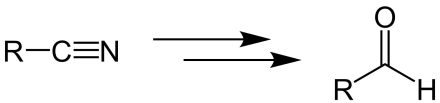
Синтез Стивена Альдегида , названная реакция в химии, был изобретен Генри Стивеном ( OBE / MBE ). Эта реакция включает в себя приготовление альдегидов (R-CHO) из нитрилов (R-CN) с использованием хлорида олова (II) (SNCL 2 ), соляной кислоты (HCL) и гашения полученной иминиемной соли ([R-CH = NH 2 ] + Калькуляция − ) с водой (H 2 O). [ 1 ] [ 2 ] Во время синтеза хлорид аммония также вырабатывается .
Механизм
[ редактировать ]Следующая схема показывает механизм реакции:

Путем добавления хлорида водорода используемый нитрил ( 1 ) реагирует на соответствующую соль ( 2 ). Считается, что эта соль уменьшается на одну перенос электрона хлоридом олова (II) ( 3A и 3B ). [ 3 ] Полученная соль ( 4 ) осаждается через некоторое время в виде хлорида альдимина олова ( 5 ). Гидролиз 5 производит гемиминальный ( 6 ), из которого альдегид ( 7 образуется ).
Заменители, которые увеличивают плотность электронов, способствуют образованию аддукта хлорида альдимин-тина. При отмене электронов заместители облегчены образование амид -хлорида. [ 4 ] В прошлом реакцию проводили путем осаждения хлорида альдимин-тина, промыв его эфиром, а затем гидролизовать его. Тем не менее, было обнаружено, что этот шаг не нужен, а хлорид олова альдимина может быть гидролизирован непосредственно в растворе. [ 5 ]
Эта реакция более эффективна, когда ароматические нитрилы используются вместо алифатических. Однако даже для некоторых ароматических нитрилов (например, этиловый эфир 2-цинобензойной кислоты) выход может быть низким. [ 5 ]
Сонн-Мюллер Метод
[ редактировать ]В методе Sonn-Müller [ 6 ] [ 7 ] Промежуточная соль иминия получается в результате реакции амидной фонхфы с пентахлоридом фосфора .
Смотрите также
[ редактировать ]- Амидное сокращение
- Нитриловое восстановление
- Реакция Пиннера - аналогичная реакция с использованием спиртов или аминов в качестве нуклеофила и без восстановления ; сгенерировали сложные эфиры, углексидаты или ортоэфиры .
Ссылки
[ редактировать ]- ^ Уильямс, Джонатан В. (1943). «β-нафтальдегид». Органические синтезы . 23 : 63. doi : 10.15227/orgsyn.023.0063 .
- ^ Стивен, Генри. (1925). «Новый синтез альдегидов». J. Chem. Soc., Trans. 127 : 1874–1877. doi : 10.1039/ct9252701874 .
- ^ Ван, Зеронг (2009). Комплексные органические реакции и реагенты, 3 набора томов . Джон Уайли и сыновья, Хобокен, Нью -Джерси. С. 2659–2660. ISBN 978-0-471-70450-8 .
- ^ Рабиновиц, Мордехай (1970). «Глава 7. Снижение группы Cyano». В Раппопорте, Зви (ред.). Cyano Group (1970) . Химия функциональных групп Патая. John Wiley & Sons, Ltd., Чичестер, Великобритания. п. 308. doi : 10.1002/9780470771242.ch7 . ISBN 978-0-470-77124-2 .
- ^ Jump up to: а беременный Ван, Зеронг (2009). Комплексные органические реакции и реагенты, 3 набора томов . Джон Уайли и сыновья, Хобокен, Нью -Джерси. С. 2659–2660. ISBN 978-0-471-70450-8 .
- ^ Адольф, Сонн; Мюллер, Эрнст (1919). «На новом методе преобразования карбоновых кислот в альдегид» [о новом методе преобразования карбоновых кислот в альдегиды]. Отчеты Германского химического общества (серия A и B) . 52 (10): 1927–1934. Doi : 10.1002/cber.19190521002 .
- ^ Уильямс, Джонатан В.; Виттен, Чарльз Х.; Криницкий, Джон А. (1946). " O -tolualdehyde". Органические синтезы . 26 : 97. doi : 10.15227/orgsyn.026.0097 .