Электронная плотность
Электронная плотность или электронная плотность — это мера вероятности присутствия электрона в бесконечно малом элементе пространства, окружающем любую данную точку. Это скалярная величина, зависящая от трех пространственных переменных, и обычно обозначается либо как или . Плотность определяется по определению нормализованным электрона - волновая функция , которая сама зависит от переменные ( пространственный и спиновые координаты). И наоборот, плотность определяет волновую функцию по модулю с точностью до фазового множителя, обеспечивая формальную основу теории функционала плотности .
Согласно квантовой механике , из-за принципа неопределенности в атомном масштабе невозможно предсказать точное местоположение электрона, а только вероятность его нахождения в заданном положении; поэтому электроны в атомах и молекулах действуют так, как будто они «размазаны» в пространстве. Для одноэлектронных систем плотность электронов в любой точке пропорциональна квадрату величины волновой функции .
Обзор [ править ]
В молекулах обычно находятся области с большой электронной плотностью вокруг атома и его связей . В делокализованных или сопряженных системах , таких как фенол , бензол и такие соединения, как гемоглобин и хлорофилл , электронная плотность значительна во всей области, т. е. в бензоле они находятся выше и ниже плоского кольца. Иногда это изображают схематически как серию чередующихся одинарных и двойных связей. В случае фенола и бензола кружок внутри шестиугольника показывает делокализованную природу соединения. Это показано ниже:

В соединениях с несколькими взаимосвязанными кольцевыми системами это уже неточно, поэтому используются чередующиеся одинарные и двойные связи. В таких соединениях, как хлорофилл и фенол, на некоторых диаграммах показана пунктирная или пунктирная линия, обозначающая делокализацию областей, где электронная плотность выше рядом с одинарными связями. [1] Сопряженные системы иногда могут представлять собой области, где электромагнитное излучение поглощается на разных длинах волн, в результате чего соединения кажутся окрашенными. В полимерах эти области известны как хромофоры.
В квантово-химических расчетах плотность электронов ρ( r ) является функцией координат r , определяемой так: ρ( r )d r — это количество электронов в небольшом объёме d r . Для с закрытой оболочкой молекул может быть записано через сумму произведений базисных функций φ:
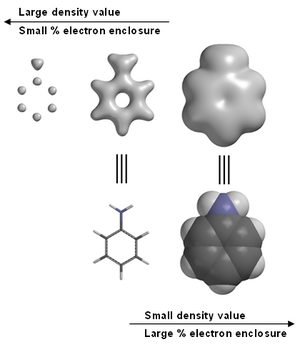
где P — матрица плотности . Плотность электронов часто выражается в виде изоповерхности (поверхности изоплотности), при этом размер и форма поверхности определяются значением выбранной плотности, или в процентах от общего количества заключенных электронов.
Программное обеспечение для молекулярного моделирования часто предоставляет графические изображения электронной плотности. Например, в анилине (см. изображение справа). Графические модели, включая электронную плотность, являются широко используемым инструментом в образовании по химии. [2] Обратите внимание, что на крайнем левом изображении анилина высокие плотности электронов связаны с атомами углерода и азота , но атомы водорода , имеющие только один протон в ядрах, не видны. Это причина того, что рентгеновская дифракция затрудняет определение положения водорода.
Большинство пакетов программного обеспечения для молекулярного моделирования позволяют пользователю выбирать значение электронной плотности, часто называемое изозначением. Некоторое программное обеспечение [3] также позволяет указать электронную плотность в процентах от общего количества включенных электронов. В зависимости от изозначения (типичными единицами измерения являются электроны на кубический бор ) или процента от общего количества включенных электронов, поверхность электронной плотности может использоваться для определения местоположения атомов, подчеркивания электронной плотности, связанной с химическими связями , или для указания общего размера и формы молекулы. [4]
Графически поверхность электронной плотности также служит холстом, на котором могут отображаться другие электронные свойства. Карта электростатического потенциала (свойство электростатического потенциала, отображаемого на электронной плотности) служит индикатором распределения заряда в молекуле. Карта локального потенциала ионизации (свойство локального потенциала ионизации, отображаемое на электронной плотности) является индикатором электрофильности. А карта LUMO ( самая низкая незанятая молекулярная орбиталь, отображаемая на основе электронной плотности) может служить индикатором нуклеофильности. [5]
Определение [ править ]
Электронная плотность, соответствующая нормированному -электронная волновая функция (с и обозначающие пространственную и спиновую переменные соответственно) определяется как [6]
где оператор, соответствующий наблюдаемой плотности, равен
Вычисление как определено выше, мы можем упростить выражение следующим образом.
Другими словами: удержание одного электрона на месте. мы суммируем по всем возможным расположениям других электронов. Коэффициент N возникает, поскольку все электроны неразличимы, и, следовательно, все интегралы имеют одно и то же значение.
В теориях Хартри-Фока и функционала плотности волновая функция обычно представляется как один определитель Слейтера, построенный из орбитали, , с соответствующими профессиями . В этих ситуациях плотность упрощается до
Общие свойства [ править ]
По определению, электронная плотность является неотрицательной функцией, интегрирующейся с общим числом электронов. Далее, для системы с кинетической энергией T плотность удовлетворяет неравенствам [7]
Для конечных кинетических энергий первое (более сильное) неравенство помещает квадратный корень из плотности в пространство Соболева . Вместе с нормализацией и неотрицательностью это определяет пространство, содержащее физически приемлемые плотности как
Второе неравенство помещает плотность в L 3 космос . Вместе со свойством нормализации размещает приемлемые плотности в пределах пересечения L 1 и Л 3 - суперсет .
Топология [ править ]
Предполагается, что электронная основного состояния плотность атома является монотонно убывающей функцией расстояния от ядра . [8]
Состояние ядерного возврата [ править ]
Электронная плотность имеет выступы на каждом ядре молекулы из-за неограниченного электрон-ядерного кулоновского потенциала. Это поведение количественно определяется условием возврата Като, сформулированным в терминах сферически усредненной плотности: , относительно любого данного ядра как [9]
То есть радиальная производная сферически усредненной плотности, оцененная в любом ядре, равна удвоенной плотности в этом ядре, умноженной на отрицательное значение атомного номера ( ).
поведение Асимптотическое
Условие ядерного возврата обеспечивает околоядерное (малое) ) поведение плотности как
Дальняя (большая ) известно также поведение плотности, принимающее вид [10]
где I — энергия ионизации системы.
Плотность ответа [ править ]
Другое более общее определение плотности - это «плотность линейного отклика». [11] [12] Это плотность, которая при сжатиис любым бесспиновым одноэлектронным оператором получается соответствующее свойство, определяемое как производная энергии. Например, дипольный момент является производной энергии по внешнему магнитному полю и не является математическим ожиданием оператора над волновой функцией. Для некоторых теорий они одинаковы, когда волновая функция сходится. Числа занятости не ограничены диапазоном от нуля до двух, и поэтому иногда даже плотность отклика может быть отрицательной в определенных регионах космоса. [13]
Эксперименты [ править ]
Многие экспериментальные методы позволяют измерить электронную плотность. Например, квантовая кристаллография посредством рентгеновского дифракционного сканирования, когда рентгеновские лучи подходящей длины волны направляются на образец и измерения проводятся с течением времени, дает вероятностное представление о местоположении электронов. С этих позиций часто можно определить молекулярные структуры, а также точное распределение плотности заряда для кристаллизованных систем. Квантовая электродинамика и некоторые разделы квантовой теории поля также изучают и анализируют суперпозицию электронов и другие связанные явления, такие как индекс NCI , который позволяет изучать нековалентные взаимодействия с использованием электронной плотности. Анализ населения Малликена основан на плотности электронов в молекулах и представляет собой способ разделения плотности между атомами для оценки атомных зарядов.
В просвечивающей электронной микроскопии (ПЭМ) и глубоконеупругом рассеянии , а также в других экспериментах с частицами высоких энергий электроны высокой энергии взаимодействуют с электронным облаком, что дает прямое представление об электронной плотности. ПЭМ, сканирующая туннельная микроскопия (СТМ) и атомно-силовая микроскопия (АСМ) могут использоваться для исследования электронной плотности конкретных отдельных атомов. [ нужна ссылка ]
Спиновая плотность [ править ]
Спиновая плотность — это электронная плотность применительно к свободным радикалам . Она определяется как общая электронная плотность электронов одного спина минус полная электронная плотность электронов другого спина. Одним из способов его экспериментального измерения является метод электронного спинового резонанса . [14] нейтронная дифракция позволяет напрямую картировать спиновую плотность в трехмерном пространстве.
См. также [ править ]
- Карта плотности различий
- Электронное облако
- Электронная конфигурация
- Разрешение (электронная плотность)
- Плотность заряда
- Теория функционала плотности
- Вероятностный ток
Ссылки [ править ]
- ^ например, белая линия на диаграмме хлорофиллов и каротиноидов. Архивировано 9 августа 2017 г. в Wayback Machine.
- ^ Алан Дж. Шустерман; Гвендолин П. Шустерман (1997). «Преподавание химии с помощью моделей электронной плотности». Журнал химического образования . 74 (7): 771–775. Бибкод : 1997JChEd..74..771S . дои : 10.1021/ed074p771 .
- ^ или, например, программа Spartan от Wavefunction, Inc.
- ^ Уоррен Дж. Хехре; Алан Дж. Шустерман; Джанет Э. Нельсон (1998). Рабочая тетрадь по молекулярному моделированию по органической химии . Ирвин, Калифорния: Волновая функция. стр. 61–86. ISBN 978-1-890661-18-2 .
- ^ Хере, Уоррен Дж. (2003). Руководство по молекулярной механике и квантово-химическим расчетам . Ирвин, Калифорния: Wavefunction, Inc., стр. 85–100. ISBN 978-1-890661-06-9 .
- ^ Парр, Роберт Г.; Ян, Вэйтао (1989). Плотно-функциональная теория атомов и молекул . Нью-Йорк: Издательство Оксфордского университета. ISBN 978-0-19-509276-9 .
- ^ Либ, Эллиот Х. (1983). «Функционалы плотности для кулоновских систем». Международный журнал квантовой химии . 24 (3): 243–277. дои : 10.1002/qua.560240302 .
- ^ Айерс, Пол В.; Парр, Роберт Г. (2003). «Достаточное условие монотонного спада электронной плотности в многоэлектронных системах». Международный журнал квантовой химии . 95 (6): 877–881. дои : 10.1002/qua.10622 .
- ^ Като, Тосио (1957). «О собственных функциях многочастичных систем в квантовой механике». Сообщения по чистой и прикладной математике . 10 (2): 151–177. дои : 10.1002/cpa.3160100201 .
- ^ Моррелл, Мэрилин М.; Парр, Роберт. Г.; Леви, Мел (1975). «Расчет потенциалов ионизации на основе матриц плотности и натуральных функций, а также поведение естественных орбиталей и электронной плотности на больших расстояниях» . Журнал химической физики . 62 (2): 549–554. Бибкод : 1975ЖЧФ..62..549М . дои : 10.1063/1.430509 .
- ^ Хэнди, Николас С.; Шефер, Генри Ф. (1984). «Об оценке аналитических производных энергии для коррелированных волновых функций». Журнал химической физики . 81 (11): 5031–5033. Бибкод : 1984JChPh..81.5031H . дои : 10.1063/1.447489 .
- ^ Виберг, Кеннет Б.; Хадад, Кристофер М.; Лепаж, Тереза Дж.; Бренеман, Курт М.; Фриш, Майкл Дж. (1992). «Анализ влияния электронной корреляции на распределение плотности заряда». Журнал физической химии . 96 (2): 671–679. дои : 10.1021/j100181a030 .
- ^ Гордон, Марк С.; Шмидт, Майкл В.; Чабан Галина М.; Глеземанн, Курт Р.; Стивенс, Уолтер Дж.; Гонсалес, Карлос (1999). «Естественная орбитальная диагностика многоконфигурационного характера коррелированных волновых функций» . Дж. Хим. Физ . 110 (9): 4199–4207. Бибкод : 1999JChPh.110.4199G . дои : 10.1063/1.478301 . S2CID 480255 .
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « Спиновая плотность ». два : 10.1351/goldbook.S05864


























