Убикитин Д
| УБД | ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | UBD , FAT10, GABBR1, UBD-3, убиквитин D | |||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 606050 ; МГИ : 1344410 ; Гомологен : 4665 ; GeneCards : UBD ; ОМА : UBD - ортологи | |||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
Убиквитин D — это белок , который у человека кодируется геном , UBD также известным как FAT10. [5] [6] [7] UBD действует подобно убиквитину , ковалентно модифицируя белки и помечая их для разрушения в протеасоме.
Убикитин
[ редактировать ]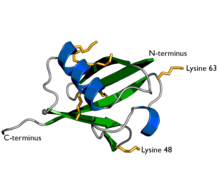
Убиквитин – это белок, состоящий из 76 аминокислот. Чтобы убиквитин мог связываться с другими белками, он должен пройти процесс активации с помощью E1, АТФ-зависимого фермента, активирующего убиквитин. Карбоксильный конец (С-конец) убиквитина связан с остатком цистеина белка Е1 высокоэнергетической тиоэфирной связью и активируется. Эта реакция требует АТФ и протекает через ковалентный промежуточный продукт АМФ-убиквитин.
Важность убиквитина
[ редактировать ]Протеолиз в клетках является важным процессом для предотвращения производства нежелательных или аномальных белков. При деградации белков процесс, при котором протеолитические ферменты действуют АТФ-зависимым образом, преимущественно происходит при деградации белков-субстратов с коротким периодом полураспада. В частности, в эукариотических клетках важную роль в регуляции периода полураспада и функции белков играет процесс протеолиза путем связывания убиквитина, состоящего из 76 аминокислот. [8]
Убиквитин-связывающие ферменты E1, E2 и E3
[ редактировать ]Белки E1, E2 и ферменты E3 необходимы для прикрепления убиквитина к белкам матрикса. Среди них у человека существует только один тип белка Е1, и известно, что это число самое большое.
Известно, что у дрожжей существует около дюжины белков E2 в качестве белков-переносчиков, которые переносят убиквитин от E1 к E3 или субстратам, и было подтверждено, что у высших эукариот существует больше типов, чем у дрожжей. Фермент Е3, также называемый лигазой Е3, представляет собой фермент, который действует на заключительном этапе прикрепления убиквитина к белку-субстрату. Специфичность убиквитинируемого белка-субстрата определяется ферментом Е3.
В частности, ферменты Е3 можно разделить на четыре типа, такие как HECT, RING-finger, U-box и PHD-finger, по методу определения специфичности белка-субстрата. Известно, что среди них фермент E3 RING-пальца лучше всего следует правилу аминоконца. Правило аминоконца означает, что скорость деградации белка, то есть период полураспада белка, варьируется в зависимости от того, какой аминокислотный остаток находится на аминоконце. В аминоконцевом правиле дрожжей известно, что период полураспада белков варьирует в зависимости от наличия 12 нестабильных аминокислотных остатков (аргинин, лизин, гистидин, тирозин, триптофан, изолейцин, аспарагиновая кислота, глутаминовая кислота, аспарагин). , глутамин) из 20 аминокислот. Когда метионин, глицин, серин, валин или пролин расположены на аминоконце, его период полураспада составляет более 20 часов, тогда как когда такие остатки, как тирозин, глутамин, лейцин, фенилаланин, аспартат, лизин или аргинин расположены, период полувыведения сокращается до менее 10 минут. [9]
Активированный убиквитин, связанный с Е1, переносится на цистеиновый остаток молекулы Е2 (убиквитин-конъюгирующий фермент). Молекулы Е2 образуют комплексы с молекулами белка Е3, которые являются вспомогательными белками. В комплексе E2-E3, называемом убиквитинлигазой, компонент E3 связывается со специфическим сигналом деградации в белке-субстрате, а затем фермент E2 помогает сформировать мультиубиквитиновую цепь на остатке лизина белка-субстрата. Чтобы сформировать мультиубиквитиновую цепь, С-концевая область следующей молекулы убиквитина соединяется с остатком лизина предыдущего убиквитина.
В клетках млекопитающих существует около 30 различных E2, и обнаружено более 300 специфических комплексов E2-E3. Благодаря функции компонента E3 они могут распознавать специфические сигналы деградации белков-мишеней. В общем, Е2 называют убиквитин-связывающим ферментом, а Е3 традиционно называют убиквитин-связывающим ферментом. Однако функционально комплекс E2-E3 правильнее называть убиквитинлигазой. Цепи мультиубиквитина на белках-мишенях распознаются специфическими рецепторами протеасомы.
В целом протеасома отвечает за удаление структурно аномальных белков, а также способствует регуляции продолжительности жизни конкретных белков в зависимости от внутриклеточной среды. Например, митотические циклины, необходимые для индукции митоза (или митоза), остаются долгоживущими на протяжении всего клеточного цикла, но предназначены для резкой деградации в конце митоза.
Тогда как же происходит эта регуляция деградации белка? Активация Е3, фермента, связывающего убиквитин, может быть достигнута путем фосфорилирования или аллостерического перехода после связывания лиганда или субъединицы. Например, комплекс, способствующий анафазе (APC), представляет собой мультиубиквитин-связывающий фермент, который активируется во время митоза путем добавления субъединиц в ходе клеточного цикла. Активированный APC способствует протеолизу митотических циклинов и регуляторов позднего метафазного перехода. [10]
УБД
[ редактировать ]UBD был впервые обнаружен в ретикулоэндотелиальных тканях и лимфоидных иммунологических системах, связанных со слизистой оболочкой, как один из генов локуса I класса главного комплекса гистосовместимости человека на хромосоме 6. Ген UBD кодирует белок массой 18 кДа, содержащий N- и C-концы с 29 и 36% идентичности с убиквитином соответственно. Из идентифицированных убиквитиноподобных белков UBD является единственным, который конъюгирует с белками-мишенями посредством мотива свободного диглицина на С-конце и непосредственно направляет нековалентно связанные белки к протеосомной деградации.
UBD также играет важную роль в митозе клеток, нестабильности хромосом, апоптозе и иммунном ответе. Нарушение регуляции UBD может вызывать аномальные изменения апоптоза, деления клеток или нестабильности хромосом, которые связаны с неопластическими изменениями. Экспрессия UBD в опухолях демонстрирует некоторую тканевую специфичность: усиление транскрипции наблюдается при аденокарциномах печени, шейки матки, яичников, поджелудочной железы, желудка и тонкой кишки, но не при раке щитовидной железы, простаты или почек. В клетках рака печени повышенная экспрессия UBD была связана с ядерным антигеном пролиферирующих клеток, маркером клеточной пролиферации, и, как сообщалось, обеспечивало преимущество роста по сравнению с клетками без экспрессии UBD. Высокая экспрессия UBD также способствовала развитию гепатоцеллюлярной карциномы на мышиной модели и образованию телец Мэллори-Денка, которые представляют собой предопухолевые изменения при хроническом заболевании печени. Сверхэкспрессия UBD при раке желудка коррелирует с метастазами и стадией опухоли, а уровни мРНК и белка UBD были идентифицированы как независимые прогностические факторы для этого заболевания. Увеличение UBD также положительно коррелирует с мутантной экспрессией р53, которая может активировать экспрессию UBD и косвенно способствовать прогрессированию рака желудка. Интерферон-γ и фактор некроза опухоли-α действуют синергически, индуцируя промотор UBD через чувствительный к последовательности интерферон элемент. В совокупности эти данные указывают на то, что UBD может быть маркером предраковых поражений и способствовать прогрессированию рака. [11]
Взаимодействия
[ редактировать ]Было показано, что UBD взаимодействует с NUB1. [12] и MAD2L1 . [13]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с ENSG00000231968, ENSG00000206468, ENSG00000206513, ENSG00000224654, ENSG00000213886, ENSG00000226898 GRCh38: Версия ансамбля 89: ENSG00000228913, 0000231968, ENSG00000206468, ENSG00000206513, ENSG00000224654, ENSG00000213886, ENSG00000226898 – ансамбль , май 2017 г.
- ^ Перейти обратно: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000035186 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Бейтс Э.Э., Равель О., Дье М.С., Хо С., Гюре С., Брайдон Дж.М., Айт-Яхья С., Бриер Ф., Ко С., Баншеро Дж. , Лебек С. (октябрь 1997 г.). «Идентификация и анализ нового члена семейства убиквитинов, экспрессируемого в дендритных клетках и зрелых B-клетках». Европейский журнал иммунологии . 27 (10): 2471–7. дои : 10.1002/eji.1830271002 . ПМИД 9368598 . S2CID 21652482 .
- ^ Фан В., Кай В., Паримо С., Шварц Д.К., Леннон Г.Г., Вайсман С.М. (август 1996 г.). «Идентификация семи новых генов области человеческого MHC класса I вокруг локуса HLA-F». Иммуногенетика . 44 (2): 97–103. дои : 10.1007/BF02660056 . ПМИД 8662070 . S2CID 21628804 .
- ^ «Вход в ген: UBD-убиквитин D» .
- ^ «유비퀴틴» . terms.naver.com (на корейском языке) . Проверено 27 апреля 2023 г.
- ^ «유비퀴틴» . terms.naver.com (на корейском языке) . Проверено 27 апреля 2023 г.
- ^ «유비퀴틴» . terms.naver.com (на корейском языке) . Проверено 27 апреля 2023 г.
- ^ Ян Д.В., Ли Д.В., Ян YX, Ся J, Ван XL, Чжоу CZ, Фань JW, Вэнь Ю.Г., Сунь ХК, Ван Q, Цю GQ, Тан HM, Пэн Чж. (сентябрь 2010 г.). «Убиквитин D коррелирует с прогрессированием рака толстой кишки и предсказывает рецидив заболевания на стадии II-III после радикального хирургического вмешательства» . Британский журнал рака . 103 (7): 961–969. дои : 10.1038/sj.bjc.6605870 . ISSN 1532-1827 . ПМЦ 2965875 . ПМИД 20808312 .
- ^ Хипп М.С., Рааси С., Гроеттруп М., Шмидтке Г. (апрель 2004 г.). «NEDD8 Ultimate Buster-1L взаимодействует с убиквитиноподобным белком FAT10 и ускоряет его деградацию» . Журнал биологической химии . 279 (16): 16503–10. дои : 10.1074/jbc.M310114200 . ПМИД 14757770 .
- ^ Лю Ю.К., Пань Дж., Чжан С., Фань В., Коллиндж М., Бендер-младший, Вайсман С.М. (апрель 1999 г.). «Убиквитиноподобный белок (FAT10), кодируемый MHC, нековалентно связывается с белком контрольной точки сборки веретена MAD2» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (8): 4313–8. Бибкод : 1999PNAS...96.4313L . дои : 10.1073/pnas.96.8.4313 . ЧВК 16329 . ПМИД 10200259 .
Дальнейшее чтение
[ редактировать ]- Мацце FM, Дегрев Л. (2006). «Роль вирусных и клеточных белков в почковании вируса иммунодефицита человека». Акта вирусологика . 50 (2): 75–85. ПМИД 16808324 .
- Отт Д.Е., Корен Л.В., Коупленд Т.Д., Кейн Б.П., Джонсон Д.Г., Соудер Р.К., Йошинака Ю., Орослан С., Артур Л.О., Хендерсон Л.Е. (апрель 1998 г.). «Убиквитин ковалентно связан с белками p6Gag вируса иммунодефицита человека типа 1 и вируса иммунодефицита обезьян, а также с белком p12Gag вируса мышиного лейкоза Молони» . Журнал вирусологии . 72 (4): 2962–8. doi : 10.1128/JVI.72.4.2962–2968.1998 . ПМК 109742 . ПМИД 9525617 .
- Лю Ю.К., Пань Дж., Чжан С., Фань В., Коллиндж М., Бендер-младший, Вайсман С.М. (апрель 1999 г.). «Убиквитиноподобный белок (FAT10), кодируемый MHC, нековалентно связывается с белком контрольной точки сборки веретена MAD2» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (8): 4313–8. Бибкод : 1999PNAS...96.4313L . дои : 10.1073/pnas.96.8.4313 . ЧВК 16329 . ПМИД 10200259 .
- Шуберт У, Отт Д.Е., Чертова Е.Н., Велкер Р., Тессмер У., Принчотта М.Ф., Беннинк Дж.Р., Краусслих Х.Г., Юделл Дж.В. (ноябрь 2000 г.). «Ингибирование протеасом препятствует процессингу, высвобождению и созреванию полипротеина gag, а также созреванию ВИЧ-1 и ВИЧ-2» . Труды Национальной академии наук Соединенных Штатов Америки . 97 (24): 13057–62. Бибкод : 2000PNAS...9713057S . дои : 10.1073/pnas.97.24.13057 . ПМК 27177 . ПМИД 11087859 .
- Страк Б, Калистри А, Аккола М.А., Палу Г., Готтлингер Х.Г. (ноябрь 2000 г.). «Роль рекрутирования убиквитинлигазы в высвобождении ретровирусов» . Труды Национальной академии наук Соединенных Штатов Америки . 97 (24): 13063–8. Бибкод : 2000PNAS...9713063S . дои : 10.1073/pnas.97.24.13063 . ПМК 27178 . ПМИД 11087860 .
- Отт Д.Е., Корен Л.В., Чертова Е.Н., Гальярди Т.Д., Шуберт У. (декабрь 2000 г.). «Убиквитинирование ВИЧ-1 и MuLV Gag» . Вирусология . 278 (1): 111–21. дои : 10.1006/виро.2000.0648 . ПМИД 11112487 .
- Страк Б, Калистри А, Гёттлингер Х.Г. (июнь 2002 г.). «Функция домена поздней сборки может проявлять контекстную зависимость и включать остатки убиквитина, участвующие в эндоцитозе» . Журнал вирусологии . 76 (11): 5472–9. doi : 10.1128/JVI.76.11.5472-5479.2002 . ПМК 137019 . ПМИД 11991975 .
- Отт Д.Э., Корен Л.В., Соудер Р.К., Адамс Дж., Шуберт У. (март 2003 г.). «Ретровирусы предъявляют разные требования к функции протеасом в процессе почкования» . Журнал вирусологии . 77 (6): 3384–93. doi : 10.1128/JVI.77.6.3384-3393.2003 . ПМК 149504 . ПМИД 12610113 .
- Ли К.Г., Рен Дж., Чонг И.С., Пан К.Х., Оой Л.Л., Ён Тан С., Кан А., Нучпраюн И., Джин Р., Ли К.Х., Чоти М., Ли Л.А. (май 2003 г.). «Экспрессия гена FAT10 сильно повышается при гепатоцеллюлярной карциноме и других желудочно-кишечных и гинекологических раковых заболеваниях» . Онкоген . 22 (17): 2592–603. дои : 10.1038/sj.onc.1206337 . ПМИД 12730673 .
- Брес В., Кирнан Р.Э., Линарес Л.К., Шабле-Бессиа С., Плечакова О., Треанд С., Эмилиани С., Пелопонез Ж.М., Жанг К.Т., Ку О., Шеффнер М., Бенкиран М. (август 2003 г.). «Непротеолитическая роль убиквитина в Tat-опосредованной трансактивации промотора ВИЧ-1». Природная клеточная биология . 5 (8): 754–61. дои : 10.1038/ncb1023 . ПМИД 12883554 . S2CID 8414608 .
- Хипп М.С., Рааси С., Гроеттруп М., Шмидтке Г. (апрель 2004 г.). «NEDD8 Ultimate Buster-1L взаимодействует с убиквитиноподобным белком FAT10 и ускоряет его деградацию» . Журнал биологической химии . 279 (16): 16503–10. дои : 10.1074/jbc.M310114200 . ПМИД 14757770 .
- Барриос-Родилес М, Браун КР, Оздамар Б, Бозе Р, Лю З, Донован Р.С., Синдзё Ф, Лю Ю, Дембови Дж, Тейлор И.В., Луга В., Пржуль Н., Робинсон М., Сузуки Х., Хаяшизаки Ю., Юришица И., Врана Дж.Л. (март 2005 г.). «Высокопроизводительное картирование динамической сигнальной сети в клетках млекопитающих». Наука . 307 (5715): 1621–5. Бибкод : 2005Sci...307.1621B . дои : 10.1126/science.1105776 . ПМИД 15761153 . S2CID 39457788 .
- Хипп М.С., Калверам Б., Рааси С., Гроттруп М., Шмидтке Г. (май 2005 г.). «FAT10, убиквитин-независимый сигнал протеасомной деградации» . Молекулярная и клеточная биология . 25 (9): 3483–91. дои : 10.1128/MCB.25.9.3483-3491.2005 . ПМЦ 1084302 . ПМИД 15831455 .
- Готтвейн Э., Кроусслих Х.Г. (июль 2005 г.). «Анализ Gag-убиквитинирования вируса иммунодефицита человека типа 1» . Журнал вирусологии . 79 (14): 9134–44. doi : 10.1128/JVI.79.14.9134-9144.2005 . ПМЦ 1168789 . ПМИД 15994808 .
- Руал Дж.Ф., Венкатесан К., Хао Т., Хиродзан-Кисикава Т., Дрико А., Ли Н., Берриз Г.Ф., Гиббонс Ф.Д., Дрезе М., Айви-Гедехуссу Н., Клитгорд Н., Саймон С., Боксем М., Мильштейн С., Розенберг Дж., Голдберг Д.С., Чжан Л.В., Вонг С.Л., Франклин Г., Ли С., Альбала Дж.С., Лим Дж., Фротон С., Лламосас Е., Чевик С., Бекс С., Ламеш П., Сикорски Р.С., Ванденхаут Дж., Зогби Х.И., Смоляр А., Босак С., Секерра Р., Дусетт-Стамм Л., Кьюсик М.Е., Хилл Д.Е., Рот Ф.П., Видал М. (октябрь 2005 г.). «К карте сети белок-белковых взаимодействий человека в масштабе протеома». Природа . 437 (7062): 1173–8. Бибкод : 2005Natur.437.1173R . дои : 10.1038/nature04209 . ПМИД 16189514 . S2CID 4427026 .



