Манганат
В неорганической номенклатуре мангагат представляет собой любую отрицательно заряженную молекулярную сущность с марганцем в качестве центрального атома. [ 1 ] Тем не менее, название обычно используется для обозначения аниона тетраоксидоманганата (2-) , MNO 2−
4 , также известный как Manganate (VI) , потому что он содержит марганец в состоянии окисления +6 . [ 1 ] Мангататы - единственные известные соединения марганца (VI). [ 2 ]
Другие мангататы включают гипоманганат или мангагат (V), MNO 3−
4 , Peranganate или Manganaate (VII), MNO −
4 , и диманганат или диманганат (iii) mn
2 o 6−
6 .
Manganate (iv) анион Mno 4−
4 был получен радиолизом разбавленных растворов перманганата . [ 3 ] [ 4 ] Он является мононуклеарным в разбавленном растворе и показывает сильное поглощение ультрафиолета и более слабое поглощение при 650 нм. [ 3 ]
Структура
[ редактировать ]
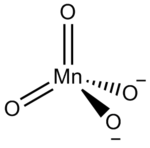
Ион мангагата (VI) тетраэдричен, похож на сульфат или хромат: действительно, мангататы часто являются изоструктурными с сульфатами и хроматами, факт, впервые отмеченный Эйлардом Мицшерлихом в 1831 году. [ 5 ] Марганец в - расстояние кислорода составляет 165,9 вечера, примерно в 3 часа дня длиннее, чем перманганате . [ 5 ] Как объявление 1 Ион, это парамагнитно , но любое искажение Jahn-Teller слишком мала, чтобы их можно было обнаружить с помощью рентгеновской кристаллографии . [ 5 ] Мангататы темно -зеленый цвет, с видимым максимумом поглощения λ max = 606 нм ( ε = 1710 дм 3 мол −1 см −1 ). [ 6 ] [ 7 ] Спектр комбинационного рассеяния также был зарегистрирован. [ 8 ]
Подготовка
[ редактировать ]Мангаты натрия и калия обычно готовится в лаборатории путем перемешивания эквивалентного перманганата в концентрированном растворе (5–10 м) гидроксида в течение 24 часов [ 6 ] или с нагревом. [ 9 ]
- 4 слишком много −
4 + 4 Ох − → 4 слишком много 2−
4 + 2 H 2 O + O 2
Мангатат калия готовится промышленно, в качестве промежуточного до перманганата калия путем растворения диоксида марганца в гидроксиде расплавленного калия с нитратом или воздухом калия в качестве окислителя . [ 2 ]
- 2 Mno 2 + 4 OH − + O 2 → 2 mno 2−
4 + 2 H 2 O
Диспропорция
[ редактировать ]Мангататы нестабильны к диспропорции во всех, кроме самых щелочных водных растворов . [ 2 ] Конечными продуктами являются перманганат и диоксид марганца , но кинетика сложна, а механизм может включать протонированные и/или марганцевые (V) виды. [ 10 ] [ 11 ]
Использование
[ редактировать ]Мангаты, в частности нерастворимый барий манганат , Bamno 4 , использовались в качестве окислительных агентов в органическом синтезе : они будут окислять первичные спирты до альдегидов , а затем до карбоновых кислот и вторичные спирты в кетоны . [ 12 ] [ 13 ] Barium Manganate также использовался для окисления гидразонов до соединений Diazo . [ 14 ]
Связанные соединения
[ редактировать ]Манганат формально является конъюгатной основой гипотетической магганной кислоты H
2 мно
4 , который не может быть сформирован из -за его быстрой диспропорции. Тем не менее, его вторая константа диссоциации кислоты была оценена методами импульсного радиолиза : [ 3 ]
- HMNO −
4 ⇌ слишком много 2−
4 + h + p k a = 7,4 ± 0,1
Мангагаты
[ редактировать ]Название « Мангарит » используется для соединений, которые, как считалось, содержат анион MNO 3−
3 , с марганцем в состоянии +3 окисления. Тем не менее, большинство из этих «манганитов» не содержат отдельных оксианионов , но являются смешанными оксидами с перовскитом (LAMN Iii O 3 , Camn IV O 3 ), Spinel (Limn III, iv
2 O 4 ) или хлорид натрия (LIMN Iii O 2 , имя Iii O 2 ) Структуры.
Единственным исключением является калийманганат (III) , K 6 мн 2 O 6 , который содержит дискретный Mn 2 O 6−
6 анионов. [ 15 ]
Ссылки
[ редактировать ]- ^ Jump up to: а беременный Международный союз чистой и прикладной химии (2005). Номенклатура неорганической химии (рекомендации IUPAC 2005). Кембридж (Великобритания): RSC - Iupac . ISBN 0-85404-438-8 . С. 74–75, 77–78, 313, 338. Электронная версия. Полем
- ^ Jump up to: а беременный в Коттон, Ф. Альберт ; Wilkinson, Geoffrey (1980), Advanced Inorganic Chemistry (4 -е изд.), Нью -Йорк: Wiley, p. 746, ISBN 0-471-02775-8 .
- ^ Jump up to: а беременный в Раш, JD; Bielski, BHJ (1995), «Исследования мангагата (v), -(vi) и -(vii) тетраоксианионов пульс -радиолизом. Оптические спектры протонированных форм», Inorg. Химический , 34 (23): 5832–38, doi : 10.1021/ic00127a022
- ^ Ли, Дональд Дж.; Чен, Тао (1989), «Окисление углеводородов. 18. Механизм реакции между перманганатными и углеродными двойными связями», J. Am. Химический Соц , 111 (19): 7534–38, doi : 10.1021/ja00201a039 .
- ^ Jump up to: а беременный в Palenik, Gus J. (1967), «Кристаллическая структура манганата калия», Inorg. Химический , 6 (3): 507–11, doi : 10.1021/ic50049a016 .
- ^ Jump up to: а беременный Carrington, A.; Symons, MCR (1956), «Структура и реакционная способность окси-анионов переходных металлов. Часть I. Манганец окси-анионы», J. Chem. Соц : 3373–80, doi : 10.1039/jr9560003373
- ^ Ли, Дональд Дж.; Chen, Tao (1993), «Снижение мангагата (VI) по мандельной кислоте и его значение для развития общего механизма датиоксина органических соединений с помощью высоковалентных оксидов переходных металлов», J. Am. Химический Соц , 115 (24): 11231–36, doi : 10.1021/ja00077a023 .
- ^ Юберта, ах; Вареттия, Эл (1982), «Нормальные и резонансные комбинационные спектры некоторых мангататов», J. Mol. Структура , 79 1–2): 285–88 bibcode : 1982j . ( , Большинство
- ^ Nyholm, Rs ; Woolliams, PR (1968), "Manganates (VI)", Inorg. Синтезатор , 11 : 56–61
- ^ Саттер, Джоан Х.; Colquitt, Кевин; Саттер, Джон Р. (1974), «Кинетика диспропорции мангагата в кислотном растворе», Inorg. Химический , 13 (6): 1444–46, doi : 10.1021/ic50136a037 .
- ^ Sekula-Brzezińska, K.; Wrona, PK; Galus, Z. (1979), «скорость MNO 4 − /Mno 4 2− и Mno 4 2− /Mno 4 3− Реакции электродов в щелочных растворах у твердых электродов », Electrochim. Acta , 24 (5): 555–63, doi : 10.1016/0013-4686 (79) 85032-x .
- ^ Procter, G.; Лей, SV; Castle, GH (2004), "Barium Manganate", в Paquette, L. (ed.), Энциклопедия реагентов для органического синтеза , Нью -Йорк: Wiley, doi : 10.1002/047084289x , HDL : 10261/236866 , ISBN , 9780471936237 .
- ^ Firouzabadi, Habib; Mashafavipoor, Zohreh (1983), «Синтез», Bull . Химический Соц JPN , 56 (3): 914–17, doi : 10,1246/bcsj.56,914 .
- ^ Guziec, Frank S. Jr.; Мерфи, Кристофер Дж.; Каллен, Эдвард Р. (1985), «Тепловые и фотохимические исследования симметричных и несимметричных дигидро-1,3,4-селенадозолов», J. Chem. Soc., Perkin Trans. 1 : 107–13, doi : 10.1039/p19850000107
- ^ Brachtel, G.; Hoppe, R. (1976), «Первый оксоманганат (III) со структурой острова: K 6 [Mn 2 O 6 ]», Natural Sciences , 63 (7): 339, Bibcode : 1976nw ..... 63 .. 39b , doi : 10.1007/bf00597313 , s2cid 45344152 .