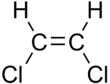
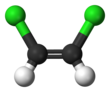
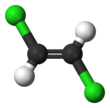
1,2-Дихлорэтилен
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК 1,2-Дихлорэтен | |||
| Другие имена 1,2-Дихлорэтен 1,2-ДКЭ Ацетилена дихлорид сим -Дихлорэтилен | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ЧЭБИ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.007.956 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
ПабХим CID | |||
| НЕКОТОРЫЙ |
| ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 2 Н 2 Cl 2 | |||
| Молярная масса | 96.95 g/mol | ||
| Появление | бесцветная жидкость | ||
| Запах | сладкий [1] | ||
| Плотность | Z : 1,28 г/см 3 Е : 1,26 г/см 3 | ||
| Температура плавления | Z : −81,47 °С Е : −49,44 °С | ||
| Точка кипения | З : 60,2 °С Е : 48,5°С | ||
| |||
| З : 1,9 Д Э : 0 Д | |||
| Опасности | |||
| точка возгорания | 2–4 °С; 36–39 ° F; 275–277 К | ||
| Взрывоопасные пределы | 5.6–12.8% [2] | ||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза ) | 770 мг/кг (перорально, крыса) 1275 мг/кг (перорально, крыса, транс -изомер) [3] | ||
ЛК 50 ( средняя концентрация ) | 21 273 м.д. (мышь, 6 часов, транс -изомер) [3] | ||
LC Lo ( самый низкий из опубликованных ) | 16000 м.д. (крыса, 6 часов, цис -изомер) [3] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
МЕХ (Допускается) | СВВ 200 частей на миллион (790 мг/м 3 ) [2] | ||
РЕЛ (рекомендуется) | СВВ 200 частей на миллион (790 мг/м 3 ) [2] | ||
IDLH (Непосредственная опасность) | 1000 частей на миллион [2] | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
1,2-Дихлорэтилен или 1,2-ДХЭ — название пары хлорорганических соединений с молекулярной формулой С 2 Н 2 Cl 2 . Оба соединения представляют собой изомеры, каждое из которых представляет собой бесцветную жидкость со сладким запахом. Он может существовать в виде одного из двух геометрических изомеров : цис -1,2-дихлорэтена или транс -1,2-дихлорэтена, но часто используется в виде их смеси. Они имеют умеренную растворимость в воде. Эти соединения имеют некоторые применения в качестве обезжиривающего растворителя. [1] В отличие от большинства цис-транс -соединений , Z -изомер ( цис ) более стабилен, чем E -изомер ( транс ) на 0,4 ккал/моль. [4]
Производство, использование и реакции
[ редактировать ]цис -ДХЭ, Z , можно получить контролируемым хлорированием ацетилена - изомер :
- C 2 H 2 + Cl 2 → C 2 H 2 Cl 2
В промышленности оба изомера возникают как побочные продукты производства винилхлорида , который производится в огромных масштабах. В отличие от 1,1-дихлорэтилена изомеры 1,2-дихлорэтилена не полимеризуются. [1]
транс -1,2-DCE находит применение в очистке электроники, прецизионной очистке и некоторых видах очистки металлов. [5]
Оба изомера участвуют в реакциях сочетания Кумады . транс -1,2-Дихлорэтилен участвует в реакциях циклоприсоединения . [6]
Проблемы безопасности и окружающей среды
[ редактировать ]Эти соединения обладают «умеренной пероральной токсичностью для крыс». [1]
Изомеры дихлорэтилена встречаются в некоторых загрязненных водах и почвах как продукты разложения трихлорэтилена . Значительное внимание уделялось их дальнейшей деградации, например, частицами железа. [7] [8]
См. также
[ редактировать ]- 1,1-Дихлорэтен
- 1,2-Дихлорэтан , который также часто обозначают сокращенно 1,2-ДХЭ.
Ссылки
[ редактировать ]- ^ Jump up to: а б с д Э.-Л. токарь; Т.Р. Торкельсон; К.К. Сумка (2011). «Хлорэтаны и хлорэтилены». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.o06_o01 . ISBN 978-3527306732 .
- ^ Jump up to: а б с д и Карманный справочник NIOSH по химическим опасностям. «#0195» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Jump up to: а б с «1,2-Дихлорэтилен» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Питцер, Кеннет С.; Холленберг, Дж. Л. (1954). Цис- . и транс -дихлорэтилены. Инфракрасные спектры 130–400 См –1 и термодинамические свойства». J. Am. Chem. Soc . 76 (6): 1493–1496. doi : 10.1021/ja01635a010 .
- ^ «Хлорированные растворители и сырье - Axiall» . Архивировано из оригинала 8 апреля 2016 г. Проверено 23 марта 2016 г.
- ^ Ван, Сяо Минь; Хоу, Сюэлун; Чжоу, Чжунюань; Мак, Томас CW; Вонг, Генри, Северная Каролина (1993). «Синтез арена реакцией экструзии. 16. Компланарные и стабильные производные 13,14-дидегидро-трибензо[а,с,е]циклооктена: Синтез 5,6-дидегидро-1,1,14,14-тетраметил-10, 11-метано-1Н-бензо[5,6]циклоокта[1,2,3,4-деф]флуорен и 5,6-дидегидро-10,11-метано-1Н-бензо[5,6]циклоокта[1, 2,3,4-def]флуорен-1,14-дион и рентгеноструктурные кристаллические структуры 1,1,14,14-тетраметил-10,11-метано-1H-бензо[5,6-циклоокта[1, 2,3,4-def]флуорен и 1,12-дигидро-1,1,12,12-тетраметилдициклопента[def,JKL]тетрафенилен». Журнал органической химии . 58 (26): 7498–7506. дои : 10.1021/jo00078a031 .
- ^ Мэттс, Тимоти Э.; Александр, Энн К.; Коулман, Николас В. (2010). «Аэробное биоразложение хлорэтенов: пути, ферменты, экология и эволюция» . Обзоры микробиологии FEMS . 34 (4): 445–475. дои : 10.1111/j.1574-6976.2010.00210.x . ПМИД 20146755 .
- ^ Шрик, Беттина; Блау, Дженнифер Л.; Джонс, А. Дэниел; Маллук, Томас Э. (2002). «Гидродехлорирование трихлорэтилена до углеводородов с использованием биметаллических наночастиц никель-железо». Химия материалов . 14 (12): 5140–5147. дои : 10.1021/cm020737i .
Внешние ссылки
[ редактировать ]- Международная карта химической безопасности 0436
- Карманный справочник NIOSH по химическим опасностям. «#0195» . Национальный институт охраны труда и здоровья (NIOSH).