Тетрасульфид натрия
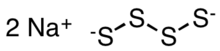 | |
| Имена | |
|---|---|
| Название ИЮПАК Тетрасульфид натрия | |
| Другие имена динатрийтетрасульфид, сульфид натрия | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.031.628 |
| Номер ЕС |
|
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| № 2 С 4 | |
| Молярная масса | 174,24 г/моль |
| Появление | Темно-красная, слегка вязкая жидкость или желтый кристаллический порошок. |
| Плотность | 1,268 г/см 3 при 15,5 °С |
| Температура плавления | 275 ° С (527 ° F; 548 К) |
| Растворим в воде | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Стабилен при комнатной температуре, но может стать взрывоопасным при нагревании. Реакции с кислотами или окислителями приводят к образованию газообразных побочных продуктов, которые могут быть опасны при вдыхании. |
| СГС Маркировка : | |
    | |
| Опасность | |
| Х228 , Х301 , Х311 , Х314 , Х400 | |
| P210 , P240 , P241 , P260 , P264 , P270 , P273 , P280 , P301+P310 , P301+P330+P331 , P302+P352 , P303+P361+P353 , P304+P340 , P305+P351+ П338 , П310 , П312 , P321 , P322 , P330 , P361 , P363 , P370+P378 , P391 , P405 , P501 | |
| NFPA 704 (огненный алмаз) | |
| Непригодный | |
| Паспорт безопасности (SDS) | [1] [1] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Тетрасульфид натрия — неорганическое соединение формулы Na 2 S 4 . Это желто-оранжевое твердое вещество, растворяющееся в воде путем гидролиза. [2] Это предшественник некоторых специальных полимеров и промежуточных продуктов в прототипах натриево-серной батареи .
Синтез и структура
[ редактировать ]Его получают в результате реакции элементарной серы и гидросульфида натрия в спиртовом растворе: [3]
- 2НаШ + 4 S → Na 2 S 4 + H 2 S
Полисульфид-анионы образуют зигзагообразные цепочки атомов серы. Расстояния SS составляют около 2,05 Å, а двугранные углы SSSS составляют около 90°. [4]
Реакции и применение
[ редактировать ]При обработке кислотой он превращается в сероводород и элементарную серу. Обработка алкилирующими агентами дает органические полисульфиды. В одном коммерческом применении его используют для производства сшивающего агента бис(триэтоксисилилпропил)тетрасульфида : [5]
- Na 2 S 4 + 2 ClC 3 H 6 Si(OEt) 3 → S 4 [C 3 H 6 Si(OEt) 3 ] 2 + 2 NaCl
Иногда в смеси с другими полисульфидами тетрасульфид натрия используется для получения полимера, называемого тиоколом. Реакция включает алкилирование этиленхлоридом :
- Na 2 S 4 + C 2 H 4 Cl 2 → 1/n (C 2 H 4 )S x ] n + 2 NaCl
Эти материалы, имеющие приблизительную формулу (C 2 H 4 )S x ] n (x ~ 4), обладают высокой устойчивостью к разложению растворителями и кислотами. [6]
Ссылки
[ редактировать ]- ^ «Паспорт безопасности тетрасульфида натрия» (PDF) . Пфальц и Бауэр. Архивировано из оригинала (PDF) 3 марта 2016 г. Проверено 17 ноября 2013 г.
- ^ Справочник по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, Нью-Йорк. Том. 1. п. 365.
- ^ ДР Кисть (2000). «Сульфиды натрия». Энциклопедия химической технологии Кирка-Отмера . дои : 10.1002/0471238961.1915040902211908.a01 . ISBN 0471238961 .
- ^ Р. Тегман «Кристаллическая структура тетрасульфида натрия Na 2 S 4 » Acta Crystallogr. (1973). Б29, 1463-1469 гг. дои : 10.1107/S0567740873004735
- ^ Турн, Фридрих; Мейер-Симон, Ойген; Мишель, Рудольф «Процесс производства кремнийорганических соединений (Непрерывное производство бис[3-(триэтоксисилил)пропил]тетрасульфида)» Ger. (1973), DE 2212239 А1 19731004.
- ^ Сульфиды, полисульфиды и сульфаны» в Энциклопедии промышленной химии Ульмана, Людвиг Ланге и Вольфганг Трибель, 2000, Wiley-VCH, Вайнхайм. два : 10.1002/14356007.a25_443
