ванадат

В химии ванадат анионный координационный комплекс ванадия — . Часто ванадат относится к оксоанионам ванадия , большинство из которых существуют в высшей степени окисления +5. Комплексы [В(CN) 6 ] 3− и [В 2 Кл 9 ] 3− обозначаются как гексацианованадат(III) и нонахлордиванадат(III) соответственно.
Простой ион ванадата представляет собой тетраэдрический ортованадат-анион, VO 3− 4 (который также называют ванадатом(V)), который присутствует, например, в ортованадате натрия и в растворах V 2 O 5 в сильном основании ( pH > 13 [ 1 ] ). Условно этот ион представляют с одинарной двойной связью, однако это резонансная форма , поскольку ион представляет собой правильный тетраэдр с четырьмя эквивалентными атомами кислорода.
Кроме того, существует ряд ионов полиоксованадата, которые включают дискретные ионы и «бесконечные» полимерные ионы. [ 2 ] Существуют также ванадаты, такие как ванадат родия, RhVO 4 , имеющий статистическую рутиловую структуру, в которой резус 3+ и V 5+ ионы случайным образом занимают Из 4+ позиции в решетке рутила, [ 3 ] которые не содержат решетки катионов и уравновешивающих ванадат-анионов, а представляют собой смешанные оксиды .
В химической номенклатуре, когда ванадат является частью названия, это указывает на то, что соединение содержит анион с центральным атомом ванадия, например гексафторованадат аммония является общим названием соединения. [NH 4 ] 3 [VF 6 ] с названием IUPAC гексафторидованадат(III) аммония.
Примеры ионов оксованадата
[ редактировать ]Некоторые примеры дискретных ионов:
- VO 3− 4 «ортованадат», тетраэдрический. [ 2 ]
- V 2 O 4− 7 «пированадат», общий угол Тетраэдры VO 4 , подобные дихромат- иону [ 2 ]
- V 3 O 3− 9 , циклический с общим углом VO 4 тетраэдры [ 4 ]
- V 4 O 4− 12 , циклический с общим углом VO 4 тетраэдры [ 5 ]
- V 5 O 3− 14 , общий угол VO 4 тетраэдры [ 6 ]
- V 6 O 6− 18 , кольцо. [ 7 ]
- V 10 O 6− 28 «деканадат», общий край и угол ВО 6 октаэдров [ 2 ]
- В 12 О 4− 32
- В 13 О 3− 34 , плавленый ВО 6 октаэдров [ 8 ]
- В 18 О 12− 42 [ 9 ]
Некоторые примеры полимерных «бесконечных» ионов:
 |
 |
 |
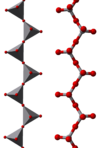
метаванадатные цепи
|
В 5 О 14
|
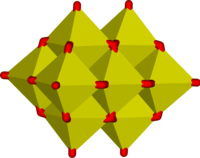
декаванадат-ион
|
В этих ионах ванадий проявляет тетраэдрическую, квадратно-пирамидальную и октаэдрическую координацию. В этом отношении ванадий обнаруживает сходство с вольфраматом и молибдатом , тогда как хром, однако, имеет более ограниченный набор ионов.
Водные растворы
[ редактировать ]Растворение пятиокиси ванадия в сильноосновном водном растворе дает бесцветный VO 3− 4 ион. При подкислении цвет этого раствора постепенно темнеет от оранжевого до красного при pH около 7. Коричневый гидратированный V2O5 выпадает в осадок при pH 2, повторно растворяясь с образованием светло-желтого раствора, содержащего [VO 2 (H 2 O) 4 ] + ион. Количество и идентичность оксианионов, существующих при pH от 13 до 2, зависят от pH, а также от концентрации. Например, протонирование ванадата инициирует серию конденсаций с образованием ионов полиоксованадата: [ 2 ]
- pH 9–12: ХВО 2- 4 , В 2 О 4− 7
- pH 4–9: Ч 2 ВО - 4 , В 4 О 4− 12 , ВВ 10 О 5− 28
- pH 2–4: Ч 3 ВО 4 , Ч 2 В 10 О 4– 28
Фармакологические свойства
[ редактировать ]Ванадат является мощным ингибитором некоторых АТФаз плазматической мембраны , таких как Na. + /К + -АТФаза и Са 2+ -АТФаза ( PMCA ). Действуя как аналог фосфата в переходном состоянии, ванадат подвергается нуклеофильной атаке со стороны воды во время переноса фосфорила, по существу «захватывая» АТФазы P-типа в их фосфорилированном состоянии E2. [ 11 ] [ 12 ] Он также ингибирует активность актомиозина MgATPазы скелетных мышц. [ 13 ] и активируемая кальцием генерация силы актомиозином в сократительном аппарате интактных скелетных мышц. [ 14 ] Однако он не ингибирует другие АТФазы, такие как SERCA (сарко/эндоплазматический ретикулум Ca). 2+ -АТФаза) или митохондриальная АТФаза. [ 15 ] [ 16 ] [ 17 ]
Ссылки
[ редактировать ]- ^ Коттон, Ф. Альберт ; Уилкинсон, Джеффри ; Мурильо, Карлос А.; Бохманн, Манфред (1999), Передовая неорганическая химия (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5
- ^ Перейти обратно: а б с д и ж Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Уэллс А.Ф. (1984) Структурная неорганическая химия, 5-е издание Oxford Science Publications ISBN 0-19-855370-6
- ^ Гамильтон Э.Э.; Фанвик ЧП; Уилкер Джей Джей (2002). «Неуловимый Ванадат (V 3 O 9 ) 3− : Изоляция, кристаллическая структура и поведение неводного раствора» . J. Am. Chem. Soc. 124 (1): 78–82. doi : 10.1021/ja010820r . PMID 11772064 .
- ^ Г.-Ю. Ян, Д.-В. Гао, Ю. Чен, Ж.-К. Сюй, Q.-X. Цзэн, Х.-Р. Сунь, З.-В. Пей, Ц. Су, Ю. Син, Ю.-Х. Линг и H.-Q. Цзя (1998). «[Ni(C 10 H 8 N 2 ) 3 ]2[V 4 O 12 ]·11H 2 O». Акта Кристаллографика C. 54 (5): 616–618. Бибкод : 1998AcCrC..54..616Y . дои : 10.1107/S0108270197018751 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ День Фольксвагена; Уолтер Г. Клемперер ; ОМ Яги (1989). «Новый тип структуры в химии полиоксоанионов: синтез и строение V
5 О 3−
14 анион». J. Am. Chem. Soc. 111 (12): 4518. doi : 10.1021/ja00194a068 . - ^ Гуан-Чуань Оу.; Лун Цзян; Сяо-Лун Фэн; Тонг-Бу Лу (2009). «Макроциклические металлокомплексы ванадия с полиоксоанион-мостиковыми связями: от одномерных к трехмерным структурам». Транзакции Далтона . 1 (1): 71–76. дои : 10.1039/B810802A . ПМИД 19081973 . S2CID 35209358 .
- ^ Хоу Д.; Хаген К.Д.; Хилл КЛ (1992). «Тридекаванадат, [V 13 O 34 ] 3− , новый изополиванадат с высоким потенциалом». J. Am. Chem. Soc. 114 (14): 5864. doi : 10.1021/ja00040a061 .
- ^ Мюллер А.; Сессоли Р.; Крикемейер Э.; Бёгге Х.; Мейер Дж.; Гаттески Д.; Парди Л.; Вестфаль Дж.; Ховемайер К.; Ролфинг Р.; Деринг Дж; Хелльвег Ф.; Бегхольт К.; Шмидтманн М. (1997). «Полиоксованадаты: высокоядерные спиновые кластеры с интересными системами хозяин-гость и различными популяциями электронов. Синтез, спиновая организация, магнитохимия и спектроскопические исследования». Неорг. хим. 36 (23): 5239. doi : 10.1021/ic9703641 .
- ^ Жуанно, С.; Вербар, А.; Гайомар, Д. (2003). «О новом ванадате кальция: синтез, структура и поведение внедрения Li». Журнал химии твердого тела . 172 (1): 116–122. Бибкод : 2003JSSCh.172..116J . дои : 10.1016/S0022-4596(02)00164-0 .
- ^ Кюльбрандт, Вернер (апрель 2004 г.). «Биология, структура и механизм АТФаз Р-типа». Обзоры природы. Молекулярно-клеточная биология . 5 (4): 282–295. дои : 10.1038/nrm1354 . ISSN 1471-0072 . ПМИД 15071553 . S2CID 24927167 .
- ^ Дэвис, Дуглас Р.; Хол, Вим Дж.Дж. (19 ноября 2004 г.). «Сила ванадата в кристаллографических исследованиях ферментов, переносящих фосфорил» . Письма ФЭБС . 577 (3): 315–321. дои : 10.1016/j.febslet.2004.10.022 . ISSN 0014-5793 . ПМИД 15556602 .
- ^ Гудно, CC; Тейлор, EW (1982). «Ингибирование актомиозиновой АТФазы ванадатом» . Труды Национальной академии наук США . 79 (1): 21–25. Бибкод : 1982ПНАС...79...21Г . дои : 10.1073/pnas.79.1.21 . ПМЦ 345653 . ПМИД 6459580 .
- ^ Уилсон, Дж.Дж.; Шулл, SE; Кук, Р. (1995). «Подавление мышечной силы ванадатом» . Биофизический журнал . 68 (1): 216–226. Бибкод : 1995BpJ....68..216W . дои : 10.1016/S0006-3495(95)80177-3 . ПМЦ 1281679 . ПМИД 7711244 .
- ^ Ло Д.; Наказава М.; Ёсида Ю.; Кай Дж.; Имаи С. (2000). «Эффекты трех разных Ca 2+ Ингибиторы АТФазы помпы на вызванные сокращения аорты кролика и активность Ca 2+ АТФазы насоса в аорте свиньи». Общая фармакология: Сосудистая система . 34 (3): 211–220. doi : 10.1016/S0306-3623(00)00064-1 . PMID 11120383 .
- ^ Боуман Би Джей; Слейман CW (1979). «Влияние ванадата на АТФазу плазматической мембраны Neurospora crassa» . Журнал биологической химии . 254 (8): 2928–2934. дои : 10.1016/S0021-9258(17)30163-1 . ПМИД 155060 .
- ^ Аурелиано, Мануэль; Кранс, Дебби С. (2009). «Декаванадат ( В.
10 О 6−
28 ) и оксованадаты: оксометаллаты со многими биологическими активностями» . Журнал неорганической биохимии . 103 (4): 536–546. doi : 10.1016/j.jinorgbio.2008.11.010 . ISSN 0162-0134 . PMID 19110314 .