Причина обсессивно-компульсивного расстройства
Причину можно обсессивно-компульсивного расстройства понять главным образом путем выявления биологических факторов риска, которые приводят к симптоматике обсессивно-компульсивного расстройства (ОКР). Ведущие гипотезы предполагают участие орбитофронтальной коры , базальных ганглиев и/или лимбической системы ; открытия сделаны в области нейроанатомии, нейрохимии, нейроиммунологии, нейрогенетики и нейроэтологии.
ОКР, вызванное наркотиками
[ редактировать ]Многие различные виды лекарств могут вызвать/индуцировать ОКР у пациентов, у которых никогда раньше не было симптомов. Новая глава об ОКР в DSM-5 (2013) теперь конкретно включает ОКР, вызванное наркотиками. [ нужна ссылка ]
атипичные нейролептики (антипсихотики второго поколения), такие как оланзапин (зипрекса), вызывают у пациентов ОКР de novo. Доказано, что [ 1 ] [ 2 ] [ 3 ] [ 4 ]
Нейроанатомия
[ редактировать ]Хотя по поводу оценки ОКР ведутся серьезные споры, текущие исследования тяготеют к структурной и функциональной нейровизуализации . Эти технологические инновации позволили лучше понять нейроанатомические факторы риска ОКР. Эти исследования можно разделить на четыре основные категории: (1) исследования в состоянии покоя, в которых сравнивается активность мозга в состоянии покоя у пациентов с ОКР с контрольной группой, (2) исследования, провоцирующие симптомы, в которых сравнивается активность мозга до и после возникновения симптомов, (3) исследования в области лечения. которые сравнивают активность мозга до и после лечения фармакотерапией , и (4) исследования когнитивной активации, которые сравнивают активность мозга при выполнении задачи у пациентов с ОКР с контрольной группой. [ 5 ]
Данные, полученные в результате этого исследования, позволяют предположить, что при ОКР задействованы три области мозга: орбитофронтальная кора (ОФК), передняя поясная извилина (АКК) и головка хвостатого ядра . [ 5 ] Несколько исследований показали, что у пациентов с ОКР эти области: (1) гиперактивны в состоянии покоя по сравнению со здоровыми людьми; (2) становятся все более активными при провокации симптомов; и (3) больше не проявляют гиперактивности после успешного лечения фармакотерапией SRI или когнитивной терапией. [ 6 ] Это понимание часто приводится в качестве доказательства того, что аномалии в этих нейроанатомических областях могут вызывать ОКР.
OFC и ACC сложно связаны с базальными ганглиями через кортико-базальные ганглии-таламо-кортикальную петлю . [ 7 ] Современные теории предполагают, что ОКР может быть результатом дисбаланса между «прямыми» и «непрямыми» путями, проходящими через базальные ганглии. Прямые пути описываются как идущие от коры к полосатому телу, затем к внутреннему сегменту бледного шара (GPi) и сетчатой части черной субстанции (SNr), затем к таламусу и, наконец, обратно в кору. Непрямые пути описываются как идущие от коры к полосатому телу, затем к внешнему сегменту бледного шара (GPe), субталамическому ядру (STN), GPi и SNr, затем к таламусу и, наконец, обратно к коре. [ 8 ] В то время как суммарный эффект прямого пути является возбуждающим, суммарный эффект непрямого пути является тормозящим. Таким образом, была выдвинута гипотеза, что чрезмерная относительная активность в прямом пути в петлях OFC/ACC CBGTC может привести к образованию петли положительной обратной связи, в которой навязчивые мысли задерживаются. [ 8 ] Хотя структурные и функциональные нейровизуализационные исследования предоставили прочную основу для этого предположения, до сих пор неясно, почему у пациентов с ОКР развиваются специфические навязчивые идеи, а не генерализованное навязчивое поведение по отношению ко всему. Хотя исследователи предполагают, что существует предвзятость реакции в отношении определенных стимулов, таких как загрязнение, основная причина до сих пор неясна. [ 9 ]
Нейрохимия
[ редактировать ]Несмотря на повсеместное понимание того, что нейрохимические функции ответственны за проявление симптомов ОКР, недавние психофармакологические исследования показали, что система нейротрансмиттеров серотонина (5-НТ) играет особенно важную роль. [ 10 ] по сравнению со здоровыми людьми долгосрочное применение селективных ингибиторов обратного захвата серотонина Было обнаружено, что (СИОЗС) более эффективно, чем ингибиторы норадренергического обратного захвата, при лечении ОКР. [ 10 ] Например, Рапопорт и др. продемонстрировали, что кломипрамин более эффективен, чем дезипрамин, в уменьшении некоторых типов повторяющегося поведения. [ 11 ] Исследования также показали, что прием антагонистов 5-НТ часто усугубляет симптомы ОКР. [ 12 ] Если бы это было правдой, можно было бы ожидать, что миртазапин (который, среди прочего, является антагонистом рецептора 5-НТ 2А ) и атипичные антипсихотики, которые также оказывают антагонистическое действие на этот рецептор, ослабят эффект СИОЗС. Однако клинические исследования этих препаратов показали обратное. миртазапин Было показано, что , хотя и не эффективен сам по себе, ускоряет эффект пароксетина (Pallanti et al., 2004), а несколько исследований показали, что атипичные антипсихотики усиливают эффекты СИОЗС у рефрактерных пациентов с ОКР (Bloch et al., 2006). ). [ 13 ] Хотя эти данные не дают четкой причины, они закладывают основу для представления о том, что психиатрические состояния можно анализировать фармакологически. Таким образом, эффективность контроля обсессий и компульсий с помощью СИОЗС позволяет предположить, что ОКР имеет нейрохимическую этиологию.
Дофаминергические системы вовлечены в ОКР из-за эффективности дофаминергических агентов, того факта, что PANDAS может быть вовлечен, [ 14 ] и различными исследованиями нейровизуализации. [ 15 ] ОКР можно лечить антипсихотическими препаратами, однако психостимуляторы также показали некоторую перспективу в облегчении симптомов ОКР. [ 16 ] Хотя их необходимо согласовать, оба они затрагивают дофаминергические системы. ОКР также часто сочетается с СДВГ. [ 17 ] который лечится психостимуляторами и может быть результатом усиления фазовой и сниженной тонической передачи сигналов дофаминергических нейронов. PANDAS также влияет на базальные ганглии, где дофамин играет большую роль нейромедиатора.
Нейроиммунология
[ редактировать ]Спорная гипотеза PANDAS предполагает, что нейроиммунологический постстрептококковый аутоиммунитет может быть потенциальной экологической причиной возникновения ОКР в детстве. [ 18 ] [ 19 ] [ 20 ] [ 21 ] После стрептококковой инфекции у подгруппы детей внезапно возникло обострение симптомов ОКР. Основная гипотеза PANDAS и более широкой PANS заключается в том, что ОКР может развиваться как следствие аутоиммунной реакции, при которой антитела к стрептококковой инфекции атакуют и повреждают базальные ганглии. [ 19 ]
Навязчивые идеи и компульсии также очень распространены при ряде других заболеваний, включая: синдром Туретта , болезнь Паркинсона , эпилепсию , шизофрению , болезнь Хантингтона , летаргический энцефалит , хорею Сиденгама и поражение определенных областей мозга. [ 22 ] Подобно ОКР, эти расстройства также демонстрируют аномалии в базальных ганглиях. Эта часть мозга отвечает за познание, эмоции и движение. Нарушение работы базальных ганглиев приводит к множеству симптомов, которые характеризуются компульсивностью (паттерны поведения, которые проявляются неоднократно) и импульсивностью (паттерны поведения, которые внезапно проявляются под действием различных раздражителей). [ 5 ] Это позволяет предположить, что у пациентов с ОКР расстройство может быть результатом нарушения функционирования базальных ганглиев.
Нейрогенетика
[ редактировать ]Исследования, предполагающие генетические факторы ОКР
[ редактировать ]Исследования близнецов [ 23 ] Исследования семейных ассоциаций показали, что существуют определенные генетические факторы, лежащие в основе обсессивно-компульсивного расстройства. Большинство исследований семейных ассоциаций показали, что по крайней мере некоторые формы ОКР являются семейными. Уровень ОКР среди родственников пострадавших был значительно выше, чем предполагаемая распространенность ОКР среди населения и уровень среди контрольной группы. Родственники взрослых с ОКР были примерно в два раза чаще подвержены этому заболеванию, чем контрольная группа, в то время как родственники детей и подростков с ОКР примерно в десять раз чаще страдали ОКР. Однако эта семейная ассоциация также могла быть вызвана культурными факторами или факторами окружающей среды. [ 24 ] В настоящее время проведено очень мало исследований, изучающих факторы окружающей среды, вызывающие ОКР. Однако в ретроспективном исследовании факторов риска окружающей среды исследователи обнаружили, что продолжительные роды и отеки во время беременности коррелируют с обсессивно-компульсивным расстройством. [ 25 ] предполагая, что окружающая среда играет некоторую роль в определении его проявления.
В результате были проведены исследования близнецов, чтобы показать, что симптомы ОКР передаются по наследству и, следовательно, генетически связаны. [ 23 ] Монозиготные, или однояйцевые, близнецы разделяют 100% своих генов, тогда как дизиготные, или разнояйцевые, близнецы разделяют в среднем 50% своих генов. Классическое исследование близнецов сравнивает монозиготных и дизиготных близнецов. Если монозиготные близнецы гораздо больше похожи друг на друга, чем дизиготные близнецы, то вполне вероятно, что генетика играет важную роль в развитии интересующего признака. Эти исследования показали, что генетическое влияние на симптомы обсессивно-компульсивного расстройства у детей составляет от 45 до 65%. Влияние было меньше у взрослых и составляло от 27 до 47%. [ 23 ] Однако результаты исследований осложняются тем, что присутствие в выборке лиц с ОКР зачастую было низким. В результате исследователи часто включали в исследование людей с обсессивно-компульсивными симптомами или субклиническим ОКР. [ 24 ] Таким образом, они, возможно, включили в исследование пациентов с другими, схожими расстройствами. Ранние исследования близнецов были позже повторены с использованием близнецов с ОКР, соответствующих критериям DSM, и выявлением пробандов , но были проведены лишь некоторые из них. [ 23 ]
ОКР с ранним началом
[ редактировать ]ОКР с ранним началом, манифестирующее в детстве или подростковом возрасте, представляет собой подтип ОКР, этиологически отличный от ОКР с началом во взрослом возрасте. Сообщается, что это ОКР с ранним началом генетически связано с тиками и синдромом Туретта , поскольку одно исследование показало, что пациенты с ОКР с ранним началом имеют более высокий уровень развития синдрома Туретта и других тиковых расстройств. [ 25 ] Исследования семейных ассоциаций [ 26 ] предположили, что раннее начало ОКР коррелирует с повышенным семейным и, возможно, генетическим риском. Частота ОКР и субклинического ОКР среди родственников пробандов, у которых ОКР манифестировала в детстве или подростковом возрасте, была как минимум в два раза выше, чем среди родственников пробандов, у которых ОКР манифестировало во взрослом возрасте. [ 26 ] Другие исследования также показали, что существует обратная зависимость между возрастом пробанда и риском ОКР у родственников. [ 27 ] Следовательно, возможно, что за двумя типами ОКР стоят разные генетические механизмы; поэтому при исследовании генов-кандидатов может возникнуть необходимость контролировать возраст начала заболевания.
Ген-кандидат SLC1A1
[ редактировать ]Вполне вероятно, что ряд генов важен для развития ОКР. Некоторые из этих генов-кандидатов были идентифицированы, но ни одно из исследований генов-кандидатов не было последовательно воспроизведено, за исключением тех, которые относятся к гену переносчика глутамата, SLC1A1 (семейство растворенных переносчиков 1, член 1), который кодирует переносчик глутамата , EAAC1. [ 24 ] Было высказано предположение, что трудности с идентификацией генов-кандидатов могут быть связаны с тем фактом, что большинство исследований генов игнорировали факторы окружающей среды.[9] Следовательно, для дальнейших генетических исследований может потребоваться разработка моделей взаимодействия генетических факторов и факторов окружающей среды для определенных подтипов ОКР. Также были завершены три полногеномных исследования ассоциации ОКР, которые выявили потенциальные области интереса, включая область, содержащую SLC1A1, 9p24. [ 24 ] SLC1A1 экспрессируется в коре головного мозга, полосатом теле и таламусе (кортико-стриато-таламокортикальный контур) и связан с нейротрансмиссией глутамата. [ 28 ] Нейровизуализация, исследования генов-кандидатов и исследования на животных моделях предоставили доказательства связи SLC1A1 и передачи сигналов глутамата с возникновением ОКР. Нейровизуализационные исследования показали, что концентрации глутаматергической глутамата в хвостатой части поясной извилины ниже и выше в хвостатой зоне у пациентов с ОКР с ранним началом по сравнению с контрольной группой, что позволяет предположить, что транспорт глутамата (и, в свою очередь, ген-переносчик глутамата SLC1A1) связан с возникновением ОКР. . [ 29 ]
Однонуклеотидные полиморфизмы (SNP) в гене SLC1A1 неизменно связаны с ОКР. Помимо транспорта глутамата, EAAC1, транспортер, кодируемый SLC1A1, также связан с синтезом ГАМК, что может способствовать предрасположенности к ОКР. Первоначальное исследование продемонстрировало значительную связь между ОКР и 3-сцепленными полиморфизмами в гене SLC1A1. [ 30 ] Этот результат был повторен в многочисленных исследованиях. В одном исследовании проверялось наличие четырех SNP в гене SLC1A1 у людей с ранним началом ОКР в ханьской популяции. [ 31 ] и обнаружили, что один SNP, rs10491734, встречался значительно чаще у пациентов с ОКР, чем в контрольной группе. Однако точные SNP, выявленные в разных исследованиях, различаются, хотя возможно, что это связано с тем, что исследования проводились на разных этнических группах. [ 31 ] Например, семейное исследование ассоциаций проанализировало случаи SNP внутри и вокруг SLC1A1 в семьях по всей территории США и обнаружило, что другой SNP, rs4740788, и 3-SNP гаплотип, rs4740788-rs10491734-rs10491733, оба были связаны с ОКР. [ 32 ]
Для изучения обсессивно-компульсивного расстройства было разработано несколько моделей на мышах. Модельные организмы полезны для того, чтобы позволить исследовать аспекты некоторых психических расстройств у одного вида (в данном случае у людей) на других видах (в данном случае на мышах). Примечательно, что мыши с нулевым SLC1A1 демонстрировали компульсивное поведение, проявляя повышенную агрессию и чрезмерный уход за собой, что приводило к выпадению шерсти. Однако, поскольку это были только два вида поведения, слабо связанные с ОКР, это не предоставило убедительных доказательств связи между потерей EAAC1 и поведением, подобным ОКР. Учитывая сильную корреляцию между геном SLC1A1 и ОКР, это позволяет предположить, что отсутствие EAAC1 приводит к поведению, подобному ОКР, только тогда, когда оно сочетается с другими редкими мутациями в генах, связанных с CSTC или кортико-стриато-таламокортикальным контуром. [ 33 ]
Нейроэтология
[ редактировать ]Огромный монолит психиатрических исследований сделал акцент на непосредственных механизмах как причине болезней. Напротив, эволюционная теория породила вопросы относительно того, как дистальные механизмы могут быть вовлечены в патогенез. ОКР включает в себя несколько поведенческих схем, которые, возможно, сохранились на протяжении всей истории эволюции. Многие виды унаследовали когнитивные модели, позволяющие отслеживать опасность, избегать заражения и копить еду. [ 34 ] Теоретики выдвинули гипотезу, что дисфункция любой из этих стратегий может привести к выражению ОКР. Эта гипотеза дополнительно подтверждается доказательствами того, что такие унаследованные, видоспецифичные стратегии хранятся в базальных ганглиях. [ 5 ]
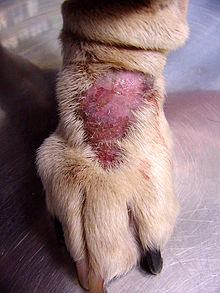
Рассматривая проявление ОКР у видов, отличных от человека, исследователи изучили акральный дерматит облизывания (также известный как облизывающая гранулема ) у крупных собак. Это заболевание характеризуется чрезмерным облизыванием или расчесыванием, что приводит к алопеции (выпадению волос) и последующим гранулематозным поражениям (сосудистой ткани на поверхности раны). [ 11 ] Рапопорт и др. обнаружили, что это обсессивно-компульсивное поведение облегчалось у собак после введения кломипрамина. [ 11 ] Таким образом, вполне возможно, что эволюционно выбранные черты могут стать дезадаптивной продолжающейся неврологической дисфункцией.
Ссылки
[ редактировать ]- ^ Алевизос, Василий; Папагеоргиу, Хараламбос; Христодулу, Джордж Н. (1 сентября 2004 г.). «Обсессивно-компульсивные симптомы при применении оланзапина» . Международный журнал нейропсихофармакологии . 7 (3): 375–377. дои : 10.1017/S1461145704004456 . ISSN 1461-1457 . ПМИД 15231024 .
- ^ Кулкарни, Гаджанан; Нараянасвами, Джанарданан К.; Математика, Суреш Бада (1 января 2012 г.). «Оланзапин индуцировал обсессивно-компульсивное расстройство de novo у пациента с шизофренией» . Индийский журнал фармакологии . 44 (5): 649–650. дои : 10.4103/0253-7613.100406 . ISSN 0253-7613 . ПМЦ 3480803 . ПМИД 23112432 .
- ^ Ликурас, Л.; Зервас, И.М.; Гурнеллис, Р.; Маллиори, М.; Рабавилас, А. (1 сентября 2000 г.). «Оланзапин и обсессивно-компульсивные симптомы». Европейская нейропсихофармакология . 10 (5): 385–387. дои : 10.1016/s0924-977x(00)00096-1 . ISSN 0924-977X . ПМИД 10974610 . S2CID 276209 .
- ^ Ширмбек, Фредерика; Цинк, Матиас (1 марта 2012 г.). «Обсессивно-компульсивные симптомы, вызванные клозапином, при шизофрении: критический обзор» . Современная нейрофармакология . 10 (1): 88–95. дои : 10.2174/157015912799362724 . ISSN 1570-159X . ПМК 3286851 . ПМИД 22942882 .
- ^ Jump up to: а б с д Майя, ТВ, Куни, Р.Э. и Петерсон, Б.С. (2008). Нейронные основы обсессивно-компульсивного расстройства у детей и взрослых. Развитие и психопатология, 1251–1283.
- ^ Уайтсайд, СП; Порт, Джей Ди; Абрамовиц, Дж. С. (2004). «Метаанализ функциональной нейровизуализации при обсессивно-компульсивном расстройстве». Психиатрические исследования . 132 (1): 69–79. doi : 10.1016/j.pscychresns.2004.07.001 . ПМИД 15546704 . S2CID 9941792 .
- ^ Александр, генеральный директор; Делонг, MR; Стрик, PL (1986). «Параллельная организация функционально разделенных цепей, связывающих базальные ганглии и кору». Ежегодный обзор неврологии . 9 : 357–381. дои : 10.1146/annurev.neuro.9.1.357 . ПМИД 3085570 .
- ^ Jump up to: а б Саксена, С.; Раух, С.Л. (2000). «Функциональная нейровизуализация и нейроанатомия обсессивно-компульсивного расстройства». Психиатрические клиники Северной Америки . 23 (3): 563–586. дои : 10.1016/s0193-953x(05)70181-7 . ПМИД 10986728 .
- ^ Сассон, Ю.; Зохар, Дж.; Чопра, М.; Люстиг, М.; Янку, И.; Хендлер, Т. (1997). «Эпидемиология обсессивно-компульсивного расстройства». Семинары по клинической нейропсихиатрии . 6 : 82–101.
- ^ Jump up to: а б Зохар, Дж (1987). «Обсессивно-компульсивное расстройство: психобиологические подходы к диагностике, лечению и патофизиологии». Биологическая психиатрия . 22 (6): 667–687. дои : 10.1016/0006-3223(87)90199-5 . ПМИД 3036259 . S2CID 24410666 .
- ^ Jump up to: а б с Рапопорт, Дж.Л.; Райланд, Д.Х.; Криете, М. (1992). «Медикаментозное лечение акрального облизывания собак: модель обсессивно-компульсивного расстройства на животных». Архив общей психиатрии . 49 (7): 517–521. дои : 10.1001/archpsyc.1992.01820070011002 . ПМИД 1385694 .
- ^ Холландер, Э.; Либовиц, MR; ДеКариа, CM (1994). «Серотонинергическая чувствительность при пограничном расстройстве личности: предварительные результаты». Американский журнал психиатрии . 151 (2): 277–280. дои : 10.1176/ajp.151.2.277 . ПМИД 8296905 .
- ^ ван Дейк, Эдди; Кломпмейкерс, Андре; Денис, Дамиан (2010). «Серотонинергическая система при обсессивно-компульсивном расстройстве». Справочник по поведенческой нейробиологии серотонина . Справочник по поведенческой нейронауке. Том. 21. С. 547–563. дои : 10.1016/s1569-7339(10)70100-4 . ISBN 9780123746344 .
- ^ Орефичи, Грациелла; Кардона, Франческо; Кокс, Кэрол; Каннингем, Мадлен. Детские аутоиммунные нервно-психические расстройства, связанные со стрептококковыми инфекциями (PANDAS) . Оклахома-Сити: Центр медицинских наук Университета Оклахомы.
- ^ Майя, Тьяго; Куни, Ребекка; Петерсон, Брэдли (2008). «Нейронные основы обсессивно-компульсивного расстройства у детей и взрослых» . Дев Психопатология . 20 (4): 1251–1283. дои : 10.1017/S0954579408000606 . ПМК 3079445 . ПМИД 18838041 .
- ^ Коран, Лоррин; Абуджауд, Элиас; Гамель, Нона (2009). «Двойное слепое исследование декстроамфетамина по сравнению с добавлением кофеина для лечения резистентного обсессивно-компульсивного расстройства». Журнал клинической психиатрии . 70 (11): 1530–1535. дои : 10.4088/JCP.08m04605 . ПМИД 19573497 .
- ^ Дар, Реувен; Миттельман, Эндрю; Вильгельм, Сабина (2015). «Коморбидность между синдромом дефицита внимания/гиперактивности и обсессивно-компульсивным расстройством на протяжении всей жизни». Гарвардский обзор психиатрии : 245–262.
- ^ Уилбур С., Битнун А., Кроненберг С., Лаксер Р.М., Леви Д.М., Логан В.Дж., Шоулдис М., Йе Е.А. (май 2019 г.). «ПАНДЫ/ПАНСЫ в детстве: Споры и доказательства» . Педиатр по здоровью детей . 24 (2): 85–91. дои : 10.1093/pch/pxy145 . ПМК 6462125 . ПМИД 30996598 .
- ^ Jump up to: а б Сигра С, Хессельмарк Е, Бежеро С (март 2018 г.). «Лечение PANDAS и PANS: систематический обзор» . Neurosci Biobehav Rev. 86 : 51–65. doi : 10.1016/j.neubiorev.2018.01.001 . ПМИД 29309797 . S2CID 40827012 .
- ^ Мараццити Д., Муччи Ф., Фонтенель Л.Ф. (июль 2018 г.). «Иммунная система и обсессивно-компульсивное расстройство». Психонейроэндокринология (обзор). 93 : 39–44. doi : 10.1016/j.psyneuen.2018.04.013 . ПМИД 29689421 . S2CID 13681480 .
- ^ Зиборди Ф., Зорзи Г., Кареккио М., Нардоччи Н. (март 2018 г.). «CANS: острые нервно-психические синдромы у детей». Eur J Paediatr Neurol (обзор). 22 (2): 316–320. дои : 10.1016/j.ejpn.2018.01.011 . ПМИД 29398245 .
- ^ Нештадт, Г., Градос, М., и Сэмюэлс, Дж. Ф. (2010). Генетика обсессивно-компульсивного расстройства. Психиатрические клиники Северной Америки, 141–158.
- ^ Jump up to: а б с д ван Гротист, Дэниел С.; Кэт, Даниэль С.; Бикман, Аартжан Т.; Бумсма, Доррет И. (2005). «Близнецовые исследования обсессивно-компульсивного расстройства: обзор» . Исследования близнецов и генетика человека . 8 (5): 450–458. дои : 10.1375/твин.8.5.450 . hdl : 1871/17957 .
- ^ Jump up to: а б с д Паулс, Дэвид Л. (2010). «Генетика обсессивно-компульсивного расстройства: обзор» . Диалоги в клинической неврологии . 12 (2): 149–163. дои : 10.31887/DCNS.2010.12.2/dpauls . ПМК 3181951 . ПМИД 20623920 .
- ^ Jump up to: а б Салем Васконселос, Маркос; Сантос Сампайо, Алин; и др. (2007). «Пренатальные, перинатальные и послеродовые факторы риска обсессивно-компульсивного расстройства». Биологическая психиатрия . 61 (3): 301–307. doi : 10.1016/j.biopsych.2006.07.014 . ПМИД 17123475 . S2CID 41596757 .
- ^ Jump up to: а б Эйхштедт, Джули А.; Арнольд, Шэрон Л. (2001). «Обсессивно-компульсивное расстройство, возникшее в детстве: подтип ОКР, связанный с тиками?». Обзор клинической психологии . 21 (1): 137–158. дои : 10.1016/s0272-7358(99)00044-6 . ПМИД 11148894 .
- ^ Нештадт, Джеральд; Градос, Марко; Сэмюэлс, Дж. Ф. (2010). «Генетика ОКР» . Психиатрические клиники Северной Америки . 33 (1): 141–158. дои : 10.1016/j.psc.2009.11.001 . ПМЦ 2824902 . ПМИД 20159344 .
- ^ Йошикацу Канаи и Маттиас А. Хедигер, «Семейство транспортеров глутамата/нейтральных аминокислот SLC1: молекулярные, физиологические и фармакологические аспекты», Архив Pflügers: Европейский журнал физиологии 447, вып. 5 (2003): 467-479.
- ^ Розенберг, Дэвид Р.; Макмастер, Фрэнк П.; Кешаван, Матчери С.; и др. (2000). «Снижение концентрации хвостатого глутаматергического вещества у детей с обсессивно-компульсивным расстройством, принимающих пароксетин». Журнал Американской академии детской и подростковой психиатрии . 39 (9): 1096–1103. дои : 10.1097/00004583-200009000-00008 . ПМИД 10986805 .
- ^ Дэниел Арнольд, Пол; Сикард, Триша; Берроуз, Элиза; Рихтер, Маргарет А.; Кеннеди, Джеймс Л. (2006). «Ген-переносчик глутамата SLC1A1, связанный с обсессивно-компульсивным расстройством» . Архив общей психиатрии . 63 (7): 769–776. дои : 10.1001/archpsyc.63.7.769 . ПМИД 16818866 .
- ^ Jump up to: а б Ву, Хайсу; Ван, Сюэмэй; Сяо, Зепин; и др. (2013). «Связь между геном SLC1A1 и ранним началом ОКР у населения ханьцев: исследование случай-контроль». Журнал молекулярной нейронауки . 50 (2): 353–359. дои : 10.1007/s12031-013-9995-6 . ПМИД 23564280 . S2CID 14316918 .
- ^ Сэмюэлс, Джек; Ван, Ин; Риддл, Марк А.; и др. (2011). «Комплексное семейное исследование гена-переносчика глутамата SLC1A1 при обсессивно-компульсивном расстройстве» . Американский журнал медицинской генетики. Часть B: Нейропсихиатрическая генетика . 156 (4): 472–477. дои : 10.1002/ajmg.b.31184 . ПМК 3082623 . ПМИД 21445956 .
- ^ Тинг, Джонатан Т.; Фэн, Гопин (2011). «Нейробиология обсессивно-компульсивного расстройства: понимание дисфункции нейронных цепей с помощью генетики мышей» . Современное мнение в нейробиологии . 21 (6): 842–848. дои : 10.1016/j.conb.2011.04.010 . hdl : 1721.1/102180 . ПМК 3192923 . ПМИД 21605970 .
- ^ О'Коннор, Джей-Джей (2008). Дефект ткани. Журнал современной психотерапии, 87-96.