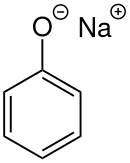
Феноксид натрия
| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Феноксид натрия [ 1 ] | |
| Другие имена
Фенолят натрия
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.004.862 |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 6 Н 5 НаО | |
| Молярная масса | 116.09 g/mol |
| Появление | Белый твердый |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
Вредный, Коррозионный |
| точка возгорания | Невоспламеняющийся |
| Невоспламеняющийся | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Феноксид натрия ( фенолят натрия ) — органическое соединение с формулой NaOC 6 H 5 . Это белое кристаллическое твердое вещество. также известный как фенолят, представляет собой сопряженное основание фенола Его анион, феноксид , . Он используется в качестве предшественника многих других органических соединений, таких как ариловые эфиры .
Синтез и структура
[ редактировать ]Чаще всего растворы феноксида натрия получают обработкой фенола гидроксидом натрия. [ 2 ] Безводные производные можно получить путем объединения фенола и натрия. В соответствующей обновленной процедуре вместо гидроксида натрия используется метоксид натрия: [ 3 ]
- NaOCH 3 + HOC 6 H 5 → NaOC 6 H 5 + HOCH 3
Феноксид натрия также можно получить путем «щелочного плавления» бензолсульфоновой кислоты , при котором сульфонатные группы замещаются гидроксидом:
- C 6 H 5 SO 3 Na + 2 NaOH → C 6 H 5 OH + Na 2 SO 3
Когда-то этот путь был основным промышленным путем получения фенола. [ нужна ссылка ]
Структура
[ редактировать ]Как и другие алкоксиды натрия , твердый феноксид натрия имеет сложную структуру, включающую множество связей Na-O. Материал, не содержащий растворителей, является полимерным, каждый центр Na связан с тремя кислородными лигандами, а также с фенильным кольцом . Аддукты феноксида натрия являются молекулярными, например кластер кубанового типа [NaOPh] 4 ( HMPA ) 4 . [ 4 ]
Реакции
[ редактировать ]Феноксид натрия – умеренно сильное основание. Подкисление дает фенол: [ 5 ]
- PhOH ⇌ PhO − + Ч + (К = 10 −10 )
Кислотно-основное поведение осложняется гомоассоциацией , отражающей ассоциацию фенола и феноксида. [ 6 ]
Феноксид натрия реагирует с алкилирующими агентами с образованием алкилфениловых эфиров: [ 2 ]
- NaOC 6 H 5 + RBr → ROC 6 H 5 + NaBr
Преобразование является продолжением синтеза эфира Вильямсона . С помощью ацилирующих агентов получают фениловые эфиры: [ нужна ссылка ]
- NaOC 6 H 5 + RC(O)Cl → RCO 2 C 6 H 5 + NaCl
Феноксид натрия подвержен определенным типам электрофильных ароматических замещений . Например, он реагирует с диоксидом углерода с образованием 2-гидроксибензоата, сопряженного основания салициловой кислоты . Однако в целом электрофилы необратимо атакуют кислородный центр феноксида. [ нужна ссылка ]
Ссылки
[ редактировать ]- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 . Королевское химическое общество . стр. 1071, 1129. doi : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ^ Jump up to: а б КС Марвел; А. Л. Таненбаум (1929). «γ-феноксипропилбромид». Орг. Синтез . 9:72 . дои : 10.15227/orgsyn.009.0072 .
- ^ Корнблюм, Натан; Лурье, Арнольд П. (1959). «Гетерогенность как фактор алкилирования амбидентных анионов: феноксид-ионы1,2». Журнал Американского химического общества . 81 (11): 2705–2715. дои : 10.1021/ja01520a030 .
- ^ Майкл Кунерт, Экхард Диньюс, Мария Наук, Иоахим Зилер «Структура и реакционная способность феноксида натрия - по ходу реакции Кольбе-Шмитта» Chemical Reports, 1997, том 130, выпуск 10, страницы 1461–1465. два : 10.1002/cber.19971301017
- ^ Смит, Майкл Б.; Марч, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ К. Изуцу (1990). Константы кислотно-основной диссоциации в диполярных апротонных растворителях . Том. 35. Научные публикации Блэквелла.
Внешние ссылки
[ редактировать ]![]() СМИ, связанные с феноксидом натрия, на Викискладе?
СМИ, связанные с феноксидом натрия, на Викискладе?


