Реакция Кенигса-Кнорра
Кенигса -Кнорра в органической химии представляет собой замещения гликозилгалогенида реакцию Реакция спиртом образованием с гликозида . Это одна из старейших реакций гликозилирования. Он назван в честь Вильгельма Кенигса (1851–1906), ученика фон Байера и однокурсника Германа Эмиля Фишера , и Эдварда Кнорра, ученика Кенигса.

В исходном виде Кенигс и Кнорр обрабатывали ацетобромглюкозу спиртами в присутствии карбоната серебра . [1] Вскоре после этого Фишер и Армстронг сообщили об очень похожих результатах. [2]
В приведенном выше примере стереохимический результат определяется наличием соседней группы у C2, которая оказывает анхимерную помощь , что приводит к образованию 1,2-транс-стереохимической структуры. Сложные эфиры (например, ацетил , бензоил , пивалил ) обычно обеспечивают хорошую анхимерную поддержку, тогда как простые эфиры (например, бензил , метил и т. д.) этого не делают, что приводит к смесям стереоизомеров .
Механизм
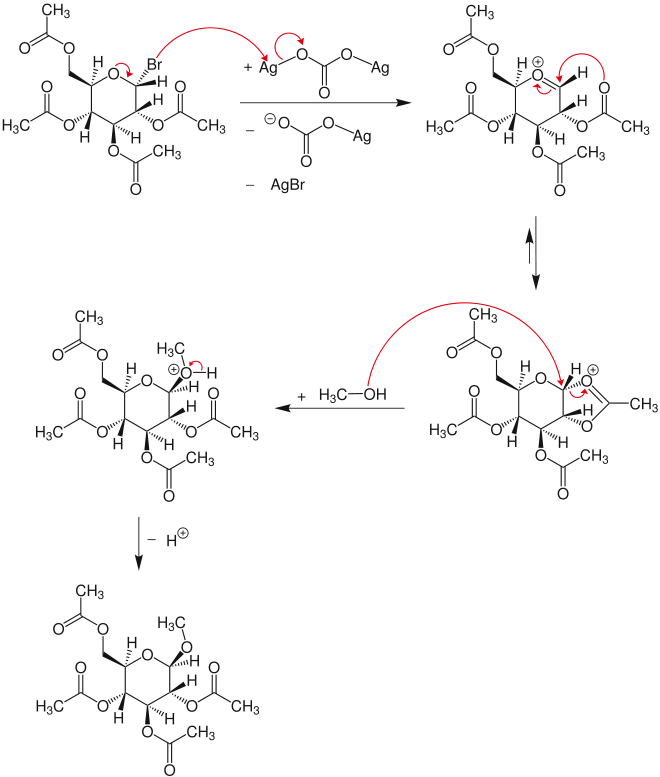
[ редактировать ]На первой стадии механизма гликозилбромид реагирует с карбонатом серебра при отщеплении бромида серебра и аниона карбоната серебра до иона оксокарбения. Из этой структуры образуется диоксоланиевое кольцо, которое подвергается атаке метанола через SN.
2 механизм при карбонильном атоме углерода. Эта атака приводит к инверсии. После депротонирования промежуточного оксония образуется продукт гликозид. [3]
Реакцию также можно применять к углеводам с другими защитными группами. При синтезе олигосахаридов вместо метанола используются другие углеводы, модифицированные защитными группами таким образом, что доступна только одна гидроксильная группа.
История
[ редактировать ]Позже Эмиль Фишер и Буркхардт Хелферих перенесли этот метод на другие хлорзамещенные пурины и таким образом впервые получили синтетические нуклеозиды. Позже он был улучшен и модифицирован многочисленными химиками.
Альтернативные реакции
[ редактировать ]Как правило, реакция Кенигса-Кнорра относится к использованию гликозилхлоридов, бромидов и, в последнее время, йодидов в качестве доноров гликозила. Реакцию Кенигса-Кнорра можно проводить с альтернативными промоторами, такими как различные соли тяжелых металлов, включая бромид ртути / оксид ртути , цианид ртути и трифлат серебра . [4] [5] Когда используются соли ртути, реакцию обычно называют методом Хелфериха . Другими методами гликозидирования являются гликозилирование по Фишеру , использование гликозилацетатов , тиогликозидов , гликозилтрихлорацетимидатов , гликозилфторидов или н-пентенилгликозидов в качестве гликозильных доноров или внутримолекулярная доставка агликонов .
Ссылки
[ редактировать ]- ^ Кенигс, Вильгельм; Норр, Эдвард (1901). «О некоторых производных глюкозы и галактозы (р)» . Отчеты Немецкого химического общества . 34 (1): 957–981. дои : 10.1002/cber.190103401162 .
- ^ Фишер, HE ; Армстронг, EF (1901). «Об изомерных ацетогалогенпроизводных глюкозы и синтезе глюкозидов» . Отчеты Немецкого химического общества . 34 (2): 2885–2900. дои : 10.1002/cber.190103402251 .
- ^ Курти, Ласло; Чако, Барбара (2005). Стратегическое применение названных реакций в органическом синтезе: предпосылки и подробные механизмы . Эльзевир. п. 246–7. ISBN 978-0-12-429785-2 .
- ^ Хелферих, Б.; Зирнер, Дж. (1962). «О синтезе тетраацетилгексоз со свободным 2-гидроксилом. Синтез некоторых дисахаридов». хим. Бер. 95 (11): 2604. doi : 10.1002/cber.19620951103 .
- ^ Ханессян, С.; Бануб, Дж. (2012) [1980]. «35. Получение 1,2-транс-гликозидов в присутствии трифторметансульфоната серебра» . Общие методы . Методы химии углеводов. Том. 8. Эльзевир. стр. 247–250. ISBN 9780323153645 .