ЙОЙО-1
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
[1 2 (2) Z ,16(17 2 ) Z ]-1 3 ,7,7,11,11,17 3 -Гексаметил-1 3 Н , 17 3 Н -7,11-диаза-3 1 л 5 ,15 1 л 5 -3(4,1),15(1,4)-дихинолин-1,17(2)-бис([1,3]бензоксазола)гептадекафан-1 2 (2),16(17 2 )-диен-7,11-диий-3 1 ,15 1 -бис(илий)тетраиодид | |
| Другие имена
ЙОЙО, ЙОЙО-1, ЙОЙО-1
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХимическийПаук | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 49 Н 58 И 4 Н 6 О 2 | |
| Молярная масса | 1270.642 g/mol |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
YOYO-1 — зеленый флуоресцентный краситель , используемый для ДНК окрашивания . [ 1 ] Он принадлежит к семейству монометинцианиновых красителей и представляет собой тетракатионный гомодимер оксазолового желтого (сокращенно YO, отсюда и название YOYO), обычно доступный в виде тетраиодидной соли. В водном буфере свободный краситель YOYO-1 (поглощение: λ макс. 458 нм, испускание: λ макс. 564 нм) имеет очень низкий квантовый выход флуоресценции . Однако интенсивность флуоресценции увеличивается в 3200 раз при связывании посредством бис-интеркаляции с двухцепочечной ДНК (поглощение: λ макс. 489 нм, испускание: λ макс. 509 нм). [ 2 ]
Синтез
[ редактировать ]YOYO-1 получают алкилированием N , N , N ', N' -тетраметил-1,3-пропандиамина 2 эквивалентами N- (3-йодопропилового) аналога оксазолового желтого , [ 2 ] который доступен в три стадии из 2-меркаптобензоксазола: [ 3 ]
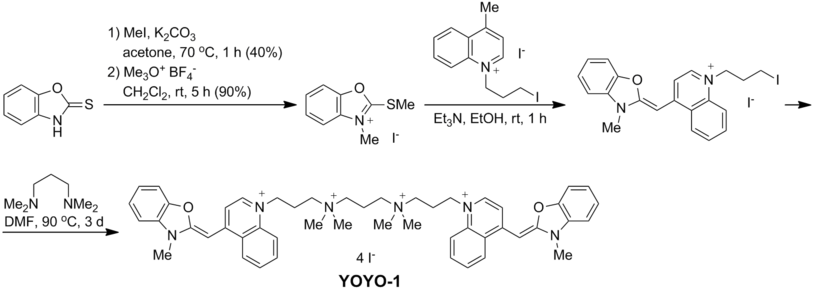
Фотофизика
[ редактировать ]Молярный коэффициент затухания на пике поглощения YOYO-1 составляет около 10. 5 см −1 М −1 , среди высоких значений типичных органических красителей. Квантовый выход флуоресценции YOYO-1 в воде очень мал (<0,1%) и, следовательно, нефлуоресцентен. При связывании с ДНК его квантовый выход увеличивается более чем в 1000 раз и достигает 50%, среди самых ярких флуоресцентных органических красителей.
При световом возбуждении у YOYO-1 в ДНК наблюдаются фотомигание и фотообесцвечивание. Последнее также считается причиной фоторасщепления молекул ДНК хозяина за счет образования реактивных свободных радикалов.
В литературе были предложены два основных механизма, объясняющих, почему YOYO-1 не флуоресцирует в полярных растворителях, но флуоресцирует при интеркалировании в пары оснований ДНК. Первый из них — внутримолекулярный перенос заряда, второй — межмолекулярный перенос заряда. Оба все еще активно изучаются, какой из них доминирует.
Механизм внутримолекулярного переноса заряда был установлен примерно в 1980-х годах. При освещении светом в воде возбужденный электрон в молекуле смещает свою вероятность поперек метиновой группы, что позволяет молекуле вращаться вместе с метиновой группой - реакция фотоизомеризации . Это вращение ослабляет энергию безызлучательно, поэтому молекула не флуоресцирует. Однако когда YOYO-1 внедряется в пары оснований ДНК, он застревает и не может вращаться. Таким образом, молекула остается флуоресцентной. Основным доказательством является то, что при увеличении вязкости раствора путем охлаждения и увеличении содержания глюкозы в смешанном растворе квантовый выход YOYO-1 увеличивается.
Механизм межмолекулярного переноса заряда был предложен в 2018 году. [ 4 ] YOYO-1 слабо связан с молекулами полярного растворителя. При его возбуждении светом в молекуле создается пара электрон-дырка. Дырка способна получить дополнительный электрон от растворителя, который создал отрицательно заряженный радикал YOYO-1 и положительно заряженный радикал в растворе. В большинстве случаев радикалы нейтрализуют друг друга очень быстро и безызлучательно. Это процесс переноса электронов Декстера , который тушит флуоресценцию и создает вращение молекулы YOYO-1. По существу, вращение является продуктом тушения, а не причиной тушения, предполагаемой в механизме внутримолекулярного переноса заряда. Существует небольшая вероятность того, что радикалы разделятся друг с другом и диффундируют, что делает молекулу YOYO-1 восприимчивой к фотообесцвечиванию. Когда молекулы YOYO-1 интеркалируются в молекулу ДНК, гидрофобные пары оснований значительно уменьшают образование радикалов, поскольку ДНК является плохим электрическим проводником. Таким образом, тушение флуоресценции растворителем значительно снижается. Небольшое количество утекающих зарядов создает долгоживущие радикалы и разрезает остов ДНК, что приводит к фоторасщеплению ДНК. Этот механизм подтверждается данными фемтосекундной спектроскопии сверхбыстрого переходного поглощения.
Если механизм внутримолекулярного переноса заряда доминирует в тушении флуоресценции YOYO-1 в воде, то можно добавить объемистый лиганд, чтобы остановить или замедлить вращение, чтобы увеличить его квантовый выход в воде. Однако, если доминирует межмолекулярный перенос заряда, можно модифицировать молекулу, чтобы остановить перенос заряда между YOYO-1 и водой, либо путем пассивации заряда, либо путем модификации лиганда для смещения ее окислительно-восстановительного потенциала.
Приложения
[ редактировать ]Основным применением YOYO-1 является окрашивание ДНК. При нормальных условиях и уровне pH четыре положительных заряда каждой молекулы YOYO-1 позволяют очень легко связываться с молекулами ДНК, имеющими отрицательно заряженные основные цепи. Затем краситель легко интеркалируется в ДНК либо с одного конца, либо с двух концов, в зависимости от температуры отжига и доступного помещения. Затем ДНК загорается под флуоресцентным микроскопом на очень небольшом фоне несвязанного YOYO-1. Измерение может проводиться на уровне объемного ансамбля или на уровне отдельной молекулы. Последний позволил достичь сверхвысокого разрешения с помощью микроскопии сверхвысокого разрешения . [ 5 ] Известно, что при высокой мощности освещения краситель генерирует свободные радикалы, которые затем фоторасщепляют нити ДНК.
Ссылки
[ редактировать ]- ^ Беннинк, ML; Шерер, О.Д.; Канаар, Р; Саката-Согава, К; и др. (июнь 1999 г.). «Одномолекулярные манипуляции с двухцепочечной ДНК с помощью оптического пинцета: исследования взаимодействия ДНК с RecA и YOYO-1» . Цитометрия Часть А. 36 (3): 200–208. doi : 10.1002/(SICI)1097-0320(19990701)36:3<200::AID-CYTO9>3.0.CO;2-T . ПМИД 10404969 .
- ^ Перейти обратно: а б Рожь, ХС; Юэ, С; Веммер, Делавэр; Кесада, Массачусетс; и др. (1992). «Стабильные флуоресцентные комплексы двухцепочечной ДНК с бис-интеркалирующими асимметричными цианиновыми красителями: свойства и применение» . Исследования нуклеиновых кислот . 20 (11): 2803–2812. дои : 10.1093/нар/20.11.2803 . ПМК 336925 . ПМИД 1614866 .
- ^ WO 2010141833 , Ли Джозефсон; Элизабет Гарангер и Скотт Хильдербранд и др., «Важно важные конъюгаты флуорохромов и методы их использования», опубликовано 9 декабря 2010 г., передано The General Hospital Corp.
- ^ Ван, Л; Пайл, младший; Чимату, Калифорния; Чен, Дж. (1 декабря 2018 г.). «Сверхбыстрые переходные спектры поглощения фотовозбужденных молекул YOYO-1 требуют дополнительных исследований механизма тушения их флуоресценции» . Журнал фотохимии и фотобиологии A: Химия . 367 : 411–419. doi : 10.1016/j.jphotochem.2018.09.012 . ПМК 6217845 . ПМИД 30410276 .
- ^ Пайл, Джозеф Р.; Чен, Цзисинь (2 ноября 2017 г.). «Фотообесцвечивание YOYO-1 при флуоресцентной визуализации одиночной ДНК со сверхвысоким разрешением» . Журнал нанотехнологий Бейльштейна . 8 : 2296–2306. дои : 10.3762/bjnano.8.229 . ПМК 5687005 . ПМИД 29181286 .