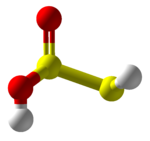
Тиолифурная кислота

| |||
| |||
| Имена | |||
|---|---|---|---|
| Имена IUPAC | |||
| Систематическое имя IUPAC
Гидроксидуксидосульфанидосульфур [ 1 ] | |||
| Другие имена
серная кислота
Тиотионил -гидроксид (незначительный таутомер) | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| Чеби | |||
| Chemspider | |||
| 184467 | |||
PubChem CID
|
|||
Comptox Dashboard ( EPA )
|
|||
| Характеристики | |||
| H 2 S 2 O 2 | |||
| Молярная масса | 98.14668 | ||
| Сопряженная база | Тиосульфит | ||
| Связанные соединения | |||
Связанные соединения
|
Тиозольфурическая кислота SSO тиосульфиновая кислота | ||
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |||
Тиолифурная кислота является гипотетическим химическим соединением с формулой hs -s (= o) -Oh или ho -s (= s) −oh. Попытка синтеза приводит к полимерам. [ 3 ] Это низкоокисление (+1) серная кислота. [ 4 ] Это арреневая кислота для окиси диульфур . Соли, полученные из тиолинозной кислоты, которая также неизвестна, называются «тиосульфитами», «тионосульфитами» или «серымиротиотами». Ион s = so 2−
2 .
Структуры
[ редактировать ]Другими возможными изомерами являются дигидроксидисульфановый или гиподитионный кислотный хоссох, линейная цепь и тиотионил -гидроксид (s = s (OH) 2 ) таутомер, где водород перемещался из серы к кислороду. [ 5 ] Хоссош может иметь два разных ротамеров с симметрией C 1 и C 2 . Изомер с одним водородом на сере и один на кислороде является наиболее стабильным в соответствии с расчетами. [ 6 ]
Дитиозолическая кислота
[ редактировать ]Аналог серы тиозольфурической кислоты ( HS -S (= O) 2 -OH ), в котором два атома серы отражаются от центрального атома серы линейной дигидрогена (S =) 2 s (−sh) 2 или ( − S-) 2 с 2+ (−sh) 2 ) также изучался вычислительно. [ 7 ]
Реакция
[ редактировать ]По -видимому, он разлагается на оксид полисульфана или политионные кислоты в воде, которая называется жидкостью Wakenroder . [ 5 ]
В щелочных условиях тиозольстная кислота быстро ухудшается образуя смесь сульфида, серы, сульфита и тиосульфата. В кислых условиях он также будет образовывать сероводород и диоксид серы. Некоторые из них реагируют на образование пентатионата и других политионатов . Тиолифурная кислота реагирует с серной кислотой с получением тетратионата, а с тиолиновой кислотой - гексатионат. [ 8 ]
Эфир
[ редактировать ]Четыре изомера возможны для R 2 S 2 O 2 , по крайней мере, ограничивая серу до ди- и тетравалентности: (ro) 2 s = s, rossor, rs (o) 2 sr и rs (o) sor. Для первых двух групп R эквивалентны, и во вторых двух они не являются неравенными. Простым примером является диэтилтисульфит, (Eto) 2 s = s. Он также известен как диэтилтионосульфит. Это стереохимически жесткий на ЯМР -шкале с примерно 140 ° C, что несколько похоже на диэтилсульфоксид. Многие производные были приготовлены из гликолей. Из мезо-гидробензоина (PHCH (OH) -CH (OH) pH) pH) получают два изомера; Третий изомер получает D , L -phch (OH) -CH (OH) pH. [ 9 ] [ 10 ]
Реакция с простыми алкоксидными источниками с дихлоридом дивлорида дает неразветвленный россор. Они несмешиваются в воде, но растворяются в бензоле или тетрахлориде углерода. [ 8 ] Эти виды менее жесткие, чем эфиры тиосульфита.
Ссылки
[ редактировать ]- ^ Jump up to: а беременный Международный союз чистой и прикладной химии (2005). Номенклатура неорганической химии (рекомендации IUPAC 2005). Кембридж (Великобритания): RSC - Iupac . ISBN 0-85404-438-8 . п. 139. Электронная версия.
- ^ Acd chemsketch Имя бесплатно
- ^ Шмидт, Хайнар; Ральф Студель; Детлев Суэлцл; Гельмут Шварц (1992). «Соединения серы. 148. Генерация и характеристика дигидрокси дисульфида, Хоссо: цепный изомер тиозльфурной кислоты». Неорганическая химия . 31 (6): 941–944. doi : 10.1021/ic00032a004 . ISSN 0020-1669 .
- ^ +1 - это среднее состояние окисления двух структурно разных атомов серы. Внешний атом имеет количество окисления -1, в то время как центральный атом серы имеет состояние окисления +3.
- ^ Jump up to: а беременный Wiberg, Egon; Wiberg, Nils (2001). Неорганическая химия . Академическая пресса. п. 552. ISBN 9780123526519 Полем Получено 3 ноября 2013 года .
- ^ Миаскевич, Карол; Ральф Студель (1991). «Соединения серы. Часть 140. Структуры и относительная стабильность семи изомерных форм H2S2O2». Журнал химического общества, Dalton Transactions (9): 2395. DOI : 10.1039/DT9910002395 . ISSN 0300-9246 .
- ^ Нишимото, Акико; Чжан, Дейзи Ю. (2003). «Гипервалентность в серых ? Серные буквы . 26 (5/6): 171–180. doi : 10.1080/02786110310001622767 . S2CID 95470892 .
- ^ Jump up to: а беременный Наир, К.Г. Рамачандран; Ар Васудева Мурти (19 июня 1961 года). «Гидролитические реакции сложных эфиров и амидов тиозолистической кислоты» (PDF) . Труды Индийской академии наук . 56 (3). Бангалор: 130–140. doi : 10.1007/bf03045863 . S2CID 35057986 .
- ^ Эли Зисман-Колман Дэвид Н. Харпп "Дисульфиды Диалокси и их филионосульфитные изомеры" J. Sulfur Chemistry 2004, vol. 25, с. 155–182. doi : 10.1080/1741599342000202176
- ^ Зисман-Колман, Эли; Чарльз Б. Абрамс; Дэвид Н. Харпп (2003). «Синтез новых циклических тионосульфитов». Журнал органической химии . 68 (18): 7059–7062. doi : 10.1021/jo0346306 . ISSN 0022-3263 . PMID 12946149 .