Метилбисульфат
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Метил гидросульфат | |
| Систематическое название ИЮПАК Метоксисульфоновая кислота | |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol ) | |
| КЭБ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.000.834 |
| Номер ЕС |
|
| КЕГГ | |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| (СН 3 )HSO 4 | |
| Молярная масса | 112.10 g·mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
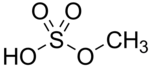
Метилбисульфат представляет собой химическое соединение с молекулярной формулой (СН 3 )HSO 4 . Это соединение представляет собой монометиловый эфир кислоты серной . Его структура CH 3 -O-S(=O) 2 -OH . Значение метилбисульфата состоит в том, что он является промежуточным продуктом гидролиза важного реагента диметилсульфата . (СН 3 ) 2 SO 4 : [1]
- (CH 3 ) 2 SO 4 + H 2 O → (CH 3 )HSO 4 + CH 3 OH
Метилбисульфат – сильная кислота:
- (CH 3 )HSO 4 → (CH 3 )SO − 4 + H +
Метилбисульфат стал известен общественности в 1993 году, когда было обнаружено, что некоторые в метана метилбисульфат с соединения ртути катализируют превращение хорошими выходами и превосходной селективностью в концентрированной серной кислоте . [2] Однако из-за токсичности и опасений по поводу использования ртути только в 1998 году были обнаружены комплексы платины, катализирующие реакцию ртути. CH 4 от SO 3 и О 2 что это попало в центр внимания: [3] [4] [5]
- 2 CH 4 + 2 SO 3 + O 2 → 2 (CH 3 )HSO 4
Это открытие указало на возможный метод переработки недорогого и широко доступного метана ( природного газа ) в метанол , который одновременно является более полезным химическим веществом и его легче транспортировать, чем метан. Предполагается, что процесс протекает через промежуточный продукт, содержащий Pt − CH 3 . Группа [6]
с метилбисульфатом, Основание, сопряженное используется в качестве противоиона в рецептурах некоторых фармацевтических препаратов , где его обычно называют метилсульфатом . [7]
Ссылки
[ редактировать ]- ^ Робертсон, Р.Э.; Сугамон, ЮВ (1966). «Гидролиз диметилсульфата и диэтилсульфата в воде» . Канадский химический журнал . 44 (14): 1728–1730. дои : 10.1139/v66-260 .
- ^ Периана, РА; Таубе, диджей; Эвитт, скорая помощь; Лоффлер, Д.Г.; Вентчек, PR; Восс, Г.; Масуда, Т. (1993). «Высокопроизводительная система окисления метана в метанол, катализируемая ртутью». Наука . 259 (5093): 340–343. дои : 10.1126/SCIENCE.259.5093.340 . ПМИД 17832346 .
- ^ Христов, И.Г.; Зиглер, Т. (2003). «Возможная роль SO 3 как окислителя в функционализации метана каталитическим процессом. Исследование теории функционала плотности». Металлоорганические соединения . 22 (8): 1668–1674. дои : 10.1021/om020774j .
- ^ Периана, РА; Миринов О.; Таубе, диджей; Гэмбл, С. (2002). «Высокопроизводительная конверсия метана в метилбисульфат, катализируемая катионами йода». Химические коммуникации (20): 2376–2377. дои : 10.1039/b205366g .
- ^ Вольф, Д. (1999). «Высокие выходы метанола из метана путем активации связей CH при низких температурах». Angewandte Chemie, международное издание . 37 (24): 3351–3353. doi : 10.1002/(SICI)1521-3773(19981231)37:24<3351::AID-ANIE3351>3.0.CO;2-U .
- ^ Периана, РА; Таубе, диджей; Гэмбл, С.; Таубе, Х.; Сато, Т.; Фуджи, Х. (1998). «Платиновые катализаторы высокопроизводительного окисления метана до производного метанола». Наука . 280 (5363): 560–564. дои : 10.1126/science.280.5363.560 . ПМИД 9554841 .
- ^ Международные непатентованные наименования (МНН) фармацевтических субстанций . Всемирная организация здравоохранения .