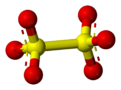
дитионат
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК
дитионат
| |||
| Систематическое название ИЮПАК
Бис(триоксидосульфат)( S — S )(2-) [ 1 ] | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| КЭБ | |||
| ХимическийПаук | |||
ПабХим CID
|
|||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 22О 2− 6 | |||
| Молярная масса | 160.126 g mol −1 | ||
| Кислотность ( pKa ) | 0.5 [ 2 ] | ||
| Конъюгатная кислота | Дитионовая кислота | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Дитионатный или метабисульфатный ) анион S (
22О 2−
6 – серы . оксоанион [ 3 ] производное дитионовой кислоты H 2 S 2 O 6 . Его химическая формула иногда записывается в полуструктурном формате, как [O 3 SSO 3 ] 2− . Это первый член политионатов .
Атомы серы дитионат-иона находятся в степени окисления +5 из-за наличия связи S–S. Как правило, дитионаты образуют стабильные соединения, которые трудно окисляются или восстанавливаются. Сильные окислители окисляют их до сульфатов , а сильные восстановители восстанавливают до сульфитов и дитионитов . [ 4 ] Водные растворы дитионатов достаточно устойчивы и могут кипятиться без разложения. [ 5 ]
При γ-облучении кристаллических дитионатов образуется SO. •−
3 ион- радикала . [ 6 ] Неспаренный электрон в SO •−
Радикал 3 можно обнаружить с помощью электронного парамагнитного резонанса , а дитионат бария был предложен в качестве основы для дозиметра радиации . [ 7 ]
Дитионат-ион может действовать как бидентатный лиганд . [ 8 ]
Структура дитионат-иона в твердом состоянии O шахматная в Na 2 S 2 O 6 ·2H 2 , тогда как в безводной калиевой соли она практически затмевается . [ 4 ]
Соединения
[ редактировать ]Соединения, содержащие дитионат-ион, включают:
- дитионат натрия , Na 2 S 2 O 6
- дитионат калия , K 2 S 2 O 6
- дитионат бария, BaS 2 O 6
Ссылки
[ редактировать ]- ^ «Дитионат(2-) (CHEBI:29209)» . Химические соединения биологического интереса (ХЭБИ) . Великобритания: Европейский институт биоинформатики.
- ^ Перрин, Д.Д., изд. (1982) [1969]. Константы ионизации неорганических кислот и оснований в водных растворах . Химические данные ИЮПАК (2 nd ред.). Оксфорд: Пергамон (опубликовано в 1984 г.). Запись 63. ISBN. 0-08-029214-3 . LCCN 82-16524 .
- ^ Международный союз теоретической и прикладной химии (2005). Номенклатура неорганической химии (Рекомендации ИЮПАК 2005 г.). Кембридж (Великобритания): RSC – IUPAC . ISBN 0-85404-438-8 . п. 130. Электронная версия.
- ^ Перейти обратно: а б Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Коттон, Ф. Альберт ; Уилкинсон, Джеффри ; Мурильо, Карлос А.; Бохманн, Манфред (1999), Передовая неорганическая химия (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5
- ^ Радиационная химия дитионатов Г. С. Мурти, Р. Л. Игер и К. Дж. МакКаллум Кан. Дж. Хим. 49(22),(1971), 3733
- ^ Barium dithionate as an EPR dosemeter Baran M.P., Bugay O.A., Kolesnik S. P., Maksimenko V. M., Teslenko V. V., Petrenko T. L. Desrosiers M. F. Radiation Protection Dosimetry 2006 120 , 202; дои : 10.1093/rpd/nci531
- ^ Структуры некоторых комплексов меди (II), содержащих S
22О 2−
6 Ион Исии М. Вестник Университета Ямагата 5 , 1,(2001), 7
Внешние ссылки
[ редактировать ]![]() СМИ, связанные с дитионат-ионом, на Викискладе?
СМИ, связанные с дитионат-ионом, на Викискладе?