Нитрон

В органической химии нитрон состоящая — функциональная группа, из N - имина оксида . Общая структура Р 1 Р 2 С=Н + (-О − )(−R 3 ) , где R 3 это не водород . Их основное применение — промежуточные продукты химического синтеза . Нитрон — это 1,3-диполь, используемый в циклоприсоединениях , и имитатор карбонила .
Структура
[ редактировать ]Нитроны, как тетразамещенная двойная связь , допускают цис - транс -изомерию . [ 1 ] : 474
Генерация нитронов
[ редактировать ]Типичными источниками нитрона являются гидроксиламина окисление или конденсация с карбонильными соединениями . Вторичные гидроксиламины окисляются на воздухе до нитронов в течение нескольких недель, при этом соли меди ускоряют этот процесс. [ 1 ] : 476 [ 2 ] : 332–333 Наиболее распространенным реагентом, используемым для окисления гидроксиламинов, является водный раствор оксида ртути : [ 1 ] : 476 [ 3 ]

Однако гидроксиламин с двумя α- водородами может быть ненасыщенным с обеих сторон. Карбонильная конденсация позволяет избежать этой двусмысленности... [ 4 ]

...но ингибируется, если оба кетоновых заместителя объемистые. [ 1 ] : 477
В принципе, N - алкилирование могло бы производить нитроны из оксимов , но на практике электрофилы обычно осуществляют смесь N- и O -атак. [ 1 ] : 479 [ 2 ] : 334
Реакции
[ редактировать ]Некоторые нитроны олигомеризуются: [ 1 ] : 483 [ 2 ] : 334,337-338 [ 5 ]
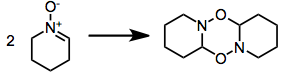
Синтезы с предшественниками нитрона устраняют проблему повышения температуры и преувеличивают энтропийные факторы; или с избытком нитрона.
Карбонильный имитатор
[ редактировать ]Как и многие другие ненасыщенные функциональные группы, нитроны активируют α- и β-углероды для реакции. α-углерод является электрофилом, а β-углерод — нуклеофилом; то есть нитроны поляризуются так же, как карбонилы и нитрилы, но в отличие от нитросоединений и производных винилсеры. [ 1 ] : 483 [ 2 ] : 338–340
Нитроны чрезвычайно легко гидролизуются до соответствующего карбонила и N-гидроксиламина. [ 1 ] : 491 [ 2 ] : 344
1,3-диполярное циклоприсоединение
[ редактировать ]В качестве 1,3-диполей нитроны совершают [3+2] циклоприсоединение . [ 6 ] Например, диполярофильный алкен соединяется с образованием изоксазолидина :

другие реакции замыкания цикла : Известны и [ 7 ] включая формальные [3+3] и [5+2] циклоприсоединения . [ 6 ]
изомеризация
[ редактировать ]Дезоксигенирующие реагенты , свет или нагревание катализируют перегруппировку в амид . Кислоты катализируют перегруппировку в эфир оксима . [ 1 ] : 489–490 [ 2 ] : 345–347
Снижение
[ редактировать ]Гидриды добавляются с образованием гидроксиламинов . Восстановление кислот Льюиса (например, металлов , SO 2 ) вместо этого дезоксигенирует до имина . [ 1 ] : 490 [ 2 ] : 343
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я дж Хамер, Ян; Макалузо, Энтони (1 августа 1964 г.). «Нитроны» . Химические обзоры . 64 (4): 473–495. дои : 10.1021/cr60230a006 . ISSN 0009-2665 .
- ^ Jump up to: а б с д и ж г Дельпьер, Греция; Ламхен, М. (1965). «Нитроны» . Ежеквартальные обзоры, Химическое общество . 19 (4): 329. doi : 10.1039/qr9651900329 . ISSN 0009-2681 .
- ^ Тизинг, Ян; Майер, Ганс (1957). «Циклические нитроны II. О полимерах 2.3.4.5-тетрагидропиридин-N-оксида и родственных соединениях». «Анн» Юстуса Либиха. Хим. 609 : 46-57. дои : 10.1002/jlac.19576090105 .
- ^ Экснер, О. (1951). «Новый синтез N-метилкетоксимов». ХимПлюсХим . 16 : 258-267. дои : 10.1135/cccc19510258 .
- ^ Тизинг, Ян; Майер, Ганс (1956). «Циклический нитрон I: димеры 2.3.4.5-тетрагидропиридин-N-оксид». хим. Бер. 89 (9): 2159-2167. дои : 10.1002/cber.19560890919 .
- ^ Jump up to: а б Ян, Цзюн (2012). «Последние достижения в химии нитронов». Синлетт . 23 : 2293-97. дои : 10.1055/s-0032-1317096 .
- ^ Мурахаси, Сюн-Ичи; Имада, Ясуси (15 марта 2019 г.). «Синтез и превращения нитронов для органического синтеза». Химические обзоры . 119 (7): 4684–4716. doi : 10.1021/acs.chemrev.8b00476 . ПМИД 30875202 . S2CID 80623450 .