Вставка пакета лекарств
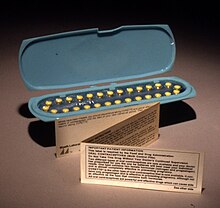
Вставка пакета - это документ, включенный в , который пакет лекарства предоставляет информацию об этом препарате и его использовании. Для рецептурных лекарств вставка является технической , предоставляя медицинскую информацию о том, как назначить препарат. Вставки пакетов для рецептурных лекарств часто включают отдельный документ, называемый «вставка пакета пациента» с информацией, написанной на простом языке, предназначенной для конечного пользователя -человека, который примет препарат или отдаст препарат другому человеку, такому как несовершеннолетний. Вставки для безрецептурных лекарств также написаны явно. [ 1 ] [ 2 ]
В Соединенных Штатах маркировка для практикующего здравоохранения называется «предписывающая информация» (PI), а маркировка для пациентов и/или лиц, осуществляющих уход, включает в себя «руководства по лекарствам», «вставки пакета пациентов» и «инструкции для использования». [ 1 ] В Европе технический документ называется « Сводка характеристик продукта » (SMPC), а документ для конечных пользователей называется « Информационная листовка для пациента » (PIL) или «пакет листовка». [ 3 ]
Аналогичные документы, прикрепленные к внешней стороне пакета, иногда называют упорными .
Ответственные агентства
[ редактировать ]В каждой стране или регионе есть свой регулирующий орган.
В Европейском союзе Европейское агентство по лекарственным средствам обладает юрисдикцией, а соответствующие документы называются «сводкой характеристик продукта» (SPC или SMPC), а документ для конечных пользователей называется «листовка для пациента» или «листовка упаковки». SPC не предназначен для того, чтобы дать общие советы по обращению с состоянием, но указывает, как продукт должен использоваться для конкретного лечения. Он составляет основу информации для медицинских работников, чтобы знать, как безопасно и эффективно использовать конкретный продукт. Листочка упаковки, поставляемая с продуктом, предназначена для конечных пользователей. [ 3 ]

В Соединенных Штатах Управление по контролю за продуктами и лекарствами (FDA) определяет требования к вставкам пакета пациентов. В Соединенных Штатах FDA иногда выпускает изменения в ранее утвержденные вставки пакетов, во многом так же, как производитель автомобилей будет выпускать отзывы , обнаружив проблему с определенным автомобилем. Список изменений маркировки наркотиков 1997 года можно найти на веб -сайте FDA, здесь . Первая вставка пакета для пациентов, требуемая FDA, была в 1968 году, что предписывает, что препарат для ингаляции изопротеренола должен содержать краткое предупреждение о том, что чрезмерное использование может вызвать трудности с дыханием. [ 4 ] [ Необходимый источник необходимы ]] Вторая вставка пакета пациентов, требуемая FDA, была в 1970 году, что обязывание комбинированных оральных противозачаточных таблеток должна содержать информацию для пациента о конкретных рисках и преимуществах. [ 5 ] [ Необходимый источник необходимы ]] Проблема с пакетом пациента была пересмотрена в 1980 году и в 1995 году без принятия окончательных действий. [1] Наконец, в январе 2006 года FDA опубликовало основной пересмотр в руководящих принципах INSERT PATED PACEDERT, первого за 25 лет. [ Цитация необходима ] Новые требования включают раздел под названием «Основные моменты», в котором суммируется наиболее важная информация о преимуществах и рисках; содержимое для легкой ссылки; дата первоначального одобрения продукта; и бесплатный номер и адрес интернета, чтобы поощрять более широкую отчетность информации о подозреваемых неблагоприятных событиях.
Другие национальные или международные организации, которые регулируют медицинскую информацию, включают Министерство здравоохранения, труда и социального обеспечения Японии (MHLW). Другие страновые агентства, особенно в случае стран ЕС ( Европейский Союз ) и кандидатов, а также страны Южной Америки и многие в Азии и на Дальнем Востоке, в значительной степени полагаются на работу этих трех основных регуляторов. [ Цитация необходима ]
Разделы предписанной информации
[ редактировать ]Информация о назначении следует за одним из двух форматов: формат «Правило маркировки врача» или формат «старый» (не PLR). Для «старого» маркировки формата «заголовок продукта» может быть перечислен первым и может включать в себя собственное имя (если таковое), непременное имя, форму (ы) дозировки и другую информацию о продукте. Другие разделы следующие:
- Описание - включает в себя собственное название (если есть), непременное название , дозировую форму (ы), качественную и/или количественную информацию об ингредиентах, фармакологический или терапевтический класс лекарственного средства, химическое название и структурная формула препарата и, если уместно, Другая важная химическая или физическая информация, такая как физическая констант или рН.
- Клиническая фармакология - рассказывает, как работает лекарство в организме, как оно поглощается и устранено, и каковы его последствия могут быть в различных концентрациях. Может также содержать результаты различных клинических испытаний (исследования) и/или объяснений влияния лекарства на различные группы населения (например, дети, женщины и т. Д.).
- Показания и использование - Использование (показания), для которых препарат был одобрен FDA (например, мигрени, судороги, высокое кровяное давление). Врачи на законных основаниях могут и часто назначают лекарства для целей, не указанных в этом разделе (так называемые « не по назначению »).
- Противопоказания следует использовать лекарство - перечисляет ситуации, в которых не , например, у пациентов с другими заболеваниями, такими как проблемы с почками или аллергией
- Предупреждения - охватывает возможные серьезные побочные эффекты , которые могут возникнуть (например, предупреждение о штучной упаковке )
- Меры предосторожности - объясняет, как безопасно использовать лекарство, включая физические нарушения, пищу ( грейпфруты ) и лекарственные взаимодействия; Например, «не пей алкоголь во время принимая это лекарство» или «не принимайте это лекарство, если вы в настоящее время принимаете ингибиторы MAOI »
- Побочные реакции - перечисляет все побочные эффекты, наблюдаемые во всех исследованиях препарата (в отличие от опасных побочных эффектов, которые отдельно перечислены в разделе «Предупреждения»)
- Использование в конкретных популяциях ( беременность , лактация ( грудное вскармливание ), женщины и мужчины репродуктивного потенциала, педиатрия , гериатрия )
- Злоупотребление наркотиками и зависимость - предоставляет информацию о том, может ли длительное использование лекарства вызвать физическую зависимость (включенная только в том случае, если это применимо)
- Передозировка - дает результаты передозировки и обеспечивает рекомендуемые действия в таких случаях
- Дозировка и администрирование - дает рекомендованную дозировку (ы); может перечислить более одного для разных состояний или разных пациентов (например, более низкие дозировки для детей)
- Как поставляется - включает в себя форму (ы) дозировки , прочность (ы), единицы, в которых обычно доступна форма дозировки, идентифицируя функции дозировки, такие как Национальный кодекс лекарственного средства (NDC) и специальные Условия управления и хранения (например, «Хранить между 68 и 78 ° F»)
Другое использование и инициативы
[ редактировать ]В дополнение к очевидному использованию включения с лекарствами, в других формах использовалась или предоставлена информация о назначении. предоставляется информация о назначении для тысяч рецептурных лекарств В Соединенных Штатах на веб -сайте Dailymed , предоставленных Национальной медициной. [ 6 ]
Южная Африка взяла на себя инициативу по обеспечению доступных всех пакетов в электронном виде через Интернет, указанный по торговым названиям, общему названию и классификации, а Канада работает над аналогичными возможностями. Британский сборник электронных лекарств [ 7 ] Предоставляет свободно доступный онлайн -доступ как к информационным листочкам для пациентов (предназначенных для потребителей), так и сводки характеристик продукта (предназначенные для медицинских работников) для продуктов, доступных в Великобритании.
Понятно, что информация о пациентах обычно генерируется изначально на родном языке страны, где разрабатывается продукт. Это приводит к несоответствию в формате, терминологии, тоне и содержании. Таблетки (Система локализации языка информации о пациентах)-это годовая попытка Европейской комиссии по производству прототипа, который будет поддерживать создание различных видов медицинской документации одновременно на нескольких языках, храня информацию в базе данных и разрешая разнообразие форм и языков вывода.
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а беременный Натан, Джозеф П.; VIDER, ETTY (2015). «Вставка пакета» . US Pharm . 40 (5): 8–10.
- ^ Надин Ванлаер (31 августа 2006 г.). «Вставки пакета лекарств: буква закона - упаковка шлюз» . Упаковочный шлюз .
- ^ Jump up to: а беременный «Авторизация маркетинга - требования к информации продукта» . Европейское агентство лекарств . Получено 18 августа 2018 года .
- ^ 33 Фед. Рег. 8812 (1968) (кодифицировано в 21 CFR §201.305)
- ^ 33 Фед. Рег. 9001 (1970) (кодифицировано в 21 CFR §310.510)
- ^ "Дейлимент" . Dailemed.nlm.nih.gov . Получено 2021-08-07 .
- ^ «Дом - электронные лекарства сборка (EMC)» . www.medicines.org.uk . Получено 2021-08-07 .
Внешние ссылки
[ редактировать ]- Южноафриканский электронный пакет вставки
- EMA Руководство по подготовке SMPC
- Electronic Medicines Compendium , который опубликовал SMPC и пакетные листочки в Великобритании
- Dailymed.nlm.nih.gov лекарственные метки на веб -сайте Dailymed
- Labels.fda.gov лекарственные метки на веб -сайте FDA