Белок Л
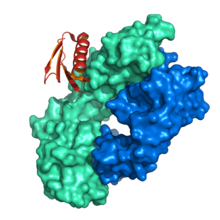
| Домен белка L b1 | |||
|---|---|---|---|
 | |||
| Идентификаторы | |||
| Символ | PpL | ||
| Пфам | PF02246 | ||
| ИнтерПро | ИПР003147 | ||
| ОБЛАСТЬ ПРИМЕНЕНИЯ 2 | 1MHH / ОБЛАСТЬ ПРИМЕНЕНИЯ / СУПФАМ | ||
| |||
Белок L был впервые выделен с поверхности бактериального вида Peptostreptococcus magnus, и было обнаружено, что он связывает иммуноглобулины посредством взаимодействия L-цепи , из-за чего было предложено название. [ 2 ] Он состоит из 719 аминокислотных остатков. [ 3 ] Молекулярную массу белка L, очищенного из клеточных стенок Peptostreptoccus magnus, сначала оценили как 95 кДа методом SDS-PAGE в присутствии восстановителя 2-меркаптоэтанола, а молекулярную массу определили до 76 кДа методом гель -хроматографии в присутствии 6 М гуанидин HCl. Белок L не содержит межцепочечных дисульфидных петель и не состоит из субъединиц, связанных дисульфидными связями. Это кислая молекула с pI 4,0. [ 4 ] В отличие от белка A и белка G , которые связываются с Fc-областью иммуноглобулинов ( антител ), белок L связывает антитела посредством легкой цепи взаимодействия . Поскольку ни одна часть тяжелой цепи не участвует во взаимодействии связывания, белок L связывает более широкий диапазон классов антител, чем белок A или G. Белок L связывается с представителями всех классов антител, включая IgG , IgM , IgA , IgE и IgD . Одноцепочечные вариабельные фрагменты ( scFv ) и Fab-фрагменты также связываются с белком L.
Несмотря на такой широкий диапазон связывания, белок L не является универсальным белком , связывающим антитела . Связывание с белком L ограничено теми антителами, которые содержат легкие каппа-цепи. У людей и мышей большинство молекул антител содержат легкие цепи каппа (κ), а остальные имеют легкие цепи лямбда (λ). Белок L эффективен только для связывания определенных подтипов легких цепей каппа. Например, он связывает человеческие подтипы VκI, VκIII и VκIV, но не связывает подтип VκII. Связывание мышиных иммуноглобулинов ограничено теми, которые имеют легкие цепи VκI. [ 5 ]
Учитывая эти специфические требования к эффективному связыванию, основным применением иммобилизованного белка L является очистка моноклональных антител из асцита или клеточной культуры супернатанта , которые, как известно, содержат легкую каппа-цепь . Белок L чрезвычайно полезен для очистки моноклональных антител, содержащих VLκ, из культурального супернатанта, поскольку он не связывает бычьи иммуноглобулины, которые часто присутствуют в средах в качестве добавки к сыворотке . Кроме того, белок L не влияет на антигенсвязывающий участок антитела, что делает его полезным для иммунопреципитации анализов , даже с использованием IgM.
Ген белка L
[ редактировать ]Ген белка L содержит пять компонентов: сигнальную последовательность из 18 аминокислот; NH2 -концевой участок («А») из 79 остатков; пять гомологичных повторов «В» по 72-76 аминокислот каждый; СООН-концевая область двух дополнительных повторов «С» (по 52 аминокислоты каждый); гидрофильный, богатый пролином предполагаемый участок клеточной стенки («W») после C-повторов; гидрофобный мембранный якорь («М»). Было обнаружено, что повторы B (36 кДа) ответственны за взаимодействие с легкими цепями Ig. [2]
Другие белки, связывающие антитела
[ редактировать ]Помимо белка L, другие бактериальные белки, связывающие иммуноглобулины, такие как белок A , белок G и белок A/G для очистки, иммобилизации или обнаружения иммуноглобулинов обычно используются . Каждый из этих иммуноглобулин-связывающих белков имеет различный профиль связывания антител с точки зрения распознаваемой части антитела, а также вида и типа антител, с которыми оно будет связываться.
Ссылки
[ редактировать ]- ^ Грайль М., Харрисон С., Крамп М.П., Финдлоу С.К., Хаусден Н.Г., Мюллер Б.Х., Баттейл-Пуаро Н., Сибай Г., Саттон Б.Дж., Тауссиг М.Дж., Жоливе-Рейно С., Гор М.Г., Стура Э.А. (декабрь 2002 г.). «Доказательства пластичности и структурной мимикрии на границе раздела легкая цепь иммуноглобулина-белок L» . J Биол Хим . 277 (49): 47500–6. дои : 10.1074/jbc.M206105200 . ПМИД 12221088 .
- ^ Бьорк Л. (февраль 1988 г.). «Белок L. Новый белок бактериальной клеточной стенки, обладающий сродством к цепям Ig L» . Дж. Иммунол . 140 (4): 1194–7. дои : 10.4049/jimmunol.140.4.1194 . ПМИД 3125250 . S2CID 35781778 .
- ^ Кастерн В., Сьёбринг У., Бьорк Л. (июнь 1992 г.). «Структура пептострептококкового белка L и идентификация повторяющегося домена, связывающего легкую цепь иммуноглобулина» . Ж. Биол. Хим . 267 (18): 12820–5. дои : 10.1016/S0021-9258(18)42349-6 . ПМИД 1618782 .
- ^ Акерстрем Б., Бьорк Л. (ноябрь 1989 г.). «Белок L: бактериальный белок, связывающий легкую цепь иммуноглобулина. Характеристика связывания и физико-химических свойств» . Ж. Биол. Хим . 264 (33): 19740–6. дои : 10.1016/S0021-9258(19)47174-3 . ПМИД 2479638 .
- ^ Нильсон Б.Х., Лёгдберг Л., Кастерн В., Бьорк Л., Акерстрем Б. (август 1993 г.). «Очистка антител с использованием белковых L-связывающих каркасных структур в вариабельном домене легкой цепи». Дж. Иммунол. Методы . 164 (1): 33–40. дои : 10.1016/0022-1759(93)90273-а . ПМИД 8360508 .