Моноклональное антитело
мАт Моноклональное антитело ( полученной , реже называемое моАт ) представляет собой антитело, полученное из клеточной линии, путем клонирования уникальных лейкоцитов . Все последующие антитела, полученные таким образом, восходят к уникальной родительской клетке.
Моноклональные антитела могут иметь моновалентное сродство, связываясь только с одним и тем же эпитопом (частью антигена , которая распознается антителом). [3] Напротив, поликлональные антитела связываются с несколькими эпитопами и обычно производятся несколькими различными линиями плазматических клеток , секретирующих антитела . Биспецифические моноклональные антитела также могут быть созданы путем увеличения терапевтических мишеней одного моноклонального антитела до двух эпитопов.
Можно производить моноклональные антитела, специфически связывающиеся практически с любым подходящим веществом; затем они могут служить для его обнаружения или очистки. Эта возможность стала исследовательским инструментом в биохимии , молекулярной биологии и медицине . Моноклональные антитела используются в диагностике таких заболеваний, как рак и инфекции. [4] и используются терапевтически при лечении, например, рака и воспалительных заболеваний.
История
[ редактировать ]В начале 1900-х годов иммунолог Пауль Эрлих предложил идею Zauberkugel – « волшебной пули », задуманной как соединение, избирательно воздействующее на болезнетворный организм и способное доставлять токсин для этого организма. Это легло в основу концепции моноклональных антител и конъюгатов моноклональных лекарств. Эрлих и Эли Мечников получили Нобелевскую премию по физиологии и медицине 1908 года за создание теоретической основы иммунологии.
К 1970-м годам были известны лимфоциты , продуцирующие одно антитело, в форме множественной миеломы – рака, поражающего В-клетки . Эти аномальные антитела или парапротеины использовались для изучения структуры антител, но получить идентичные антитела, специфичные к данному антигену , пока не удалось . [5] : 324 В 1973 году Джеррольд Швабер описал производство моноклональных антител с использованием гибридных клеток человека и мыши. [6] человеческого происхождения Эта работа по-прежнему широко цитируется среди тех, кто использует гибридомы . [7] В 1975 году Жоржу Келеру и Сезару Мильштейну удалось слить клеточные линии миеломы с В-клетками для создания гибридом, которые могли продуцировать антитела, специфичные к известным антигенам и иммортализованные. [8] они и Нильс Кай Йерне получили Нобелевскую премию по физиологии и медицине в 1984 году. За это открытие [8]
В 1988 году Грегори Винтер и его команда впервые разработали методы гуманизации моноклональных антител. [9] устранение реакций, которые вызывали многие моноклональные антитела у некоторых пациентов. К 1990-м годам исследования достигли прогресса в использовании моноклональных антител в терапевтических целях, а в 2018 году Джеймс П. Эллисон и Тасуку Хондзё получили Нобелевскую премию по физиологии и медицине за открытие терапии рака путем ингибирования негативной иммунной регуляции с использованием моноклональных антител, которые предотвращают рак. тормозные связи. [10]
Переводческая работа, необходимая для реализации этих идей, принадлежит Ли Надлеру. Как поясняется в статье Национального института здравоохранения: «Он был первым, кто открыл моноклональные антитела, направленные против антигенов, специфичных для В-клеток человека, и, по сути, все известные антигены, специфичные для В-клеток человека, были обнаружены в его лаборатории. трансляционный исследователь, поскольку он использовал эти моноклональные антитела для классификации человеческих В-клеточных лейкозов и лимфом, а также для создания терапевтических средств для пациентов. пациент с В-клеточной лимфомой)». [11]
Производство
[ редактировать ]



Развитие гибридомы
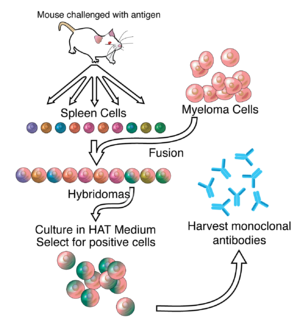
[ редактировать ]Большая часть работ по производству моноклональных антител связана с производством гибридом, которое включает в себя идентификацию антигенспецифичных клеток плазмы/плазмобластов, которые продуцируют антитела, специфичные к интересующему антигену, и слияние этих клеток с клетками миеломы . [8] В-клетки кролика можно использовать для образования гибридомы кролика . [12] [13] Полиэтиленгликоль используется для слияния соседних плазматических мембран. [14] но вероятность успеха низкая, поэтому используется селективная среда, в которой могут расти только слитые клетки. Это возможно, поскольку клетки миеломы утратили способность синтезировать гипоксантин-гуанин-фосфорибозилтрансферазу (HGPRT) — фермент, необходимый для синтеза спасательных нуклеиновых кислот. Отсутствие HGPRT не является проблемой для этих клеток, если только синтеза пуринов de novo не нарушается путь . Воздействие на клетки аминоптерина ( аналога фолиевой кислоты , который ингибирует дигидрофолатредуктазу ) делает их неспособными использовать путь de novo и становятся полностью ауксотрофными по отношению к нуклеиновым кислотам , что требует дополнительных добавок для выживания.
Селективную культуральную среду называют средой HAT, поскольку она содержит гипоксантин , аминоптерин и тимидин . Эта среда является селективной для слитых ( гибридомных ) клеток. Неслитые клетки миеломы не могут расти, поскольку в них отсутствует HGPRT и, следовательно, они не могут реплицировать свою ДНК. Несросшиеся клетки селезенки не могут расти бесконечно из-за ограниченной продолжительности жизни. Только слитые гибридные клетки, называемые гибридомами, способны неограниченно расти в среде, поскольку партнерская клетка селезенки поставляет HGPRT, а партнер миеломы обладает свойствами, которые делают ее бессмертной (аналогично раковой клетке).
Затем эту смесь клеток разбавляют и выращивают клоны из одиночных родительских клеток в лунках для микротитрования. Антитела, секретируемые различными клонами, затем анализируются на их способность связываться с антигеном (с помощью такого теста, как ELISA или анализ на микрочипах антигенов) или иммунодот -блоттинга . Затем для будущего использования отбирается наиболее продуктивный и стабильный клон.
Гибридомы можно выращивать неограниченное время в подходящей среде для культивирования клеток. Их также можно вводить мышам (в брюшную полость , окружающую кишечник). Там они производят опухоли, секретирующие богатую антителами жидкость, называемую асцитической жидкостью.
Среду необходимо обогащать во время селекции in vitro , чтобы способствовать росту гибридомы. Этого можно достичь путем использования слоя питающих клеток фиброцитов или дополнительной среды, такой как бриклон. Можно использовать культуральные среды, кондиционированные макрофагами. Обычно предпочтительным является производство в клеточной культуре, поскольку метод асцита болезненный для животного. Там, где существуют альтернативные методы, асцит считается неэтичным . [15]
Новая технология разработки моноклональных антител
[ редактировать ]Недавно было разработано несколько технологий моноклональных антител. [16] такие как фаговый дисплей , [17] культура одиночных В-клеток, [18] амплификация одиночных клеток из различных популяций B-клеток [19] [20] [21] [22] [23] и технологии опроса одиночных плазматических клеток. В отличие от традиционной гибридомной технологии, новые технологии используют методы молекулярной биологии для амплификации тяжелых и легких цепей генов антител с помощью ПЦР и их производства в системах бактерий или млекопитающих с помощью рекомбинантной технологии. Одно из преимуществ новых технологий применимо к нескольким животным, таким как кролик, лама, курица и другим обычным экспериментальным животным в лаборатории.
Очистка
[ редактировать ]После получения либо образца среды культивируемых гибридом, либо образца асцитической жидкости необходимо экстрагировать желаемые антитела. Загрязнения образцов клеточных культур состоят в основном из компонентов среды, таких как факторы роста, гормоны и трансферрины . Напротив, образец in vivo , скорее всего, будет содержать антитела хозяина, протеазы , нуклеазы , нуклеиновые кислоты и вирусы . другие выделения гибридом, такие как цитокины В обоих случаях могут присутствовать . Также может быть бактериальное загрязнение и, как следствие, эндотоксины , выделяемые бактериями. В зависимости от сложности среды, необходимой для культивирования клеток, и, следовательно, от загрязнений, может оказаться предпочтительным тот или иной метод ( in vivo или in vitro ).
Пробу сначала кондиционируют или готовят к очистке. Клетки, клеточный дебрис, липиды и свернувшийся материал сначала удаляют, обычно центрифугированием с последующей фильтрацией через фильтр 0,45 мкм. Эти крупные частицы могут вызвать явление, называемое загрязнением мембраны, на более поздних стадиях очистки. Кроме того, концентрация продукта в образце может быть недостаточной, особенно в случаях, когда желаемое антитело продуцируется клеточной линией с низким уровнем секретации. Поэтому образец концентрируют ультрафильтрацией или диализом .
Большинство заряженных примесей обычно представляют собой анионы, такие как нуклеиновые кислоты и эндотоксины. Их можно разделить с помощью ионообменной хроматографии . [24] Либо катионообменная анионообменная хроматография используется при достаточно низком pH , чтобы желаемое антитело связывалось с колонкой, в то время как анионы протекают через нее, либо хроматография используется при достаточно высоком pH, чтобы желаемое антитело проходило через колонку, пока анионы связывались с ней. Различные белки также можно разделить вместе с анионами на основе их изоэлектрической точки (pI). В белках изоэлектрическая точка (pI) определяется как pH, при котором белок не имеет суммарного заряда. Когда pH > pI, белок имеет суммарный отрицательный заряд, а когда pH < pI, белок имеет суммарный положительный заряд. Например, альбумин имеет pI 4,8, что значительно ниже, чем у большинства моноклональных антител, имеющих pI 6,1. Таким образом, при pH между 4,8 и 6,1 средний заряд молекул альбумина, вероятно, будет более отрицательным, тогда как молекулы моноклональных антител заряжены положительно, и, следовательно, их можно разделить. С другой стороны, трансферрин имеет pI 5,9, поэтому его нелегко отделить этим методом. Для хорошего разделения необходима разница в pI не менее 1.
Вместо этого трансферрин можно удалить с помощью эксклюзионной хроматографии . Этот метод является одним из наиболее надежных методов хроматографии. Поскольку мы имеем дело с белками, такие свойства, как заряд и сродство, не являются постоянными и меняются в зависимости от pH, поскольку молекулы протонируются и депротонируются, в то время как размер остается относительно постоянным. Тем не менее, он имеет такие недостатки, как низкое разрешение, низкая емкость и малое элюирования время .
Гораздо более быстрым одностадийным методом разделения является белков A/G аффинная хроматография . Антитело избирательно связывается с белком A/G, поэтому достигается высокий уровень чистоты (обычно >80%). Обычно суровые условия этого метода могут повредить легко повреждаемые антитела. Низкий pH может разорвать связи и удалить антитело из колонки. Помимо возможного воздействия на продукт, низкий уровень pH может привести к вытеканию белка A/G из колонки и появлению его в элюируемом образце. Доступны буферные системы для щадящего элюирования, в которых используются высокие концентрации соли, чтобы избежать воздействия на чувствительные антитела низкого pH. Стоимость также является важным фактором при использовании этого метода, поскольку иммобилизованный белок A/G является более дорогой смолой.
Для достижения максимальной чистоты за один этап можно провести аффинную очистку с использованием антигена для обеспечения специфичности антитела. В этом методе антиген, используемый для создания антитела, ковалентно прикрепляется к агарозной подложке. Если антиген представляет собой пептид , его обычно синтезируют с концевым цистеином , что позволяет избирательно прикрепляться к белку-носителю, такому как KLH , во время разработки и поддерживать очистку. Затем среду, содержащую антитела, инкубируют с иммобилизованным антигеном либо в периодическом режиме, либо при пропускании антитела через колонку, где оно селективно связывается и может удерживаться, пока примеси смываются. Затем для извлечения очищенного антитела из носителя используют элюирование буфером с низким pH или более мягким буфером с высоким содержанием соли.
Гетерогенность антител
[ редактировать ]Гетерогенность продукта характерна для моноклональных антител и других рекомбинантных биологических продуктов и обычно вводится либо перед экспрессией, либо после нее во время производства. [ нужна ссылка ]
Эти варианты обычно представляют собой агрегаты, продукты дезамидирования , варианты гликозилирования , окисленные боковые цепи аминокислот, а также присоединения амино- и карбоксильных концевых аминокислот. [25] Эти, казалось бы, незначительные структурные изменения могут повлиять на доклиническую стабильность и оптимизацию процесса, а также на терапевтическую эффективность, биодоступность и иммуногенность продукта . Общепринятый метод очистки технологических потоков моноклональных антител включает захват целевого продукта белком А , элюирование, подкисление для инактивации потенциальных вирусов млекопитающих с последующей ионной хроматографией сначала с анионными шариками , а затем с катионными шариками. [ нужна ссылка ]
Вытесняющая хроматография использовалась для идентификации и характеристики этих часто невидимых вариантов в количествах, которые подходят для последующих схем доклинической оценки, таких как фармакокинетические исследования на животных. [26] [27] Знания, полученные на этапе доклинической разработки, имеют решающее значение для лучшего понимания качества продукции и обеспечивают основу для управления рисками и повышения гибкости регулирования. Недавняя инициатива Управления по санитарному надзору за качеством пищевых продуктов и медикаментов « Качество за счет дизайна» направлена на предоставление рекомендаций по разработке и облегчению проектирования продуктов и процессов, которые максимизируют эффективность и профиль безопасности, одновременно повышая технологичность продукта. [28]
Рекомбинантный
[ редактировать ]Производство рекомбинантных моноклональных антител включает в себя технологии клонирования репертуара , CRISPR/Cas9 или фагового / дрожжевого дисплея . технологии [29] Инженерия рекомбинантных антител предполагает производство антител с использованием вирусов или дрожжей , а не мышей. Эти методы основаны на быстром клонировании сегментов гена иммуноглобулина для создания библиотек антител со слегка отличающимися аминокислотными последовательностями, из которых можно выбрать антитела с желаемой специфичностью. [30] Библиотеки фаговых антител представляют собой вариант библиотек фаговых антигенов. [31] Эти методы можно использовать для повышения специфичности, с которой антитела распознают антигены, их стабильности в различных условиях окружающей среды, их терапевтической эффективности и их обнаруживаемости в диагностических приложениях. [32] Ферментационные камеры использовались для крупномасштабного производства антител.
Химерные антитела
[ редактировать ]Хотя мышиные и человеческие антитела структурно схожи, различий между ними было достаточно, чтобы вызвать иммунный ответ при введении мышиных моноклональных антител человеку, что привело к их быстрому удалению из крови, а также к системным воспалительным эффектам и продукции человеческих антигенов. -мышиные антитела (НАМА).
Рекомбинантная ДНК исследуется с конца 1980-х годов с целью увеличения времени пребывания. В одном подходе, называемом «прививка CDR», [33] ДНК мыши, кодирующая связывающую часть моноклонального антитела, сливали с ДНК человека, продуцирующей антитела, в живых клетках. Экспрессия этой « химерной » или «гуманизированной» ДНК через культуру клеток дала частично мышиные, частично человеческие антитела. [34] [35]
Человеческие антитела
[ редактировать ]
С момента открытия возможности создания моноклональных антител ученые поставили перед собой цель создать полностью человеческие продукты, чтобы уменьшить побочные эффекты гуманизированных или химерных антител. Было предложено несколько успешных подходов: трансгенные мыши , [36] фаговый дисплей [17] и клонирование одиночных B-клеток. [16]
Расходы
[ редактировать ]Моноклональные антитела дороже производить, чем небольшие молекулы, из-за сложных процессов и общего размера молекул, а также огромных затрат на исследования и разработки, связанные с доставкой нового химического соединения пациентам. Цены на них установлены таким образом, чтобы производители могли окупить обычно большие инвестиционные затраты, а там, где нет контроля над ценами, как, например, в США, цены могут быть выше, если они обеспечивают большую ценность. Семь исследователей из Питтсбургского университета пришли к выводу: «Годовая стоимость терапии моноклональными антителами в онкологии и гематологии примерно на 100 000 долларов выше, чем при других болезненных состояниях», сравнив их в расчете на одного пациента с ценами при сердечно-сосудистых или метаболических расстройствах, иммунологии, инфекционных заболеваниях, аллергия и офтальмология. [37]
Приложения
[ редактировать ]Диагностические тесты
[ редактировать ]Как только моноклональные антитела к данному веществу будут произведены, их можно будет использовать для обнаружения присутствия этого вещества. Белки можно обнаружить с помощью вестерн-блоттинга и иммунодот -блоттинга . В иммуногистохимии моноклональные антитела можно использовать для обнаружения антигенов в фиксированных срезах ткани, и аналогичным образом иммунофлуоресценцию можно использовать для обнаружения вещества либо в замороженных срезах ткани, либо в живых клетках.
Аналитическое и химическое использование
[ редактировать ]Антитела также можно использовать для очистки целевых соединений от смесей методом иммунопреципитации .
Терапевтическое использование
[ редактировать ]Терапевтические моноклональные антитела действуют посредством нескольких механизмов, таких как блокирование функций целевых молекул, индуцирование апоптоза в клетках, экспрессирующих мишень, или путем модуляции сигнальных путей. [38] [39] [40]
Лечение рака
[ редактировать ]Один из возможных методов лечения рака специфичными для раковых клеток включает моноклональные антитела, которые связываются только с антигенами, , и вызывают иммунный ответ против раковой клетки-мишени. Такие mAb можно модифицировать для доставки токсина , радиоизотопа , цитокина или другого активного конъюгата или для создания биспецифических антител , которые могут связываться своими Fab-областями как с целевым антигеном, так и с конъюгатом или эффекторной клеткой. Каждое интактное антитело может связываться с клеточными рецепторами или другими белками с помощью своей области Fc .
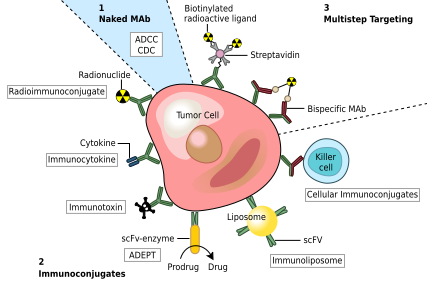
MAb, одобренные FDA для лечения рака, включают: [42]
Аутоиммунные заболевания
[ редактировать ]Моноклональные антитела, используемые при аутоиммунных заболеваниях , включают инфликсимаб и адалимумаб , которые эффективны при ревматоидном артрите , болезни Крона , язвенном колите и анкилозирующем спондилите благодаря своей способности связываться с TNF-α и ингибировать его . [43] Базиликсимаб и даклизумаб ингибируют IL-2 на активированных Т-клетках и тем самым помогают предотвратить острое отторжение трансплантата почки. [43] Омализумаб ингибирует человеческий иммуноглобулин Е (IgE) и полезен при лечении аллергической астмы средней и тяжелой степени .
Примеры терапевтических моноклональных антител
[ редактировать ]Моноклональные антитела для исследовательских целей можно найти непосредственно у поставщиков антител или с помощью специализированной поисковой системы, такой как CiteAb . Ниже приведены примеры клинически важных моноклональных антител.
| Основная категория | Тип | Приложение | Механизм/Цель | Режим |
|---|---|---|---|---|
| Анти- воспалительный | инфликсимаб [43] | ингибирует ФНО-α | химерный | |
| адалимумаб | ингибирует ФНО-α | человек | ||
| устекинумаб | блокирует интерлейкины IL-12 и IL-23 | человек | ||
| базиликсимаб [43] |
| ингибирует IL-2 на активированных Т-клетках | химерный | |
| даклизумаб [43] |
| ингибирует IL-2 на активированных Т-клетках | гуманизированный | |
| омализумаб |
| ингибирует человеческий иммуноглобулин Е (IgE) | гуманизированный | |
| Противораковый | гемтузумаб [43] |
| нацеливает поверхностный антиген миелоидных клеток CD33 на лейкемии клетки | гуманизированный |
| алемтузумаб [43] | нацеливает антиген CD52 на Т- и В-лимфоциты | гуманизированный | ||
| ритуксимаб [43] |
| нацеливается на фосфопротеин CD20 на B-лимфоцитах | химерный | |
| трастузумаб |
| нацелен на рецептор HER2/neu (erbB2) | гуманизированный | |
| нимотузумаб |
| EGFR Ингибитор | гуманизированный | |
| цетуксимаб |
| EGFR Ингибитор | химерный | |
| панитумумаб |
| EGFR Ингибитор | человек | |
| бевацизумаб и ранибизумаб |
| ингибирует VEGF | гуманизированный | |
| Противораковые и противовирусные | бавитуксимаб [44] |
| иммунотерапия , нацелена на фосфатидилсерин [44] | химерный |
| Противовирусное средство |
| иммунотерапия , нацелена на белок-шип SARS-CoV-2 | человек | |
| бамланивимаб/этезевимаб [46] |
| иммунотерапия , нацелена на белок-шип SARS-CoV-2 | человек | |
| Сотровимаб [47] |
| иммунотерапия , нацелена на белок-шип SARS-CoV-2 | человек | |
| Другой | паливизумаб [43] |
| ингибирует слитый белок RSV (F) | гуманизированный |
| абциксимаб [43] |
| ингибирует рецептор GpIIb/IIIa на тромбоцитах | химерный |
COVID-19
[ редактировать ]препаратов моноклональных антител бамланивимаб/этесевимаб и касиривимаб/имдевимаб, выдало разрешение на экстренное использование США В 2020 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов чтобы сократить количество госпитализаций, посещений отделений неотложной помощи и смертей из-за COVID-19 . [45] [46] В сентябре 2021 года администрация Байдена закупила моноклональные антитела Regeneron на сумму 2,9 миллиарда долларов США по цене 2100 долларов США за дозу, чтобы сократить дефицит. [48]
По состоянию на декабрь 2021 года тесты на нейтрализацию in vitro показали, что терапия моноклональными антителами (за исключением сотровимаба и тиксагевимаба/цилгавимаба ) вряд ли будет активна в отношении варианта Омикрон. [49]
В течение 2021–2022 годов два Кокрейновских обзора обнаружили недостаточно доказательств использования нейтрализующих моноклональных антител для лечения инфекций COVID-19. [50] [51] Обзоры относились только к людям, которые не были вакцинированы против COVID-19, и только к вариантам COVID-19, существовавшим во время исследований, а не к более новым вариантам, таким как Омикрон. [51]
В марте 2024 года пемивибарт , препарат на основе моноклональных антител, получил от FDA США разрешение на экстренное использование в качестве доконтактной профилактики для защиты некоторых лиц с умеренным и тяжелым иммунодефицитом от COVID-19. [52] [53]
Побочные эффекты
[ редактировать ]Некоторые моноклональные антитела, такие как бевацизумаб и цетуксимаб , могут вызывать различные побочные эффекты. [54] Эти побочные эффекты можно разделить на общие и серьезные побочные эффекты. [55]
Некоторые распространенные побочные эффекты включают в себя:
Среди возможных серьезных побочных эффектов можно выделить: [56]
- Анафилаксия
- Кровотечение
- Артериальные и венозные тромбы
- Аутоиммунный тиреоидит
- Гипотиреоз
- Гепатит
- Сердечная недостаточность
- Рак
- Анемия
- Снижение количества лейкоцитов
- Стоматит
- Энтероколит
- Желудочно-кишечная перфорация
- Мукозит
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Гельбоин Х.В. «Метаболизм лекарств и канцерогенов, опосредованный цитохромом P450, с использованием моноклональных антител» . home.ccr.cancer.gov . Архивировано из оригинала 15 октября 2004 года . Проверено 2 апреля 2018 г.
- ^ Гелбоин Х.В. , Крауш К.В., Гонсалес Ф.Дж., Ян Т.Дж. (ноябрь 1999 г.). «Ингибирующие моноклональные антитела к ферментам цитохрома P450 человека: новый путь для открытия лекарств» . Тенденции в фармакологических науках . 20 (11): 432–438. дои : 10.1016/S0165-6147(99)01382-6 . ПМИД 10542439 .
- ^ Лю Дж.К. (11 сентября 2014 г.). «История разработки моноклональных антител – прогресс, оставшиеся проблемы и будущие инновации» . Анналы медицины и хирургии . 3 (4): 113–116. дои : 10.1016/j.amsu.2014.09.001 . ISSN 2049-0801 . ПМЦ 4284445 . ПМИД 25568796 .
- ^ Вальдманн Т.А. (июнь 1991 г.). «Моноклональные антитела в диагностике и терапии». Наука . 252 (5013): 1657–1662. Бибкод : 1991Sci...252.1657W . дои : 10.1126/science.2047874 . ПМИД 2047874 . S2CID 19615695 .
- ^ Тэнси Э.М., Каттералл П.П. (июль 1994 г.). «Моноклональные антитела: семинар-свидетель в современной истории медицины» . Медицинская история . 38 (3): 322–327. дои : 10.1017/s0025727300036632 . ПМЦ 1036884 . ПМИД 7934322 .
- ^ Швабер Дж., Коэн Э.П. (август 1973 г.). «Гибридный клон соматических клеток человека и мыши, секретирующий иммуноглобулины обоих родительских типов». Природа . 244 (5416): 444–447. дои : 10.1038/244444a0 . ПМИД 4200460 . S2CID 4171375 .
- ^ Камбросио А., Китинг П. (1992). «Между фактом и техникой: начало гибридомной технологии». Журнал истории биологии . 25 (2): 175–230. дои : 10.1007/BF00162840 . ПМИД 11623041 . S2CID 45615711 .
- ^ Jump up to: а б с Маркс Л.В. «История Цезаря Мильштейна и моноклональных антител» . WhatisBiotechnology.org . Проверено 23 сентября 2020 г.
- ^ Рихманн Л., Кларк М., Вальдманн Х., Винтер Дж. (март 1988 г.). «Изменение человеческих антител для терапии» . Природа . 332 (6162): 323–327. Бибкод : 1988Natur.332..323R . дои : 10.1038/332323a0 . ПМИД 3127726 . S2CID 4335569 .
- ^ Альтманн Д.М. (ноябрь 2018 г.). «Задача, достойная Нобелевской премии: иммунология рака и использование иммунитета к опухолевым неоантигенам» . Иммунология . 155 (3): 283–284. дои : 10.1111/imm.13008 . ПМК 6187215 . ПМИД 30320408 .
- ^ Надлер Л.М., Робертс В.К. (октябрь 2007 г.). «Ли Маршалл Надлер, доктор медицинских наук: разговор с редактором» . Слушания . 20 (4). Национальные институты здравоохранения: 381–389. дои : 10.1080/08998280.2007.11928327 . ПМК 2014809 . ПМИД 17948113 .
- ^ Шпикер-Полет Х., Сетупати П., Ям ПК, Найт К.Л. (сентябрь 1995 г.). «Моноклональные антитела кролика: создание партнера по слиянию для получения гибридом кролика-кролика» . Труды Национальной академии наук Соединенных Штатов Америки . 92 (20): 9348–9352. Бибкод : 1995PNAS...92.9348S . дои : 10.1073/pnas.92.20.9348 . ПМК 40982 . ПМИД 7568130 .
- ^ Чжан Ю.Ф., Фунг Ю., Гао В., Кава С., Хасан Р., Пастан И. и др. (май 2015 г.). «Новые моноклональные антитела с высоким сродством распознают неперекрывающиеся эпитопы мезотелина для мониторинга и лечения мезотелиомы» . Научные отчеты . 5 : 9928. Бибкод : 2015NatSR...5E9928Z . дои : 10.1038/srep09928 . ПМЦ 4440525 . ПМИД 25996440 .
- ^ Ян Дж, Шен М.Х. (2006). «Слияние клеток, опосредованное полиэтиленгликолем». Ядерное перепрограммирование . Методы Мол Биол. Том. 325. стр. 59–66. дои : 10.1385/1-59745-005-7:59 . ISBN 1-59745-005-7 . ПМИД 16761719 .
- ^ Комитет Национального исследовательского совета (США) по методам производства моноклональных антител. «Рекомендация 1: Краткое описание : Производство моноклональных антител». Вашингтон (округ Колумбия): National Academies Press (США); 1999. ISBN 978-0309075114
- ^ Jump up to: а б с Хо М (июнь 2018 г.). «Первая редакционная статья: В поисках волшебных пуль» . Терапия антителами . 1 (1): 1–5. дои : 10.1093/abt/tby001 . ПМК 6086361 . ПМИД 30101214 .
- ^ Jump up to: а б Хо М., Фенг М., Фишер Р.Дж., Рейдер С., Пастан I (май 2011 г.). «Новое высокоаффинное человеческое моноклональное антитело к мезотелину» . Международный журнал рака . 128 (9): 2020–2030 гг. дои : 10.1002/ijc.25557 . ПМЦ 2978266 . ПМИД 20635390 .
- ^ Сибер С., Рос Ф., Тори И., Тифенталер Г., Калуца К., Лифке В. и др. (2014). «Надежная высокопроизводительная платформа для создания функциональных рекомбинантных моноклональных антител с использованием кроличьих B-клеток из периферической крови» . ПЛОС ОДИН . 9 (2): e86184. Бибкод : 2014PLoSO...986184S . дои : 10.1371/journal.pone.0086184 . ПМЦ 3913575 . ПМИД 24503933 .
- ^ Вардеманн Х., Юрасов С., Шефер А., Янг Дж.В., Меффре Э., Нуссенцвейг М.К. (сентябрь 2003 г.). «Преобладающая продукция аутоантител ранними предшественниками В-клеток человека» . Наука . 301 (5638): 1374–1377. Бибкод : 2003Sci...301.1374W . дои : 10.1126/science.1086907 . ПМИД 12920303 . S2CID 43459065 .
- ^ Кельш К., Чжэн Нью-Йорк, Чжан К., Дьюти А., Хелмс С., Матиас М.Д. и др. (июнь 2007 г.). «Класс зрелых B-клеток, переключенных на IgD, у здоровых людей является аутореактивным» . Журнал клинических исследований . 117 (6): 1558–1565. дои : 10.1172/JCI27628 . ПМК 1866247 . ПМИД 17510706 .
- ^ Смит К., Гарман Л., Раммерт Дж., Чжэн Н.Ю., Капра Дж.Д., Ахмед Р. и др. (1 января 2009 г.). «Быстрое получение полностью человеческих моноклональных антител, специфичных к вакцинирующему антигену» . Протоколы природы . 4 (3): 372–384. дои : 10.1038/nprot.2009.3 . ПМК 2750034 . ПМИД 19247287 .
- ^ Дьюти Дж.А., Содорай П., Чжэн Н.Ю., Кельш К.А., Чжан К., Святковски М. и др. (январь 2009 г.). «Функциональная анергия в субпопуляции наивных В-клеток здоровых людей, которые экспрессируют аутореактивные рецепторы иммуноглобулина» . Журнал экспериментальной медицины . 206 (1): 139–151. дои : 10.1084/jem.20080611 . ПМЦ 2626668 . ПМИД 19103878 .
- ^ Хуанг Дж., Дориа-Роуз Н.А., Лонго Н.С., Лауб Л., Лин КЛ., Тёрк Э. и др. (октябрь 2013 г.). «Выделение моноклональных антител человека из В-клеток периферической крови» . Протоколы природы . 8 (10): 1907–1915. дои : 10.1038/nprot.2013.117 . ПМЦ 4844175 . ПМИД 24030440 .
- ^ Власак Дж., Ионеску Р. (декабрь 2008 г.). «Гетерогенность моноклональных антител, выявленная зарядочувствительными методами». Современная фармацевтическая биотехнология . 9 (6): 468–481. дои : 10.2174/138920108786786402 . ПМИД 19075686 .
- ^ Бек А., Вурч Т., Байи С., Корвая Н. (май 2010 г.). «Стратегии и проблемы для следующего поколения терапевтических антител». Обзоры природы. Иммунология . 10 (5): 345–352. дои : 10.1038/nri2747 . ПМИД 20414207 . S2CID 29689097 .
- ^ Хавли Л.А., Госвами С., Хатчинсон Р., Квонг З.В., Ян Дж., Ван Х и др. (2010). «Варианты заряда IgG1: выделение, характеристика, свойства связывания in vitro и фармакокинетика у крыс» . МАБ . 2 (6): 613–624. дои : 10.4161/mabs.2.6.13333 . ПМК 3011216 . ПМИД 20818176 .
- ^ Чжан Т., Бурре Дж., Кано Т. (август 2011 г.). «Выделение и характеристика вариантов терапевтического заряда антител с использованием катионообменной хроматографии». Журнал хроматографии А. 1218 (31): 5079–5086. дои : 10.1016/j.chroma.2011.05.061 . ПМИД 21700290 .
- ^ Ратор А.С., Винкль Х. (январь 2009 г.). «Качество по дизайну для биофармацевтики». Природная биотехнология . 27 (1): 26–34. дои : 10.1038/nbt0109-26 . ПМИД 19131992 . S2CID 5523554 .
- ^ ван дер Шут Дж.М., Феннеманн Ф.Л., Валенте М., Долен Ю., Хагеманс И.М., Беккер А.М. и др. (август 2019 г.). «Функциональная диверсификация антител, продуцируемых гибридомами, с помощью геномной инженерии CRISPR/HDR» . Достижения науки . 5 (8): eaaw1822. Бибкод : 2019SciA....5.1822V . дои : 10.1126/sciadv.aaw1822 . ПМК 6713500 . ПМИД 31489367 .
- ^ Сигел Д.Л. (январь 2002 г.). «Технология рекомбинантных моноклональных антител». Клиническая и биологическая трансфузия . 9 (1): 15–22. дои : 10.1016/S1246-7820(01)00210-5 . ПМИД 11889896 .
- ^ «Доктор Георгий Печеник» . Выпускники ЛМБ . МРЦ Лаборатория молекулярной биологии (ЛМБ). 17 сентября 2009 года. Архивировано из оригинала 23 декабря 2012 года . Проверено 17 ноября 2012 г.
- ^ Шмитц У., Версмольд А., Кауфманн П., Франк Х.Г. (2000). «Фаговый дисплей: молекулярный инструмент для генерации антител – обзор». Плацента . 21 (Приложение А): S106–S112. дои : 10.1053/plac.1999.0511 . ПМИД 10831134 .
- ^ Чжан Ю.Ф., Хо М. (сентябрь 2016 г.). «Гуманизация высокоаффинных антител, нацеленных на глипикан-3 при гепатоцеллюлярной карциноме» . Научные отчеты . 6 : 33878. Бибкод : 2016NatSR...633878Z . дои : 10.1038/srep33878 . ПМК 5036187 . ПМИД 27667400 .
- ^ Булианна Г.Л., Ходзуми Н., Шульман М.Дж. (1984). «Производство функциональных химерных антител мыши/человека». Природа . 312 (5995): 643–646. Бибкод : 1984Natur.312..643B . дои : 10.1038/312643a0 . ПМИД 6095115 . S2CID 4311503 .
- ^ Чадд Х.Э., Чамов С.М. (апрель 2001 г.). «Технология терапевтической экспрессии антител». Современное мнение в области биотехнологии . 12 (2): 188–194. дои : 10.1016/S0958-1669(00)00198-1 . ПМИД 11287236 .
- ^ Лонберг Н., Хузар Д. (1995). «Человеческие антитела от трансгенных мышей». Международные обзоры иммунологии . 13 (1): 65–93. дои : 10.3109/08830189509061738 . ПМИД 7494109 .
- ^ Эрнандес И., Ботт С.В., Патель А.С., Вольф К.Г., Хосподар А.Р., Сампаткумар С. и др. (февраль 2018 г.). «Цены на терапию моноклональными антителами: выше, если они используются при раке?». Американский журнал управляемого медицинского обслуживания . 24 (2): 109–112. ПМИД 29461857 .
- ^ Бридвелд (февраль 2000 г.). «Терапевтические моноклональные антитела» . Ланцет . 355 (9205): 735–740. дои : 10.1016/S0140-6736(00)01034-5 . ПМИД 10703815 . S2CID 43781004 .
- ^ Австралийский врач (2006 г.). «Терапия моноклональными антителами доброкачественных заболеваний» . Австралийский врач . 29 (5): 130–133. дои : 10.18773/austprescr.2006.079 .
- ^ Розенн (сентябрь 2023 г.). «Моноклональная война: арсенал антител и мишени для расширенного применения» . Иммуно . 3 (3): 346–357. дои : 10.3390/immuno3030021 .
- ^ Изменено из Картер П. (ноябрь 2001 г.). «Повышение эффективности лечения рака на основе антител». Обзоры природы. Рак . 1 (2): 118–129. дои : 10.1038/35101072 . ПМИД 11905803 . S2CID 10169378 .
- ^ Такимото Ч., Кальво Э. (1 января 2005 г.) «Принципы онкологической фармакотерапии» в Паздуре Р., Вагмане Л.Д., Кампхаузене К.А., Хоскинсе В.Дж. (редакторы). Лечение рака. Архивировано 4 октября 2013 г. в Wayback Machine.
- ^ Jump up to: а б с д и ж г час я дж Позвонил HP (2003). Фармакология . Эдинбург: Черчилль Ливингстон. На стр. 241 приведены примеры инфликсимаба, базиликсимаба, абциксимаба, даклизумаба, паливусамаба, гемтузумаба, алемтузумаба и ритуксимаба, а также механизм и способ действия. ISBN 978-0443071454 .
- ^ Jump up to: а б «Бавитуксимаб – Авид Биосервисс» . АдисИнсайт . Springer Nature Switzerland AG.
- ^ Jump up to: а б «Обновление о коронавирусе (COVID-19): FDA разрешает использование моноклональных антител для лечения COVID-19» . США Управление по контролю за продуктами и лекарствами (FDA) (пресс-релиз). 21 ноября 2020 г. Проверено 21 ноября 2020 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе . - ^ Jump up to: а б «FDA разрешает использовать моноклональные антитела для лечения COVID-19» . США Управление по контролю за продуктами и лекарствами (FDA) (пресс-релиз). 9 февраля 2021 г. Проверено 10 февраля 2021 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе . - ^ «Письмо о разрешении на аварийное использование» (PDF) . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 16 декабря 2021 г. Проверено 6 января 2022 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе . - ^ Бернштейн Л. (14 сентября 2021 г.). «Администрация Байдена пытается предотвратить нехватку моноклональных антител» . Вашингтон Пост . ISSN 0190-8286 . Проверено 21 декабря 2021 г.
- ^ Козлов М. (декабрь 2021 г.). «Омикрон превосходит ключевые методы лечения антителами против COVID в ранних тестах». Природа . дои : 10.1038/d41586-021-03829-0 . ПМИД 34937889 . S2CID 245442677 .
- ^ Кройцбергер Н., Хирш С., Чай К.Л., Томлинсон Е., Хосрави З., Попп М. и др. (сентябрь 2021 г.). «Моноклональные антитела, нейтрализующие SARS-CoV-2, для лечения COVID-19» . Кокрановская база данных систематических обзоров . 2021 (9): CD013825. дои : 10.1002/14651858.cd013825.pub2 . ПМК 8411904 . ПМИД 34473343 .
- ^ Jump up to: а б Хирш С., Парк Ю.С., Пьехотта В., Чай К.Л., Эсткур Л.Дж., Монсеф И. и др. (июнь 2022 г.). «Моноклональные антитела, нейтрализующие SARS-CoV-2, для профилактики COVID-19» . Кокрановская база данных систематических обзоров . 2022 (6): CD014945. дои : 10.1002/14651858.cd014945.pub2 . ПМК 9205158 . ПМИД 35713300 .
- ^ Макмиллан С (5 апреля 2024 г.). «FDA разрешает препарат «Пемгарда» от COVID для пациентов из группы высокого риска» . Йельская медицина . Проверено 8 апреля 2024 г.
- ^ Каваццони П. (3 апреля 2024 г.). «EUA 122 Инвивид Пемгарда LOA» . Управление по контролю за продуктами и лекарствами США. Архивировано из оригинала 8 апреля 2024 года . Проверено 8 апреля 2024 г.
- ^ «Моноклональные антитела для лечения рака» . Американское онкологическое общество . Проверено 19 апреля 2018 г.
- ^ «Лекарства от рака на основе моноклональных антител: как они работают» . Клиника Мэйо . Проверено 19 апреля 2018 г.
- ^ Jump up to: а б Огбру О (12 октября 2022 г.). Дэвис С.П. (ред.). «Моноклональные антитела: список, типы, побочные эффекты и использование FDA (рак)» . МедицинаНет . Проверено 19 апреля 2018 г.
Дальнейшее чтение
[ редактировать ]- Раевский К. (ноябрь 2019 г.). «Появление и рост моноклональных антител». Природа . 575 (7781): 47–49. Бибкод : 2019Natur.575...47R . дои : 10.1038/d41586-019-02840-w . ПМИД 31686050 .
- Кимбалл Дж.А. «Моноклональные антитела» . Страницы биологии Кимбалла .
Внешние ссылки
[ редактировать ]- Моноклональные + антитела Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)
- Antibodypedia , виртуальный репозиторий с открытым доступом, публикующий данные и комментарии по любым антителам, доступным научному сообществу.
- Справочник по очистке антител. Архивировано 5 декабря 2008 г. в Wayback Machine.
